Myeloïde suppressorcel

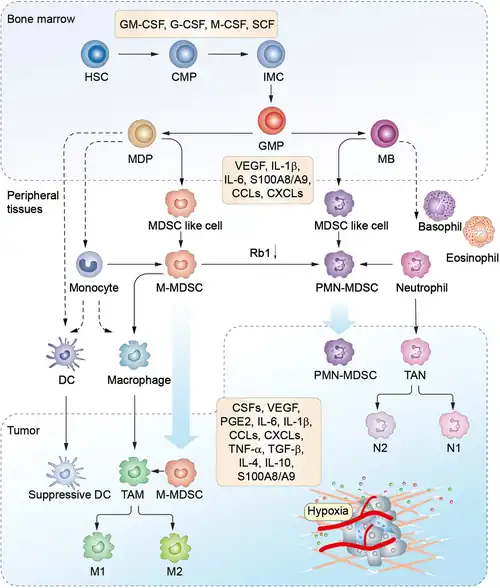
Myeloïde suppressorcellen (Engels: Myeloid-derived suppressor cells (MDSCs)) vormen een heterogene groep immuuncellen uit de myeloïde lijn (dat deel van de bloedcelvorming in het beenmerg uit hematopoëtische stamcellen waarin de zogeheten myeloïde elementen van het bloed (erytrocyten, granulocyten, monocyten, trombocyten) worden aangemaakt). De term myeloïde suppressorcel is afkomstig uit een artikel uit 2007 in Cancer Research van Gabrilovich et al. Publicaties uit 2008 hebben aangetoond dat er twee subpopulaties van MDSC bestaan: mononucleaire MDSC (M-MDSC) en polymorfonucleaire of granulocytaire MDSC (PMN-MDSC). M-MDSC lijkt op de monocyt in het bloed, terwijl PMN-MDSC fysiek verwant is aan de neutrofiele granulocyt.[1]
MDSC's breiden zich uit onder pathologische omstandigheden zoals chronische infectie en kanker, als gevolg van veranderde hematopoëse.[2] MDSC's verschillen van andere myeloïde celtypen doordat ze immuunonderdrukkende eigenschappen hebben, in tegenstelling tot immuunstimulerende eigenschappen. Net als andere bloedcellen interageren MDSC's met immuunceltypen zoals T-cellen, dendritische cellen, macrofagen en NK-cellen om hun functies te reguleren. Tumoren met een hoge mate van infiltratie door MDSC's zijn in verband gebracht met een slechte afloop van de ziekte bij de patiënt en resistentie tegen therapieën.[3][4][5][6] MDSCs can also be detected in the blood. In patients with breast cancer, levels of MDSC in blood are about 10-fold higher than normal.[7] MDSC's kunnen ook in het bloed worden gedetecteerd. Bij patiënten met borstkanker zijn de MDSC-waarden in het bloed ongeveer 10 keer hoger dan normaal.[7] De grootte van het myeloïde suppressorcompartiment wordt gezien als een belangrijke factor voor het succes of falen van kankerimmunotherapie, wat het belang van dit celtype voor de menselijke pathofysiologie benadrukt.[8] Een hoog niveau van MDSC-infiltratie in de tumormicro-omgeving correleert met kortere overlevingstijden van patiënten met kankers en zou resistentie tegen checkpointremmertherapie kunnen bemiddelen.[9]
Myeloïde suppressorcellen kunnen ook worden geïsoleerd bij gezonde individuen, maar in kleinere aantallen. Er is geopperd dat myeloïde suppressorcellen, onder fysiologische omstandigheden, deelnemen aan de regulatie van het immuunsysteem en het handhaven van tolerantie. Myeloïde suppressorcellen zouden bijvoorbeeld kunnen bijdragen aan de tolerantie van de moeder voor de foetus tijdens de zwangerschap. Hoge niveaus van MDSC's blijven aanwezig bij de baby bij de geboorte en kunnen schadelijke ontstekingen onderdrukken als gevolg van microbiële kolonisatie en blootstelling aan omgevingsantigenen. Dit kan echter ook de ontwikkeling van beschermende immuunreacties tegen infecties belemmeren.[10]
Vorming
MDSC's worden uit hematopoëtische stamcellen gevormd wanneer hematopoëtische processen worden verstoord, veroorzaakt door verschillende ziekten.[11][12] Groeiende tumoren van kankerpatiënten produceren cytokinen en andere stoffen die de ontwikkeling van MDSC's beïnvloeden. Tumorcellijnen brengen koloniestimulerende factoren (G-CSF en GM-CSF) en IL-6 tot overexpressie, die de ontwikkeling van MDSC's met een immuunonderdrukkende functie in vivo bevorderen. Andere cytokinen, waaronder IL-10, IL-1, VEGF en PGE2, zijn in verband gebracht met de vorming en regulatie van MDSC's. GM-CSF bevordert de synthese van MDSC's vanuit het beenmerg, en de transcriptiefactor c/EBP reguleert de ontwikkeling van MDSC's in het beenmerg en in tumoren. STAT3 bevordert ook de ontwikkeling van MDSC's, terwijl IRF8 MDSC-inducerende signalen zou kunnen tegengaan.[13]
MDSC's migreren als onrijpe cellen van het beenmerg naar perifere weefsels (of tumoren), waar ze differentiëren tot volwassen macrofagen, dendritische cellen en neutrofiele granulocytlen zonder onderdrukkende fenotypes onder homeostatische omstandigheden, maar gepolariseerd raken bij blootstelling aan pro-inflammatoire verbindingen, chemokines en cytokines. In de tumormicro-omgeving onderdrukken ze de antitumor-immuunrespons. De aanwezigheid van MDSC's is in verband gebracht met de progressie van darmkanker, tumorangiogenese en metastasen. Naast de productie van NO en ROS scheiden MDSC's immuunregulerende cytokines uit zoals TNF, TGF-β en IL-10. Er zijn subpopulaties van MDSC's die enkele gemeenschappelijke onderdrukkende kenmerken hebben, maar ook hun eigen unieke kenmerken; verschillende subpopulaties kunnen in verschillende gebieden van hetzelfde weefsel of tumor worden aangetroffen.[14] Tumor-infiltrerende MDSC's ontwikkelen zich als reactie op omgevingsfactoren en verhogen de regulatie van CD38 (dat NAD uit de omgeving verwijdert en nodig is voor mitochondriale biosynthese), PDL-1 (een immuun checkpoint-eiwit) en LOX1 (bevordert de consumptie van vetzuren en de bèta-oxidatie). Tumor-infiltrerende MDSC's scheiden ook exosomen uit die de immuunrespons tegen tumoren kunnen remmen.
Onrijpe myeloïde cellen bij de vorming van MDSC's
Myeloïde suppressorcellen zijn een recent ontdekt celtype afkomstig uit het beenmerg. Ze hebben kenmerken van onrijpe stamcellen met immunomodulerende eigenschappen. Ze worden zelfs gebruikt in onderzoek naar therapeutische strategieën tegen zowel auto-immuunziekten als verergering van ontstekingen, die met name interessant zijn voor het centraal zenuwstelsel. Het grootste nadeel van MDSC's is dat ze alleen worden gevormd bij ontstekingen en daarom vaak worden verzameld bij zieke proefpersonen.[15][16][17]
Een recent onderzoek van de Universiteit van Salamanca heeft echter aangetoond dat onrijpe myeloïde cellen (IMC's), de voorlopers van MDSC's, ook onder pathologische omstandigheden een potentiële immunosuppressieve activiteit hebben.[18] IMC's kunnen rechtstreeks worden verzameld uit gezond beenmerg, wat een klinisch meer haalbare bron is. Onder pathologische omstandigheden gedragen IMC's zich dan als MDSC's die immunomodulerend werken. In die zin kunnen IMC's direct worden gebruikt, waardoor ze niet bij zieke proefpersonen moeten worden verzameld.[18]
Bovendien zijn IMC's veelbelovende adjuvantia bij neurochirurgie. De toepassing ervan bij hersenchirurgie voorkwam de door deze procedure veroorzaakte schade bij muizen vrijwel volledig, waarschijnlijk door de modulatie van de ontstekingspatronen.[18] In die zin hebben IMC's een directe preklinische toepassing om de secundaire effecten die inherent zijn aan elke hersenoperatie te minimaliseren, met name in een zieke omgeving.
MDSC-differentiatie
Bij mensen
MDSC's zijn afkomstig van beenmergvoorlopercellen, meestal als gevolg van een verstoorde myeloipoëse veroorzaakt door verschillende pathologieën. Bij kankerpatiënten scheiden groeiende tumoren een verscheidenheid aan cytokinen en andere moleculen uit, die belangrijke signalen zijn die betrokken zijn bij de regeneratie van MDSC. Tumorcellijnen die koloniestimulerende factoren (bijv. G-CSF en GM-CSF) tot overexpressie brengen, worden al lang gebruikt in in-vivomodellen voor MDSC-regeneratie. GM-CSF, G-CSF en IL-6 maken de in-vitro regeneratie van MDSC mogelijk, die hun onderdrukkende functie in vivo behouden. Naast CSF zijn andere cytokinen, zoals IL-6, IL-10, VEGF, PGE2 en IL-1, betrokken bij de ontwikkeling en regulatie van MDSC.[3][19] De myeloïde differentiatiecytokine GM-CSF is een sleutelfactor in de productie van MDSC uit het beenmerg,[20] en het is aangetoond dat de c/EBPβ-transcriptiefactor een sleutelrol speelt bij de regeneratie van in vitro uit beenmerg afkomstige en in vivo tumorgeïnduceerde MDSC. Bovendien bevordert STAT3 de differentiatie en expansie van MDSC en is gesuggereerd dat IRF8 MDSC-inducerende signalen tegenwerkt.
Bij muizen
Muizen-MDSC's hebben twee verschillende fenotypen die hen onderscheiden in monocytaire MDSC's of granulocytaire MDSC's. De relatie tussen deze twee subtypen blijft controversieel, aangezien ze respectievelijk sterk lijken op monocyten en neutrofiele granulocyten. Hoewel de differentiatiepaden van monocyten en neutrofiele granulocyten in het beenmerg antagonistisch zijn en afhankelijk van de relatieve expressie van IRF8 en c/EBP-transcriptiefactoren (en er daarom geen directe voorloper-nakomeling-link is tussen deze twee myeloïde celtypen), lijkt dit niet het geval te zijn voor MDSC's. Monocytaire MDSC's lijken voorlopers te zijn van granulocytaire subsets die zowel in vitro als in vivo zijn aangetoond.[20][21] Dit differentiatieproces wordt versneld na tumorinfiltratie en mogelijk aangestuurd door de hypoxische tumormicro-omgeving.
Fenotype
Veel laboratoria hebben geprobeerd oppervlaktemarkers te identificeren (immunofenotypering) om MDSC's te karakteriseren en te isoleren. Bij muizen worden MDSC's aangetroffen in de bloedcelpopulatie die zowel de Gr1 (Ly-6G/C+) als CD11b+ markers tot expressie brengen. Omdat de Gr1-marker feitelijk tot expressie wordt gebracht door twee oppervlaktemoleculen, Ly6C en Ly6G, worden muizen-MDSC's klassiek onderverdeeld in monocytaire MDSC's (Ly6C++) en granulocytaire MDSC's (Ly6G++).
Bij mensen is de fenotypische definitie minder gestandaardiseerd. Menselijke monocytaire MDSC's worden vaak gedefinieerd als expressie van de myeloïde markers CD33 en CD14 en een lage HLA-DR-waarde. Granulocytaire MDSC's worden over het algemeen gedefinieerd als CD11b+CD14−CD33+ CD15+.[22]
NK-cellen
De uitputting van MDSC's bij muizen met leverkanker verhoogt de cytotoxiciteit van NK-cellen, de NKG2D-expressie en de productie van Interferon gamma (IFNg) aanzienlijk en induceert NK-celenergie.[23] Uitputting van MDSC's herstelde de functie van aangetaste leverNK-cellen. Een MDSC afkomstig van chronische ontsteking veroorzaakte disfunctie van T- en NK-cellen, samen met downregulatie van de TCR z-keten (CD247). Het immunosuppressieve milieu beïnvloedt direct CD247, wat cruciaal is voor het initiëren van immuunreacties. MDSC's, die werken via membraangebonden TGF-β1, remmen NK-cellen in tumordragende gastheren vanwege de activiteit van TGF-β1 op MDSC's. Daarom onderdrukken MDSC's constitutief leverNK-cellen in tumordragende gastheren via TGF-β1 op MDSC's.[24]
B-cellen
Een aantal studies heeft melding gemaakt van MDSC-regulatie van B-celreacties op activatoren en mitogenen die niet door MHC worden gereguleerd, evenals antigeenspecifieke T-celreacties. Een infectie met het retrovirus LP-BM5 kan bij muizen leiden tot verworven immuundeficiëntie, wat leidt tot sterk immunosuppressieve CD11bCGr-1CLy6CC MDSC's. Deze cellen onderdrukken T- en B-cellen door middel van signalering via stikstofmonoxide (NO).[25]
Dendritische cellen
Immuunreacties tegen tumoren en infecties worden gereguleerd door myeloïde suppressorcellen en dendritische cellen (DC's). De combinatie van LPS- en IFNg-behandeling van beenmerg-afgeleide MDSC's beperkt de DC-vorming en verbetert de MDSC-onderdrukkende werking. MDSC's blijken de effectiviteit van vaccinatie met het kankervaccin op basis van dendritische cellen te verminderen. De MDSC-frequentie heeft geen effect op de DC-productie of overleving, maar veroorzaakt wel een dosisafhankelijke vermindering van de DC-rijping. Hoge CD14CHLA-DR/lage celfrequenties kunnen de DC-rijping onderdrukken en de DC-functie verminderen, beide cruciaal voor de effectiviteit van vaccinatie. Daarom zou de balans tussen MDSC's en DC's cruciaal kunnen zijn bij de behandeling van tumoren en infecties. De balans tussen MDSC's en DC's zou dus een belangrijke rol kunnen spelen bij tumor- en infectietherapie.[26][27]
Activiteit/functie
MDSC's zijn immuunonderdrukkend en spelen een rol bij het in stand houden en de progressie van tumoren. MDSC's belemmeren ook therapieën die kanker behandelen met zowel immunotherapie als andere niet-immuunmethoden.[1] MDSC-activiteit werd oorspronkelijk beschreven als suppressor van T-cellen, met name van cytotoxische T-celreacties. Het werkingsspectrum van MDSC-activiteit omvat ook NK-cellen, dendritische cellen en macrofagen. De suppressoractiviteit van MDSC wordt bepaald door hun vermogen om de effectorfunctie van lymfocyten te remmen. Remming kan door verschillende mechanismen worden veroorzaakt. Het wordt voornamelijk toegeschreven aan de effecten van het metabolisme van L-arginine (L-arginine is de natuurlijke actieve biologische vorm). Een andere belangrijke factor die de activiteit van MDSC beïnvloedt, is onderdrukkende ROS.[3][28]
Effect van BMR-vaccinatie
MDSC's kunnen ook een positieve regulerende rol spelen. Er wordt gesteld dat het BMR-vaccin MDSC-populaties stimuleert bij mensen die het vaccin nemen, waardoor septische ontstekingen en sterfte worden geremd. Dit geldt niet alleen voor mazelen, bof en rodehond, maar ook voor door COVID-19 geïnduceerde cytokine-ontstekingen.[29] Deze vaccinstimulatie van MDSC's lijkt noch permanent noch chronisch te zijn. Hoewel MDSC's in bepaalde gevallen immunosuppressief zijn, is het BMR-vaccin zelf immunostimulerend.
Kankerbevorderende effecten van myeloïde suppressorcellen
Myeloïde suppressorcellen gebruiken verschillende mechanismen om de antitumorimmuniteit te verzwakken en tumorprogressie te bevorderen. Ze dragen bij aan de vorming van een immuunonderdrukkende omgeving, ondersteunen ook tumorprogressie en veroorzaken resistentie tegen kankerbehandeling.
Expressie van checkpointmoleculen
Uit talrijke onderzoeken is gebleken dat myeloïde suppressorcellen de expressie van PD-1-ligand (Programmed cell death protein 1) verhogen. Door het ligand voor PD-1 hoog tot expressie te brengen onderdrukken ze T-cellen die de kankercel anders zou aanvallen.[30][31] Tumor-infiltrerende myeloïde suppressorcellen vertonen consequent een hogere expressie van het PD-1-ligand dan hun perifere tegenhangers, wat duidt op aanpassing aan de hypoxische micro-omgeving[30],.[31] Bovendien vormen myeloïde suppressorcellen ook het cytotoxische T-cel-geassocieerd antigeen 4 (CTLA-4), hoewel het specifieke regulatiemechanisme onduidelijk is [15]. Bovendien vormen myeloïde suppressorcellen ook het cytotoxische T-cel-geassocieerd antigeen 4 (CTLA-4), hoewel het specifieke regulatiemechanisme onduidelijk is.[32]
Uitputting van aminozuren die nodig zijn voor T-celrespons
Van myeloïde suppressorcellen is bekend dat ze T-cellen beroven van essentiële aminozuren die nodig zijn voor het metabolisme en de functie van T-cellen. Grote hoeveelheden factoren afkomstig van de tumormicro-omgeving, zoals hypoxie-geïnduceerde factor, groeifactor, interleukine-4, interleukine-10 en interferon-gamma, kunnen de expressie van CAT-2B (een kationische aminozuurtransporteur) en arginase in myeloïde suppressorcellen induceren.[33][34] CAT-2B transporteert snel extracellulair L-arginine naar myeloïde suppressorcellen, waar het vervolgens wordt afgebroken tot ureum en L-ornithine onder katalyse van arginase.[34] Argininedeficiëntie in de extracellulaire ruimte kan leiden tot verlies van de CD3ζ-keten en remming van de T-celproliferatie.[35] Bij kankerpatiënten geven myeloïde suppressorcellen arginase af aan de extracellulaire omgeving, wat ook leidt tot het verbruik van extracellulaire L-arginine en op dezelfde manier de remming van T-cellen verder vergemakkelijkt.[36] Opmerkelijk is dat myeloïde suppressiorcellen T-celinactivatie induceren door cel-tot-cel-overdracht van methylglyoxal naar T-cellen. Methylglyoxal werkt door cytosolisch L-arginine uit te putten en ook door L-arginine-bevattende eiwitten niet-functioneel te maken door glycatie.[37] Bovendien kunnen myeloïde suppressorcellen cystine absorberen en het metaboliseren tot cysteïne. Vanwege het ontbreken van een neutrale aminozuurtransporter kunnen myeloïde suppressorcellen echter geen cysteïne exporteren naar de extracellulaire omgeving, wat leidt tot cysteïne tekort voor T-celactivering.[38] Tryptofaanuitputting door indoleamine 2,3-dioxygenase in myeloïde suppressorcellen kan T-cel-autofagie en celdood induceren.[39]
Productie van stikstofoxide, reactieve zuurstofsoorten en reactieve stikstofcomponenten
Myeloïde suppressorcellen scheiden talrijke reactieve zuurstofcomponenten en reactieve stikstofcomponenten uit om de T-celfunctie te verstoren. Verhoogde induceerbare stikstofoxidesynthase in myeloïde suppressorcellen metaboliseert L-arginine tot stikstofmonoxide en citrulline. Stikstofmonoxide induceert verschillende moleculaire blokkades in T-cellen, waaronder interferentie met interleukine 2-receptorsignalering en nitrering van T-celreceptoren die specifiek zijn voor peptiden die worden gevormd door myeloïde suppressorcellen.[40][41] Reactieve zuurstofcomponenten omvatten zuurstofradicalen (zoals het superoxide-anion, ) en hydroxylgroepen. Radicalen en niet-radicalen (zoals waterstofperoxide, H2O2) worden in grote hoeveelheden gegenereerd door de NADPH-oxidase-isovorm (NOX-2) in myeloïde suppressorcellen. Reactieve zuurstofsoorten spelen niet alleen een belangrijke rol bij de oxidatieve stress van myeloïde suppressorcellen, maar katalyseren ook de nitrering van het T-celreceptor/CD8-complex om interacties tussen T-celreceptor/major histocompatibility complex en peptide te voorkomen.[42] reageert snel met stikstofmonoxide om reactieve stikstofsoorten te produceren, zoals peroxynitriet, die nitrering/nitrosylering van T-celreceptor/CD8-complexen kunnen induceren en verder een verminderde peptideherkenning door het T-celreceptor/major histocompatibility complex kunnen veroorzaken.[43][44] Meer specifiek induceren reactieve stikstofsoorten posttranslationele modificatie van CCL2, wat verantwoordelijk is voor een verminderde affiniteit van CCL2 voor zijn receptor, waardoor de rekrutering van tumor-infiltrerende T-cellen in tumorweefsels wordt geremd. Dit leidt echter niet tot een volledig verlies van de bloedcelfunctie, aangezien bloedcellen hogere niveaus van CCR2-expressie hebben dan cytotoxische T-cellen.[45]
Adenosine en zijn receptoren
Adenosine speelt een rol in de myeloïde-afgeleide suppressie van T-cellen.[46] Hypoxische tumorweefsels geven grote hoeveelheden adenosinetrifosfaat af in de extracellulaire ruimte, die onmiddellijk worden afgebroken tot adenosines. In dit proces zet de ectonucleotidase CD39 adenosinetrifosfaat om in adenosinedifosfaat en/of adenosinemonofosfaat, en katalyseert CD73 de vorming van adenosine uit adenosinemonofosfaat.[47] Geaccumuleerde extracellulaire adenosines activeren downstreamsignaalroutes via adenosinereceptoren: A2AR, A2BR (beide worden over het algemeen geassocieerd met ernstige immunosuppressie), A1R en A3R. In de tumormicro-omgeving worden deze adenosinerge moleculen (CD39, CD73, A2AR en A2BR) over het algemeen tot expressie gebracht door tumorcellen, evenals door stroma- en immuuncellen, waardoor een positieve terugkoppeling ontstaat. Deze terugkoppeling genereert een constante stroom adenosinen, die niet alleen de ontwikkeling en het immunosuppressieve vermogen van myeloïde suppressorcellen bevorderen, maar ook de activiteit van kankerbestrijdende witte bloedcellen, waaronder T-cellen, dendritische cellen en NK-cellen, beïnvloeden.[48]
Verstoring van het T-celvervoer
Myeloïde suppressorcellen gebruiken verschillende methoden om het vervoer van T-cellen te veranderen. ADAM17 (disintegrine en metalloproteinase 17), tot expressie gebracht op myeloïde suppressorcellen, splitst direct het ectodomein van L-selectine (CD62L) op naïeve T-cellen, naïef: nog nooit in contact geweest met haar specifieke antigeen, om te voorkomen dat ze migreren naar perifere lymfeklieren en tumorlocaties.[49] Downregulatie van CD44 en CD162 op T-cellen door stikstofmonoxide geproduceerd door M-type myeloïde suppressorcellen kan de invasie en weefselinfiltratie van T-cellen belemmeren.[50] Stikstofmonoxide verlaagt de expressie van E-selectine op tumorvaten, waardoor het vervoer van T-cellen naar tumorweefsels wordt geremd.[51]
MDSC-remming
Remming van MDSC-cellen kan worden uitgevoerd op het niveau van expansie of volledige activering, wanneer hun suppressorfunctie onderdrukt is. Factoren die betrokken zijn bij de expansie van MDSC-cellen worden ook gebruikt bij hun neutralisatie. SCF-signalering wordt geremd door de KIT-receptor te blokkeren, wat de interactie van de hematopoëtische stamcel met het CSF-cytokine mogelijk maakt. Het resultaat is een verminderde expressie van MDSC-cellen en tegelijkertijd een lagere natieve angiogenese. Het is ook mogelijk om de VEGF-factor te blokkeren met specifieke antilichamen, die worden gebruikt bij patiënten met uigezaaide niercelkanker. Het is aangetoond dat deze procedure het aantal CD11b+VEGFR1+ MDSC-celpopulaties in perifeer bloed vermindert.[52] Een afname van de MDSC-expansie wordt ook waargenomen bij remming van de PIR-B-receptor (leukocytenimmunoglobulinereceptorfamilie B, lid 3 – LILRB3), die differentiatie van onrijpe myeloïde cellijnen voorkomt. MDSC's met een genetisch verwijderde PIR-B-receptor worden getransformeerd tot M1-macrofagen, die bij binnenkomst in het perifere bloed de STAT1/NFκB-signalering initiëren. Vervolgens neemt het aantal M1-macrofagen sterk toe, neemt het suppressieve vermogen van MDSC's af en worden regulatoire T-cellen geactiveerd.[13]
De functies van MDSC's worden geremd door de productie van suppressieve stoffen te reguleren. Cyclo-oxygenase 2 is nodig voor de productie van prostaglandine 2 (PGE2), wat een verhoogde expressie van arginase 1 door MDSC's triggert. Onderdrukking van cyclo-oxygenase 2 leidt tot een afname van arginase 1, terwijl tegelijkertijd de antitumorrespons van T-cellen wordt versterkt en de effectiviteit van immunotherapie toeneemt. Fosfodiësterremmers verminderen ook de expressie van arginase 1 en iNOS, dat wordt gebruikt om suppressieve functies te reguleren bij patiënten met groeiende tumoren. De effectiviteit van remmers van reactieve zuurstofcomponenten (ROS) is tot nu toe alleen aangetoond bij muizen met tumorhaarden. De productie van suppressor factoren door MDSC cellen kan ook gereguleerd worden door sommige farmacologische routes, zoals niet-steroïde anti-inflammatoire geneesmiddelen, die de ROS productie verminderen; of nitroaspirine, dat de activiteit van de enzymen arginase 1 en iNOS reguleert.[52]
Chemotherapeutische middelen die tot verschillende klassen behoren, blijken MDSC te remmen. Hoewel dit effect mogelijk secundair is aan de remming van hematopoëtische voorlopercellen, kan er aanleiding zijn om de selectiviteit te onderzoeken op basis van de al lang bekende differentiële effecten van deze middelen op immunocompetente cellen en macrofagen.[3] In 2015 werden MDSC's vergeleken met immunogene bloedcellen, wat wijst op een groep belangrijke signaalroutes die de procarcinogene functies van MDSC's controleren.[53] Veel van deze routes zijn bekende doelwitten van chemotherapiemedicijnen met sterke antikankereigenschappen.
In mei 2018 waren er nog geen door de FDA goedgekeurde geneesmiddelen ontwikkeld die MDSC's aanpakken, maar de experimentele INB03-variant is al in de vroege klinische studies terechtgekomen.[54][55]
Er is veelbelovend bewijs voor het remmen van Galectin-3 als therapeutisch doelwit om MDSC's te verminderen.[56][57] In een klinische proef in fase 1b van GR-MD-02, ontwikkeld door Galectin Therapeutics, observeerden onderzoekers een significante afname in de frequentie van suppressieve myeloïde suppressorcellen na behandeling bij melanoompatiënten.[58]
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Myeloid-derived suppressor cell op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Cellule myéloïde suppressive op de Franstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- 1 2 (en) Ostrand-Rosenberg S (4 maart 2021). Myeloid-Derived Suppressor Cells: Facilitators of Cancer and Obesity-Induced Cancer. Annual Review of Cancer Biology 5 (1): 17–38. ISSN: 2472-3428. DOI: 10.1146/annurev-cancerbio-042120-105240.
- ↑ Li T, Li X, Chen YH (May 2020). c-Rel is a myeloid checkpoint for cancer immunotherapy. Nature Cancer 1 (5): 507–517. PMID 33458695. PMC 7808269. DOI: 10.1038/s43018-020-0061-3.
- 1 2 3 4 Mantovani A (December 2010). The growing diversity and spectrum of action of myeloid-derived suppressor cells. European Journal of Immunology 40 (12): 3317–20. PMID 21110315. DOI: 10.1002/eji.201041170.
- ↑ Allavena P, Mantovani A (February 2012). Immunology in the clinic review series; focus on cancer: tumour-associated macrophages: undisputed stars of the inflammatory tumour microenvironment. Clinical and Experimental Immunology 167 (2): 195–205. PMID 22235995. PMC 3278685. DOI: 10.1111/j.1365-2249.2011.04515.x.
- ↑
- ↑ Gabrilovich DI, Ostrand-Rosenberg S, Bronte V (March 2012). Coordinated regulation of myeloid cells by tumours. Nature Reviews. Immunology 12 (4): 253–68. PMID 22437938. PMC 3587148. DOI: 10.1038/nri3175.
- 1 2 Safarzadeh E, Hashemzadeh S, Duijf PH, Mansoori B, Khaze V, Mohammadi A, Kazemi T, Yousefi M, Asadi M, Mohammadi H, Babaie F, Baradaran B (April 2019). Circulating myeloid-derived suppressor cells: An independent prognostic factor in patients with breast cancer. Journal of Cellular Physiology 234 (4): 3515–3525. PMID 30362521. DOI: 10.1002/jcp.26896.
- ↑ Kodach LL, Peppelenbosch MP (August 2021). Targeting the Myeloid-Derived Suppressor Cell Compartment for Inducing Responsiveness to Immune Checkpoint Blockade Is Best Limited to Specific Subtypes of Gastric Cancers.. Gastroenterology 161 (2). PMID 33798523. DOI: 10.1053/j.gastro.2021.03.047.
- ↑ Awad RM, De Vlaeminck Y, Maebe J, Goyvaerts C, Breckpot K (31 augustus 2018). Turn Back the TIMe: Targeting Tumor Infiltrating Myeloid Cells to Revert Cancer Progression. Frontiers in Immunology 9. PMID 30233579. PMC 6127274. DOI: 10.3389/fimmu.2018.01977.
- ↑ Soren Gantt, Ana Gervassi, Heather Jaspan et Helen Horton, « The Role of Myeloid-Derived Suppressor Cells in Immune Ontogeny », Frontiers in Immunology, vol. 5, 2014 (ISSN 1664-3224, DOI 10.3389/fimmu.2014.00387, consulté le 8 avril 2018). Gearchiveerd op 4 oktober 2024.
- ↑ Fan D, Raychoudhury S, Ai W (13 mei 2020). KLF4-Mediated Plasticity of Myeloid-Derived Suppressor Cells (MDSCs) (IntechOpen). DOI: 10.5772/intechopen.89151.
- ↑ Ouzounova M, Lee E, Piranlioglu R, El Andaloussi A, Kolhe R, Demirci MF, Marasco D, Asm I, Chadli A, Hassan KA, Thangaraju M, Zhou G, Arbab AS, Cowell JK, Korkaya H (April 2017). Monocytic and granulocytic myeloid derived suppressor cells differentially regulate spatiotemporal tumour plasticity during metastatic cascade. Nature Communications 8 (1). PMID 28382931. PMC 5384228. DOI: 10.1038/ncomms14979.
- 1 2 OCHANDO, Jordi C.; CHEN, Shu Hsia. Myeloid-derived suppressor cells in transplantation and cancer. Immunologic Research. 2012-12-01, roč. 54, čís. 1–3, s. 275–285. Dostupné online [cit. 2018-02-06. ISSN 0257-277X. doi:10.1007/s12026-012-8335-1.]
- ↑ Gabrilovich D (1 januari 2013). Abstract IA7: Regulation of myeloid-derived suppressor cells in tumor micro-environment. Cancer Research 73: IA7 (American Association for Cancer Research). DOI: 10.1158/1538-7445.tumimm2012-ia7.
- ↑ (en) Melero-Jerez, Carolina, Alonso-Gómez, Aitana, Moñivas, Esther, Lebrón-Galán, Rafael, Machín-Díaz, Isabel (July 2020). The proportion of myeloid-derived suppressor cells in the spleen is related to the severity of the clinical course and tissue damage extent in a murine model of multiple sclerosis. Neurobiology of Disease 140. PMID 32278882. DOI: 10.1016/j.nbd.2020.104869. Gearchiveerd op 13 maart 2025.
- ↑ (en) Melero-Jerez, Carolina, Fernández-Gómez, Beatriz, Lebrón-Galán, Rafael, Ortega, Maria Cristina, Sánchez-de Lara, Irene (April 2021). Myeloid-derived suppressor cells support remyelination in a murine model of multiple sclerosis by promoting oligodendrocyte precursor cell survival, proliferation, and differentiation. Glia 69 (4): 905–924. ISSN: 0894-1491. PMID 33217041. PMC 7894183. DOI: 10.1002/glia.23936.
- ↑ (en) Melero-Jerez, Carolina, Ortega, María Cristina, Moliné-Velázquez, Verónica, Clemente, Diego (March 2016). Myeloid derived suppressor cells in inflammatory conditions of the central nervous system. Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease 1862 (3): 368–380. PMID 26527182. DOI: 10.1016/j.bbadis.2015.10.015. Gearchiveerd op 13 maart 2025.
- 1 2 3 (en) del Pilar, Carlos, Garrido-Matilla, Lucía, del Pozo-Filíu, Lucía, Lebrón-Galán, Rafael, Arias, Raúl F. (14 februari 2024). Intracerebellar injection of monocytic immature myeloid cells prevents the adverse effects caused by stereotactic surgery in a model of cerebellar neurodegeneration. Journal of Neuroinflammation 21 (1). ISSN: 1742-2094. PMID 38355633. PMC 10867997. DOI: 10.1186/s12974-023-03000-8.
- ↑ Gros A, Turcotte S, Wunderlich JR, Ahmadzadeh M, Dudley ME, Rosenberg SA (October 2012). Myeloid cells obtained from the blood but not from the tumor can suppress T-cell proliferation in patients with melanoma. Clinical Cancer Research 18 (19): 5212–23. PMID 22837179. PMC 6374773. DOI: 10.1158/1078-0432.CCR-12-1108.
- 1 2 Liechtenstein T, Perez-Janices N, Gato M, Caliendo F, Kochan G, Blanco-Luquin I, Van der Jeught K, Arce F, Guerrero-Setas D, Fernandez-Irigoyen J, Santamaria E, Breckpot K, Escors D (September 2014). A highly efficient tumor-infiltrating MDSC differentiation system for discovery of anti-neoplastic targets, which circumvents the need for tumor establishment in mice. Oncotarget 5 (17): 7843–57. PMID 25151659. PMC 4202165. DOI: 10.18632/oncotarget.2279.
- ↑ Youn JI, Kumar V, Collazo M, Nefedova Y, Condamine T, Cheng P, Villagra A, Antonia S, McCaffrey JC, Fishman M, Sarnaik A, Horna P, Sotomayor E, Gabrilovich DI (March 2013). Epigenetic silencing of retinoblastoma gene regulates pathologic differentiation of myeloid cells in cancer. Nature Immunology 14 (3): 211–20. PMID 23354483. PMC 3578019. DOI: 10.1038/ni.2526.
- ↑ Gabrilovich, Dmitry I., Ostrand-Rosenberg, Suzanne, Bronte, Vincenzo (22 maart 2012). Coordinated regulation of myeloid cells by tumours. DOI:10.1038/nri3175, 253–268. Gearchiveerd op 20 maart 2023.
- ↑ Zhao Y, Wu T, Shao S, Shi B, Zhao Y (February 2016). Phenotype, development, and biological function of myeloid-derived suppressor cells. Oncoimmunology 5 (2). PMID 27057424. PMC 4801459. DOI: 10.1080/2162402x.2015.1004983.
- ↑ Engwerda C (26 april 2013). Faculty Opinions recommendation of Tumor necrosis factor-α blocks differentiation and enhances the suppressive activity of immature myeloid cells during chronic inflammation.. DOI: 10.3410/f.718002932.793475483.
- ↑ Green KA, Cook WJ, Green WR (February 2013). Myeloid-derived suppressor cells in murine retrovirus-induced AIDS inhibit T- and B-cell responses in vitro that are used to define the immunodeficiency. Journal of Virology 87 (4): 2058–2071. PMID 23221564. PMC 3571497. DOI: 10.1128/jvi.01547-12.
- ↑ Greifenberg V, Ribechini E, Rössner S, Lutz MB (October 2009). Myeloid-derived suppressor cell activation by combined LPS and IFN-gamma treatment impairs DC development. European Journal of Immunology 39 (10): 2865–2876. PMID 19637228. DOI: 10.1002/eji.200939486.
- ↑ Poschke I, Mao Y, Adamson L, Salazar-Onfray F, Masucci G, Kiessling R (June 2012). Myeloid-derived suppressor cells impair the quality of dendritic cell vaccines. Cancer Immunology, Immunotherapy 61 (6): 827–838. PMID 22080405. PMC 11028420. DOI: 10.1007/s00262-011-1143-y.
- ↑ Kusmartsev S, Nefedova Y, Yoder D, Gabrilovich DI (January 2004). Antigen-specific inhibition of CD8+ T cell response by immature myeloid cells in cancer is mediated by reactive oxygen species. Journal of Immunology 172 (2): 989–99. PMID 14707072. DOI: 10.4049/jimmunol.172.2.989.
- ↑ Fidel, Paul L., Noverr, Mairi C. (19 June 2020). Could an Unrelated Live Attenuated Vaccine Serve as a Preventive Measure To Dampen Septic Inflammation Associated with COVID-19 Infection?. mBio 11 (3). PMID 32561657. PMC 7304316. DOI: 10.1128/mbio.00907-20.
- 1 2 Zaeem Noman, Giacomo Desantis, Bassam Janji et Meriem Hasmim, « PD-L1 is a novel direct target of HIF-1α, and its blockade under hypoxia enhanced MDSC-mediated T cell activation », Journal of Experimental Medicine, vol. 211, no 5, 28 avril 2014, p. 781–790 (ISSN 1540-9538 et ISSN 0022-1007, PMID 24778419, PMCID PMC4010891, DOI 10.1084/jem.20131916, lire en ligne [archive], consulté le 10 mai 2024)
- 1 2 Joseph P. Antonios, Horacio Soto, Richard G. Everson et Diana Moughon, « Immunosuppressive tumor-infiltrating myeloid cells mediate adaptive immune resistance via a PD-1/PD-L1 mechanism in glioblastoma », Neuro-Oncology, 23 janvier 2017, now287 (ISSN 1522-8517 et ISSN 1523-5866, PMID 28115578, PMCID PMC5464463, DOI 10.1093/neuonc/now287, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Yago Pico de Coaña, Isabel Poschke, Giusy Gentilcore et Yumeng Mao, « Ipilimumab Treatment Results in an Early Decrease in the Frequency of Circulating Granulocytic Myeloid-Derived Suppressor Cells as well as Their Arginase1 Production », Cancer Immunology Research, vol. 1, no 3, 1er septembre 2013, p. 158–162 (ISSN 2326-6066 et ISSN 2326-6074, DOI 10.1158/2326-6066.CIR-13-0016, lire en ligne [archive], consulté le 10 mai 2024). Gearchiveerd op 28 juni 2025.
- ↑ Paulo C. Rodríguez et Augusto C. Ochoa, « Arginine regulation by myeloid derived suppressor cells and tolerance in cancer: mechanisms and therapeutic perspectives », Immunological Reviews, vol. 222, no 1, avril 2008, p. 180–191 (ISSN 0105-2896 et 1600-065X, PMID 18364002, PMCID PMC3546504, DOI 10.1111/j.1600-065X.2008.00608.x, lire en ligne [archive], consulté le 10 mai 2024)
- 1 2 Cansu Cimen Bozkus, Bennett D. Elzey, Scott A. Crist et Lesley G. Ellies, « Expression of Cationic Amino Acid Transporter 2 Is Required for Myeloid-Derived Suppressor Cell–Mediated Control of T Cell Immunity », The Journal of Immunology, vol. 195, no 11, 1er décembre 2015, p. 5237–5250 (ISSN 0022-1767 et ISSN 1550-6606, PMID 26491198, PMCID PMC4655170, DOI 10.4049/jimmunol.1500959, lire en ligne [archive], consulté le 10 mai 2024). Gearchiveerd op 29 april 2025.
- ↑ Arnold H. Zea, Paulo C. Rodriguez, Kirk S. Culotta et Claudia P. Hernandez, « l-Arginine modulates CD3ζ expression and T cell function in activated human T lymphocytes », Cellular Immunology, vol. 232, nos 1-2, novembre 2004, p. 21–31 (ISSN 0008-8749, DOI 10.1016/j.cellimm.2005.01.004, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Paulo C. Rodriguez, Marc S. Ernstoff, Claudia Hernandez et Michael Atkins, « Arginase I–Producing Myeloid-Derived Suppressor Cells in Renal Cell Carcinoma Are a Subpopulation of Activated Granulocytes », Cancer Research, vol. 69, no 4, 15 février 2009, p. 1553–1560 (ISSN 0008-5472 et ISSN 1538-7445, PMID 19201693, PMCID PMC2900845, DOI 10.1158/0008-5472.CAN-08-1921, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Tobias Baumann, Andreas Dunkel, Christian Schmid et Sabine Schmitt, « Regulatory myeloid cells paralyze T cells through cell–cell transfer of the metabolite methylglyoxal », Nature Immunology, vol. 21, no 5, mai 2020, p. 555–566 (ISSN 1529-2916, DOI 10.1038/s41590-020-0666-9, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Minu K. Srivastava, Pratima Sinha, Virginia K. Clements et Paulo Rodriguez, « Myeloid-Derived Suppressor Cells Inhibit T-Cell Activation by Depleting Cystine and Cysteine », Cancer Research, vol. 70, no 1, 1er janvier 2010, p. 68–77 (ISSN 0008-5472 et ISSN 1538-7445, PMID 20028852, PMCID PMC2805057, DOI 10.1158/0008-5472.CAN-09-2587, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Jinpu Yu, Weijiao Du, Fang Yan et Yue Wang, « Myeloid-Derived Suppressor Cells Suppress Antitumor Immune Responses through IDO Expression and Correlate with Lymph Node Metastasis in Patients with Breast Cancer », The Journal of Immunology, vol. 190, no 7, 1er avril 2013, p. 3783–3797 (ISSN 0022-1767 et ISSN 1550-6606, DOI 10.4049/jimmunol.1201449, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Alessandra Mazzoni, Vincenzo Bronte, Alberto Visintin et Jessica H. Spitzer, « Myeloid Suppressor Lines Inhibit T Cell Responses by an NO-Dependent Mechanism », The Journal of Immunology, vol. 168, no 2, 15 janvier 2002, p. 689–695 (ISSN 0022-1767 et ISSN 1550-6606, DOI 10.4049/jimmunol.168.2.689, lire en ligne [archive], consulté le 10 mai 2024)]
- ↑ Srinivas Nagaraj, Adam G. Schrum, Hyun-Il Cho et Esteban Celis, « Mechanism of T Cell Tolerance Induced by Myeloid-Derived Suppressor Cells », The Journal of Immunology, vol. 184, no 6, 15 mars 2010, p. 3106–3116 (ISSN 0022-1767 et ISSN 1550-6606, PMID 20142361, PMCID PMC2832724, DOI 10.4049/jimmunol.0902661, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Cesar A. Corzo, Matthew J. Cotter, Pingyan Cheng et Fendong Cheng, « Mechanism Regulating Reactive Oxygen Species in Tumor-Induced Myeloid-Derived Suppressor Cells », The Journal of Immunology, vol. 182, no 9, 1er mai 2009, p. 5693–5701 (ISSN 0022-1767 et ISSN 1550-6606, PMID 19380816, PMCID PMC2833019, DOI 10.4049/jimmunol.0900092, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Tangying Lu, Rupal Ramakrishnan, Soner Altiok et Je-In Youn, « Tumor-infiltrating myeloid cells induce tumor cell resistance to cytotoxic T cells in mice », The Journal of Clinical Investigation, vol. 121, no 10, 3 octobre 2011, p. 4015–4029 (ISSN 0021-9738, PMID 21911941, PMCID PMC3195459, DOI 10.1172/JCI45862, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Srinivas Nagaraj, Kapil Gupta, Vladimir Pisarev et Leo Kinarsky, « Altered recognition of antigen is a mechanism of CD8+ T cell tolerance in cancer », Nature Medicine, vol. 13, no 7, juillet 2007, p. 828–835 (ISSN 1546-170X, PMID 17603493, PMCID PMC2135607, DOI 10.1038/nm1609, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Barbara Molon, Stefano Ugel, Federica Del Pozzo et Cristiana Soldani, « Chemokine nitration prevents intratumoral infiltration of antigen-specific T cells », Journal of Experimental Medicine, vol. 208, no 10, 19 septembre 2011, p. 1949–1962 (ISSN 1540-9538 et 0022-1007, PMID 21930770, PMCID PMC3182051, DOI 10.1084/jem.20101956, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Sergey Ryzhov, Sergey V. Novitskiy, Anna E. Goldstein et Asel Biktasova, « Adenosinergic Regulation of the Expansion and Immunosuppressive Activity of CD11b+Gr1+ Cells », The Journal of Immunology, vol. 187, no 11, 1er décembre 2011, p. 6120–6129 (ISSN 0022-1767 et 1550-6606, PMID 22039302, PMCID PMC3221925, DOI 10.4049/jimmunol.1101225, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Bertrand Allard, Maria Serena Longhi, Simon C. Robson et John Stagg, « The ectonucleotidases CD 39 and CD 73: Novel checkpoint inhibitor targets », Immunological Reviews, vol. 276, no 1, mars 2017, p. 121–144 (ISSN 0105-2896 et 1600-065X, PMID 28258700, PMCID PMC5338647, DOI 10.1111/imr.12528, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Dipti Vijayan, Arabella Young, Michele W. L. Teng et Mark J. Smyth, « Targeting immunosuppressive adenosine in cancer », Nature Reviews Cancer, vol. 17, no 12, décembre 2017, p. 709–724 (ISSN 1474-1768, DOI 10.1038/nrc.2017.86, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Erica M. Hanson, Virginia K. Clements, Pratima Sinha et Dan Ilkovitch, « Myeloid-Derived Suppressor Cells Down-Regulate L-Selectin Expression on CD4+ and CD8+ T Cells », The Journal of Immunology, vol. 183, no 2, 15 juillet 2009, p. 937–944 (ISSN 0022-1767 et ISSN 1550-6606, PMID 19553533, PMCID PMC2800824, DOI 10.4049/jimmunol.0804253, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Elio Schouppe, Camille Mommer, Kiavash Movahedi et Damya Laoui, « Tumor‐induced myeloid‐derived suppressor cell subsets exert either inhibitory or stimulatory effects on distinct CD 8 + T ‐cell activation events », European Journal of Immunology, vol. 43, no 11, novembre 2013, p. 2930–2942 (ISSN 0014-2980 et 1521-4141, DOI 10.1002/eji.201343349, lire en ligne [archive], consulté le 10 mai 2024)
- ↑ Ahmed E. Gehad, Michael K. Lichtman, Chrysalyne D. Schmults et Jessica E. Teague, « Nitric Oxide–Producing Myeloid-Derived Suppressor Cells Inhibit Vascular E-Selectin Expression in Human Squamous Cell Carcinomas », Journal of Investigative Dermatology, vol. 132, no 11, novembre 2012, p. 2642–2651 (ISSN 0022-202X, PMID 22718118, PMCID PMC3449043, DOI 10.1038/jid.2012.190, lire en ligne [archive], consulté le 10 mai 2024)
- 1 2 GABRILOVICH, Dmitry I.; NAGARAJ, Srinivas. Myeloid-derived suppressor cells as regulators of the immune system. Nature Reviews Immunology. 2009/03, roč. 9, čís. 3, s. 162–174. Dostupné online [cit. 2018-02-06]. ISSN 1474-1741. doi:10.1038/nri2506. Gearchiveerd op 18 december 2025.
- ↑ Gato-Cañas M, Martinez de Morentin X, Blanco-Luquin I, Fernandez-Irigoyen J, Zudaire I, Liechtenstein T, Arasanz H, Lozano T, Casares N, Chaikuad A, Knapp S, Guerrero-Setas D, Escors D, Kochan G, Santamaría E (September 2015). A core of kinase-regulated interactomes defines the neoplastic MDSC lineage. Oncotarget 6 (29): 27160–75. PMID 26320174. PMC 4694980. DOI: 10.18632/oncotarget.4746.
- ↑ INmune Bio Initiates Phase I Clinical Trial Of INB03 May 2018
- ↑ Toor SM, Elkord E (October 2018). Therapeutic prospects of targeting myeloid-derived suppressor cells and immune checkpoints in cancer. Immunology and Cell Biology 96 (9): 888–897. PMID 29635843. DOI: 10.1111/imcb.12054.
- ↑ Wang T, Chu Z, Lin H, Jiang J, Zhou X, Liang X (June 2014). Galectin-3 contributes to cisplatin-induced myeloid derived suppressor cells (MDSCs) recruitment in Lewis lung cancer-bearing mice. Molecular Biology Reports 41 (6): 4069–76. PMID 24615503. DOI: 10.1007/s11033-014-3276-5.
- ↑ Blidner AG, Méndez-Huergo SP, Cagnoni AJ, Rabinovich GA (November 2015). Re-wiring regulatory cell networks in immunity by galectin-glycan interactions. FEBS Letters 589 (22): 3407–18. PMID 26352298. DOI: 10.1016/j.febslet.2015.08.037.
- ↑ Galectin Therapeutics Inc., (20 september 2018). Positive Preliminary Results from Phase 1b Clinical Trial of GR-MD-02 and KEYTRUDA® in Advanced Melanoma and Expansion of the Trial. Gearchiveerd op 27 maart 2019. Persbericht.