Polymorfonucleaire myeloïde suppressorcel
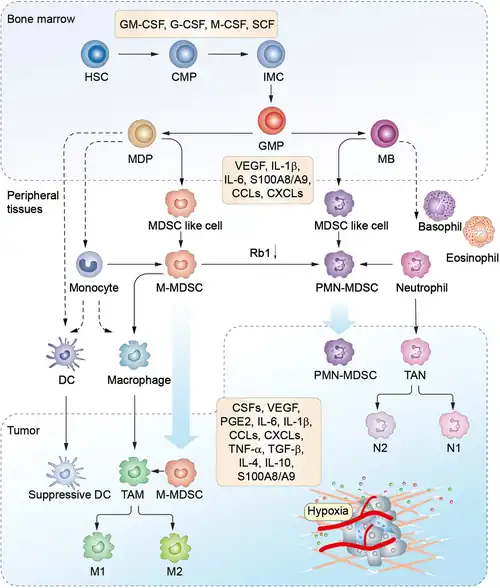
Polymorfonucleaire myeloïde suppressorcellen (Engels:Polymorphonuclear or granulocytic Myeloid-Derived Suppressor Cell (PMN-MDSC)) zijn een subpopulatie van myeloïde suppressorcellen (MDSC's). Ze lijken op neutrofiele granulocyten en hebben een celkern met meerdere lobben dit in tegenstelling tot mononucleaire myeloïde suppressorcellen (M-MDSC), die op monocyten lijken. In 2008 werd het bestaan van deze twee typen gepubliceerd.[1] Ze komen samen met neutrofiele granulocyten voor.
PMN-MDSC communiceren actief met kankercellen via ontstekingsmediatoren en groeifactoren zoals IL-8, IL-17a, CCL2, TNFα, Bv8, VEGFα en TGF-β spelen een belangrijke rol in verschillende aspecten van de verspreiding, invasie en angiogenese van tumorcellen. Na aankomst in de tumormicro-omgeving versterken PMN-MDSC hun pro-tumorigene immunosuppressieve capaciteiten en resistentie tegen apoptose als gevolg van een fenotypische omschakeling gemedieerd door de tumormicro-omgeving. Ze veroorzaken resistentie tegen kankertherapieën, terwijl ze de ziekteprogressie en metastatische verspreiding versnellen.[2]
Bij muizen brengen MDSC's de celoppervlakeiwitten Gr1 en CD11b tot expressie. Gr1 bestaat uit de Ly6C- en Ly6G-markers. Muis PMN-MDSC zijn CD11b+Ly6G+. Menselijke PMN-MDSC zijn CD33dimCD11b+CD15+CD14-HLA-DR−/laag.[3][4] Ook het vetzuurtransporteiwit 2 (FATP2) is een specifieke PMN-MDSC-marker.[2]
De PMN-MDSC in de tumormicro-omgeving heeft een overexpressie van een verscheidenheid aan pro-tumorigene cytokinen, chemokinen en adhesiemoleculen en naast ROS bevatten de cytoplasmatische granula diverse enzymen (myeloperoxidase, elastase en MMP, zoals collagenase (MMP-8) en gelatinase B (MMP-9)). MMP hermodelleert de extracellulaire matrix om de migratie van tumorcellen te bevorderen (door afbraak en herschikking van collageenfibrillen) en versnelt de angiogenese, waardoor de effecten van anti-angiogene moleculen worden tegengegaan. Proteasen, elastase en MMP afkomstig van PMN-MDSC in neutrofiele granulocyt extracellulaire vallen induceren celmotiliteit en proliferatie van slapende tumorcellen door de activering van integrine α3β1-signaalroutes. Samen met in het weefsel aanwezige stromacellen ondersteunt PMN-MDSC ook de vorming van pre-metastatische niches en de kolonisatie en uitgroei van verspreide tumorcellen.[2]
PMN-MDSC kunnen cysteïne, L-arginine en L-tryptofaan metaboliseren, die essentieel zijn voor de werking van T-cellen. Het ontbreken van deze verbindingen stimuleert de differentiatie van T-helpercellen tot regulerende T-cellen en remt de proliferatie van T-cellen en de assemblage van T-celreceptoren, waardoor T-cellen anergetisch worden en niet meer reageren op antigeenspecifieke stimulatie. Bovendien voorkomt nitrering van CCL2 door van MDSC afkomstig stikstofmonoxide de infiltratie van T-cellen in de centrale tumor, waardoor ze beperkt blijven tot het perifere stroma.[2]
PMN-MDSC stimuleren de proliferatie en overleving van cytotoxische T-cellen door hen te voorzien van energierijke lipidevesikels. De nabijheid van PMN-MDSC ten opzichte van cytotoxische T-cellen bevordert de plasticiteit van cytotoxische T-cellen en verhoogt hun metastatische potentieel. In de tumormicro-omgeving versnellen PMN-MDSC's hun eigen lipidetransport, -opname en -opslag door verhoogde expressie van FATP2-, HILDPA- en LOX1-eiwitten.[2]
In de tumormicro-omgeving kunnen cytokinen en chemokinen uit de tumorcellen de normale myelopoëse beïnvloeden en de differentiatie van M-MDSC's tot PMN-MDSC's vergroten.[5]
M-MDSC's kunnen differentiëren tot PMN-MDSC's door transcriptionele inactivatie van het retinoblastoomgen (Rb1).
- ↑ (en) (4 maart 2021). Myeloid-Derived Suppressor Cells: Facilitators of Cancer and Obesity-Induced Cancer. Annual Review of Cancer Biology 5 (1): 17–38. ISSN: 2472-3428. DOI: 10.1146/annurev-cancerbio-042120-105240.
- 1 2 3 4 5 Raskov, H., Orhan, A., Gaggar, S. et al. Neutrophils and polymorphonuclear myeloid-derived suppressor cells: an emerging battleground in cancer therapy. Oncogenesis 11, 22 (2022). https://doi.org/10.1038/s41389-022-00398-3
- ↑ Movahedi K, Guilliams M, Van den Bossche J, Van den Bergh R, Gysemans C et al. 2008. Identification of discrete tumor-induced myeloid-derived suppressor cell subpopulations with distinct T cell-suppressive activity. Blood 111:4233–44MDSC consist of two subtypes: mononuclear MDSC (M-MDSC) and polymorphonuclear/granular MDSC (PMN-MDSC)
- ↑ Youn JI, Nagaraj S, Collazo M, Gabrilovich DI 2008. Subsets of myeloid-derived suppressor cells in tumor-bearing mice. J. Immunol. 181:5791–802
- ↑ Yin K, Xia X, Rui K, Wang T and Wang S (2020) Myeloid-Derived Suppressor Cells: A New and Pivotal Player in Colorectal Cancer Progression. Front. Oncol. 10:610104. doi: 10.3389/fonc.2020.610104