Aangeboren lymfoïde cel
Aangeboren lymfoïde cellen (ILC's) zijn voornamelijk in weefsel aanwezige cellen, die zowel in lymfoïde (immuungeassocieerd) als niet-lymfoïde weefsels worden aangetroffen en zelden in het bloed. Ze komen bijzonder veel voor op slijmvliesoppervlakken en spelen een sleutelrol in de immuniteit van het slijmvlies en homeostase. Kenmerken die hun differentiatie van andere immuuncellen mogelijk maken, zijn onder andere de regelmatige lymfoïde morfologie, de afwezigheid van herschikte antigeenreceptoren op T-cellen en B-cellen (vanwege het ontbreken van het RAG-gen) en fenotypische markers die gewoonlijk aanwezig zijn op myeloïde of dendritische cellen.[1]
Aangeboren lymfoïde cellen zijn de meest recent ontdekte familie van aangeboren immuuncellen, afgeleid van gemeenschappelijke lymfoïde voorlopercellen (CLP's). Als reactie op pathogene weefselschade dragen ILC's bij aan de immuniteit via de secretie van signaalmoleculen en de regulatie van zowel aangeboren als verworven immuuncellen.
Op basis van het verschil in ontwikkelingspaden, fenotype en geproduceerde signaalmoleculen, werden ILC's in 2013 verdeeld in drie groepen: 1, 2 en 3. Na verder onderzoek zijn ze echter nu verdeeld in vijf groepen: NK-cellen, ILC1's, ILC2's, ILC3's en lymfoïde weefselinducerende (LTi) cellen.[2] ILC's zijn betrokken bij meerdere fysiologische functies, waaronder weefselhomeostase, morfogenese, metabolisme, herstel en regeneratie. Veel van hun rollen zijn vergelijkbaar met T-cellen, daarom is gesuggereerd dat ze de aangeboren tegenhangers van T-cellen zijn.[3] De ontregulating van ILC's kan leiden tot immuunpathologie zoals allergie, astma en auto-immuunziekte.[4]
Classificatie
De ontwikkeling van ILC's wordt geïnitieerd als reactie op de aanwezigheid van transcriptiefactoren die worden geactiveerd door de aanwezigheid van omringende micro-omgevingsfactoren, zoals cytokinen, Notch-liganden en het circadiaan ritme (ingebouwde gedragsveranderingen na een dagelijkse cyclus). Eenmaal gerijpt, geven de ILC's cytokinen af. De classificatie van ILC's is daarom gebaseerd op de verschillen in de transcriptiefactor- en cytokineprofielen die verband houden met de ontwikkeling en functie van de verschillende ILC-subtypen.[5]
Groep 1 ILC's
ILC1- en NK-cellijnen divergeren vroeg in hun ontwikkelingspaden en kunnen worden onderscheiden door hun verschillende afhankelijkheid van transcriptiefactoren, hun cytotoxiciteit en de expressie van hun residente marker. NK-cellen zijn cytotoxische cellen die in de bloedbaan circuleren en virusgeïnfecteerde cellen en tumorcellen doden. ILC1's zijn niet-cytotoxische of zwak cytotoxische, in weefsel verblijvende cellen die een rol spelen in de verdediging tegen infecties met virussen en bepaalde bacteriën.
Omdat ILC1's en NK-cellen zowel gedeelde als niet-gedeelde kenmerken hebben, is de classificatie van menselijke ILC1's problematisch geweest. Beide celtypen produceren IFN-γ als hun belangrijkste cytokine en hebben hiervoor de transcriptiefactor T-bet nodig. (T-bet: T-box-expressie in T-cellen)[6] Beide cellen kunnen ook IFN-γ produceren wanneer de cytokinen IL-15 of IL-12 na infectie of verwonding in weefsels worden upgereguleerd, en scheiden TGF-β1 uit in combinatie met IFN-γ wanneer ze worden gestimuleerd. Dit stimuleert de hervorming van het darmepitheel en de extracellulaire matrix.[7] IL-18-costimulatie verhoogt ook significant de IFN-γ-niveaus.[8] De afgifte van IFN-γ stimuleert macrofagen en andere eenkernige fagocyten om een antimicrobieel effect te induceren tegen intracellulaire infecties. Zuurstofradicalen die door beide celtypen worden geproduceerd, helpen ook tegen infecties. ILC1's en NK-cellen kunnen ook TNF-α produceren, wat, afhankelijk van hun moleculaire expressie, ook bijdraagt aan de ontstekingsreactie.
Er zijn verschillen in afhankelijkheid van transcriptiefactoren tussen NK-cellen en ILC1's. Hoewel beide celtypen T-bet gebruiken voor ontwikkeling, zijn NK-cellen aanwezig gebleken in T-bet-deficiënte gastheren, maar ILC1's zijn volledig afhankelijk van de aanwezigheid ervan.[6] De ontwikkeling van NK-cellen is echter volledig afhankelijk van de aanwezigheid van de transcriptiefactor eomesodermine, terwijl ILC1's zich onafhankelijk van de aanwezigheid ervan kunnen ontwikkelen.[6] Dit betekent dat eomesodermine over het algemeen kunnen worden gebruikt als marker voor NK-cellen, wat suggereert dat volwassen NK-cellen Tbet+ eomesodermine+ zijn en ILC1 Tbet+ eomesodermine-.[9]
ILC1's en NK-cellen hebben enkele fenotypische markers gemeen, waaronder: KLRB1 bij muizen, en NK-celreceptoren (NCR's) zoals NKp44 en NKp46 bij zowel mensen als muizen.[10][6] Ze vertonen ook verschillen in fenotypische markers, waaronder de expressie van CD127 op humane ILC1's, die niet op alle NK-cellen aanwezig is. Bovendien wordt NKp80, een marker voor humane NK-cellen, niet tot expressie gebracht op ILC1's. Bij muizen is aangetoond dat CD200R NK-cellen van ILC1's onderscheidt.[11] De relatie tussen de ILC1- en NK-cellijnen blijft onduidelijk vanwege een gebrek aan deze karakteristieke markers die wel aanwezig zijn op sommige NK/ILC1-cellen in bepaalde weefsels, of na bepaalde infecties/ontstekingen. Dit ondersteunt de theorie van de weefselspecifieke functie.[10] Zo is CD127, hoewel tot expressie gebracht door de meeste ILC1's, afwezig in de in de speekselklier aanwezige ILC1's, die ook het vermogen hebben om eomesodermine tot expressie te brengen, een fundamenteel kenmerk van NK-cellen.[12]
Vanwege de productie van granzymen en perforine worden NK-cellen beschouwd als de aangeboren tegenhangers van cytotoxische T-cellen, terwijl ILC1's worden beschouwd als de aangeboren tegenhangers van Th1-cellen, vanwege de exclusieve productie van IFN-γ zonder cytotoxische activiteit.[13]
Groep 2 ILC's
ILC2's komen in weefsels voor en zijn betrokken bij de aangeboren reactie op parasieten, zoals worminfecties, door te helpen bij het herstellen van weefselschade. Ze komen veel voor in de huid,[14][15] longen, lever en darmen.[6][16] Ze worden gekenmerkt door de productie van amfireguline en type 2 cytokinen, waaronder IL-4, IL-5 en IL-13, als reactie op IL-25, TSLP en IL-33.[6] Vanwege hun cytokinesignatuur worden ze beschouwd als de aangeboren tegenhangers van Th2-cellen.
Ze brengen karakteristieke oppervlaktemarkers en receptoren voor chemokinen tot expressie, die betrokken zijn bij de distributie van lymfoïde cellen naar specifieke orgaanlocaties. Bij mensen brengen ILC2's CRTH2, KLRG1, SST2, CD161 en CD25 tot expressie. Bij muizen brengen ILC2's CD44 tot expressie, maar geen CD161.[3]
ILC2's hebben IL-7 nodig voor hun ontwikkeling, wat de fundamentele transcriptiefactoren RORα en GATA3 activeert. GATA3 is ook nodig voor het behoud van de ILC2-functie, waarbij GATA3-deprivatie de ontwikkeling en functie van de cellen remt.
Hoewel ILC2's als homogeen worden beschouwd, kunnen ze worden ingedeeld in subpopulaties van natuurlijke ILC2's (nILC2's) en inflammatoire ILC2's (iILC2's), afhankelijk van hun gevoeligheid voor IL-33 en IL-25. nILC2's zijn degenen die reageren op IL-33 in weefsels in een natuurlijke immuuntoestand, terwijl iILC2's reageren op IL-25 of de wormparasiet. nILC2's brengen meer Thy1 en IL1RL1 tot expressie, en minder KLRG1. iILC2's brengen meer KLRG1 tot expressie en minder Thy1 en IL1RL1. Naast deze subpopulaties wordt een andere populatie, de ILC210-cel, gekenmerkt door zijn vermogen om IL-10 te produceren.[3]
Groep 3 ILC's
ILC3's zijn betrokken bij de aangeboren immuunrespons op extracellulaire bacteriën en schimmels. Ze spelen een sleutelrol in de homeostase van darmbacteriën en bij het reguleren van Th17-celreacties.[17] Volwassen ILC3's van de mens worden voornamelijk aangetroffen in de lamina propria van de darm en de amandelen, maar ze worden ook aangetroffen in de milt, het endometrium, de decidua en de huid.[18]
ILC3's zijn afhankelijk van de transcriptiefactor RORγt voor hun ontwikkeling en functie.[19] Ze brengen RORγt tot expressie als reactie op IL-1β en IL-23, of pathogene signalen.[20] IL-22 is het belangrijkste cytokine dat door ILC3's wordt geproduceerd en speelt een fundamentele rol bij het handhaven van de intestinale homeostase. ILC3's produceren echter een verscheidenheid aan andere cytokinen, waaronder IL-17, IL-22, IFN-γ en GM-CSF, afhankelijk van de omgevingsstimuli.[21]
Er zijn twee subgroepen ILC3's: NK-celreceptor- en NK-celreceptor+ ILC3's. De NK-celreceptor die op muizen-ILC3's wordt weergegeven, is NKp46, vergeleken met NKp44 dat op menselijke ILC3's wordt weergegeven.[21] NKp44+ ILC3's zijn sterk verrijkt in de amandelen en darmen, als exclusieve bron van IL-22.[21] Sommige ILC3's kunnen ook andere NK-celmarkers tot expressie brengen, waaronder NKp30 en CD56.[22] NK-celreceptor- ILC3's produceren voornamelijk IL-17A en IL-17F, en onder bepaalde omstandigheden IL-22.[22] NCR-ILC3's kunnen differentiëren naar NK-celreceptor+ bij verhoogde expressieniveaus van T-bet.[5] Ondanks dat ze NK-celmarkers tot expressie brengen, verschillen ILC3's enorm van NK-cellen, met verschillende ontwikkelingspaden en werkingfuncties.
Lymfoïde weefselinducerende (LTi) cellen
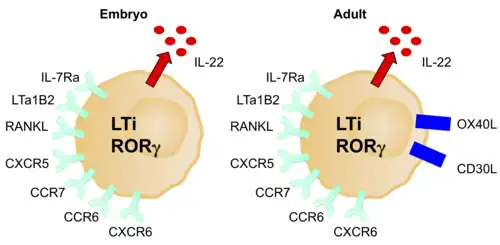
LTi-cellen worden beschouwd als een aparte afstammingslijn vanwege hun unieke ontwikkelingspad, maar worden vaak beschouwd als onderdeel van de ILC3-groep vanwege hun vele vergelijkbare kenmerken. Net als ILC3's zijn LTi-cellen afhankelijk van RORγt. Ze zijn betrokken bij de vorming van secundaire lymfeklieren en de peyerse platen door de ontwikkeling van lymfoïde weefsel te bevorderen, wat ze doen door de werking van lymfotoxine, een lid van de TNF-superfamilie.[6] Ze zijn cruciaal tijdens zowel de embryonale als de volwassen stadia van de ontwikkeling van het immuunsysteem, en daarom zijn LTi-cellen al vroeg in de embryonale ontwikkeling aanwezig in organen en weefsels.[6] Ze spelen een cruciale rol in de organisatie van primair en secundair lymfoïde weefsel en in volwassen lymfoïde weefsel, waarbij ze de verworven immuunrespons reguleren en de structuren van secundair lymfoïde weefsel in stand houden.[24]
Hun productie wordt gestimuleerd door retinezuur, CXCL13, RANK-L en de cytokinen IL-1B, IL-23 en IL-6.[25] Ze brengen c-Kit, CCR6, CD25, CD127 en CD90 tot expressie, maar geen NCR's.[6] De expressie van OX40L is een andere goede marker voor LTi-cellen bij volwassen muizen en mensen.[23] Ze kunnen CD4+/- zijn. Net als ILC3's produceren LTi-cellen na activering voornamelijk IL-17A, IL-17F en IL-22.[23] Ze worden gemedieerd door RANK, TNF, IL-17 en IL-22.
LTi-cellen induceren de expressie van AIRE, het auto-immuun regulerende gen, door de ontwikkeling van embryonale thymus-epitheelcellen mogelijk te maken. Ze doen dit via lymfotoxine α4β7 en RANK-L-signalering. LTi-cellen maken ook het overleven van T-helpercellen mogelijk, en dus ook van immuunreacties op geheugen, in nieuw gevormde lymfeklieren. Ze doen dit via de TNF-superfamilieleden OX40L en CD30L, die signalen afgeven aan T-helpercellen. Deze rol zou kunnen worden gebruikt om auto-immuniteit te voorkomen en geheugenreacties na vaccinatie te verbeteren.[23]
Ontwikkeling
Het begrip van de paden die betrokken zijn bij de ontwikkeling van ILC's is pas de laatste jaren duidelijker geworden, waarbij de kennis voornamelijk gebaseerd is op paden bij muizen.[6] CLP's kunnen differentiëren tot een aantal verschillende celtypen, waaronder T-cellen, B-cellen en ILC's, afhankelijk van de aanwezige cellulaire signalen. Met uitzondering van NK-cellen hebben alle ILC's IL-7-signalering nodig om te overleven. De transcriptionele repressor ID2 lijkt de differentiatie van B- en T-cellen te antagoniseren, wat resulteert in een ID2-afhankelijke voorloper die verder kan differentiëren met afstammingslijnspecifieke transcriptiefactoren.[4]
ILC's zijn recombinatie-activerende gen (RAG)-onafhankelijk; in plaats daarvan zijn ze voor hun ontwikkeling afhankelijk van cytokinesignalering via de gemeenschappelijke cytokine-receptor gamma-keten en de JAK3-kinase-route.[26]
Vroege ontwikkeling
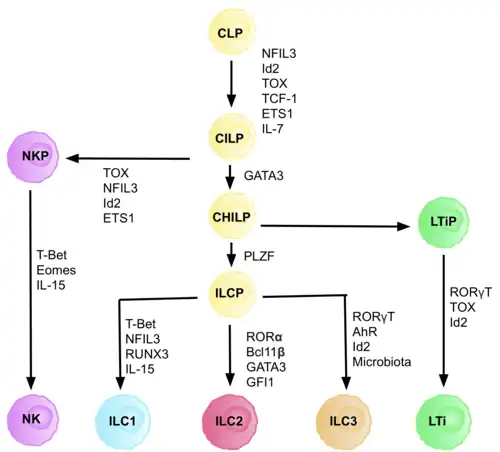
ILC's zijn afgeleid van gemeenschappelijke aangeboren lymfoïde voorlopercellen (CILP's), die op hun beurt weer afgeleid zijn van gemeenschappelijke lymfoïde voorlopercellen (CLP's), die het vermogen hebben om te differentiëren tot een aantal verschillende lymfoïde celtypen, waaronder T- en B-cellen.[6] CILP's kunnen vervolgens differentiëren tot NK-celprecursoren (NKP's), of de meer recent beschreven gemeenschappelijke helper aangeboren lymfoïde voorlopercellen (CHILP's).[6] CHILP's kunnen vervolgens differentiëren tot lymfoïde weefselinducerende voorlopercellen (LTiP's) en aangeboren lymfoïde celprecursoren (ILCP's). De factoren die aanwezig zijn in de micro-omgeving bepalen de progressie van CLP's richting specifieke ILC-subtypen, waaronder Notch-liganden, cytokines, circadiaan ritme en de expressie van transcriptiefactoren.
Identificatie van de ILC-voorlopercel (ILCP)
De ontwikkeling van CLP's tot CILP's en verder tot ILC's vereist de transcriptiefactor ID2 om de onderdrukking van het lot van lymfoïde cellen die T- en B-cellen genereren te bemiddelen. Dit gebeurt door de activiteit van E-box-transcriptiefactoren (E2A, E2-2 en TCF12) te verminderen, die cruciaal zijn bij de ontwikkeling van B- en T-cellen.[26] Aanvankelijk werd aangenomen dat ID2 nodig was om CLP's te laten differentiëren tot alle ILC-subsets, maar onderzoek heeft aangetoond dat het uitschakelen van ID2 tijdens de ontwikkeling van CLP's de ontwikkeling van alle ILC-subsets verlamt, behalve NK-celvoorlopers, die niet afhankelijk zijn van de aanwezigheid van ID2.[27] Door dit inzicht werd een groep cellen met een negatieve afstammingslijn (een vereiste voor elke echte voorlopercel) geïdentificeerd, die volledig afhankelijk waren van de aanwezigheid van ID2 en andere belangrijke ILC-markers tot expressie brachten, met het fenotype: Lin-ID2+IL7Ra+CD25-α4β7+, die nu bekend staan als de gemeenschappelijke helperachtige aangeboren lymfoïde voorlopercellen CHILPs.[27] Ze worden 'gemeenschappelijke helperachtige' cellen genoemd vanwege hun gelijkenis met het lot van de T-helpercellen.
Afhankelijkheid van transcriptiefactoren
Elke fase van differentiatie is afhankelijk van de expressie van verschillende transcriptiefactoren, waaronder: NFIL3, TCF-1, ETS1, GATA3, PLZF, T-bet, eomesodermine, RUNX3, RORα, Bcl11b, Gfi1, RORγt en AhR.[6] De gecoördineerde expressie van deze specifieke transcriptiefactoren activeert of onderdrukt doelgenen die cruciaal zijn voor de differentiatie van de lymfocytensubgroepen.[26] Met name Nfil3, waarvan de expressie wordt gereguleerd door cytokinen, controleert de differentiatie van ILC's via de transcriptiefactoren ID2, RORγt, eomesodermine en Tox.[28] Dit levert bewijs dat de weefselsignalen een sleutelrol spelen bij beslissingen over het lot van ILC-lijnen.
Oorsprong en migratie
Studies suggereren dat de primaire locatie van ILC-ontwikkeling de lever is bij de foetus en het beenmerg bij volwassenen, aangezien hier CLP's, NKP's en CHILP's zijn aangetroffen. De cellen verlaten het bloed vervolgens en circuleren in het bloed totdat ze de aangewezen weefsels bereiken, gecodeerd door celadhesiemoleculen en chemokines.[26] Er is echter ook aangetoond dat de rijping van de ILC's buiten de primaire lymfoïde weefsels kan plaatsvinden, vergelijkbaar met de rijping van naïeve T-helpercellen. (Naïef: nog nooit in contact geweest met haar specifieke antigeen)
Voorlopers van NK-cellen en ILC3-voorlopers zijn aangetroffen in de menselijke amandelen, en foetale ILCP's zijn aanwezig in de darm van muizen en hopen zich op in de peyerse platen.[29][30] Retinezuur, geproduceerd door veel celtypen, zoals zenuwcellen, dendritische cellen en stromacellen, bevordert de differentiatie van ILC3's in plaats van ILC2's, en is vereist voor hun volledige rijping.[26] Bovendien is AhR, dat kan worden geactiveerd door liganden die worden geproduceerd na het katabolisme van voedsel, vereist voor het behoud van de functie en expressie van maag-darm ILC3's.[29]
Functie
ILC's nemen deel aan onze immuunrespons op pathogenen in alle organen, met name op slijmvliesoppervlakken.[13] Ze spelen een sleutelrol in de aangeboren immuunrespons vanwege hun vermogen om snel immuunregulerende cytokinen af te scheiden, maar ze spelen ook een rol bij het vormgeven van de verworven respons door interactie met andere immuuncellen. De micro-omgeving van het weefsel waarin ze zich bevinden, bepaalt en verfijnt de expressie van de diverse ILC-profielen, waardoor hun interactie in meerdere effectorfuncties wordt vergemakkelijkt. (Effectorcel: is een cel die een reactie uitvoert op een prikkel)
De strategische positionering en diepe verankering van ILC's in weefsels stellen hen in staat homeostase en daarmee een gezonde weefselfunctie te handhaven. De ILC's spelen echter ook een nadelige rol op verschillende slijmvlieslocaties.[31]
Aangezien de functie van ILC's gekoppeld is aan hun specifieke weefsellokalisatie, zal het bepalen van de signalen die betrokken zijn bij hun lokalisatie- en migratiepatronen belangrijk zijn bij het identificeren van nieuwe behandelmogelijkheden voor ziekten.[21]
Wormparasiet infectie en weefselherstel
Een fundamentele eigenschap van type 2-immuniteit, en dus van ILC2-cellen, is de bestrijding van te grote organismen die niet verteerd kunnen worden, zoals wormparasieten.[32] In de darm scheiden epitheelcellen, als reactie op een wormparasietinfectie, hoge concentraties IL-25 uit, waardoor ILC2-cellen worden geactiveerd. ILC2's produceren IL-13, dat de differentiatie van extra epitheelcellen aanstuurt via Notch-signaalroutes. Deze instructie maakt het mogelijk om het weefsel te hervormen om de wormparasiet en andere grote pathogenen te verdrijven.
IL-13 activeert ook T-cellen, wat verdere fysiologische reacties induceert om de parasiet te verdrijven. T-cellen stimuleren de secretie van slijmbekercellen, de samentrekking van glad spierweefsel, en scheiden signalen uit die mestcellen en eosinofiele granulocytlen naar de geïnfecteerde plaats lokken, waardoor de proliferatie van B-cellen wordt gestimuleerd.[33]
De infectie kan leiden tot weefselschade, als gevolg van migratie van de wormparasiet. ILC2's spelen een sleutelrol bij het herstellen van de weefselschade na infectie, door liganden zoals amfireguline te produceren voor receptoren voor epidermalegroeifactoren, wat de differentiatie van epitheelcellen voor weefselherstel vergemakkelijkt.[6] Dit kan de barrièrefunctie van het epitheel versterken en de toegang van pathogenen vertragen.[33]

In meerdere weefselniches hebben ILC's een relatie met niet-hematopoëtische cellen zoals stromacellen. In de longen hebben ILC2's een duidelijke lokalisatie naar stromacellen, die IL-33 en TSLP afgeven. Dit bevordert de homeostase van ILC2, zowel in rusttoestand als in reactie op een worminfectie, nadat de worm zich in de darm heeft ontwikkeld en via het bloed naar de longen is gemigreerd.[34]
Long-ILC2's bevinden zich dicht bij de bloedvaten, waardoor eosinofiele granulocyten uit het bloed kunnen worden gerekruteerd. Ze bevinden zich ook in de luchtwegen, waar potentiële pathogenen zich kunnen ophopen. Dit betekent dat ze in nauw contact staan met neuro-endocriene cellen, die ILC2's activeren via de afgifte van calcitonine-gen-gerelateerd peptide.[35] Andere studies bevestigen ook de regulatie van de ILC-functie via neuronale circuits.
Bovendien geven ILC1's en ILC3's zuurstofradicalen en dodelijke, schadelijke enzymen af als reactie op een pathogene infectie, waardoor het gastheerweefsel beschadigd raakt. De herstelreacties van het weefsel worden gecoördineerd door de immuunrespons type 2, nadat de ILC3's en ILC1's het weefsel hebben gereinigd van microben en afval.
Darmslijmvlies
ILC's in het maag-darmstelsel worden blootgesteld aan voedings-, microbiële en endogene metabolieten. De homing van ILC's naar de dunne darm wordt gemedieerd door α4β7-integrine en de receptor CCR9. ILC2's brengen CCR9 tot expressie in het beenmerg en kunnen zich dus direct naar de darm verplaatsen. Retinezuur is echter vereist om CCR9-expressie op ILC1's en ILC3's mogelijk te maken.
ILC's bevorderen het behoud van de barrière-integriteit in de darm en beschermen tegen diverse bacteriën en virale infecties. ILC3's vormen de meest voorkomende subgroep in zowel de volwassen als de foetale darm.[36] De distributie van ILC's in de darm verandert tijdens de ontwikkeling en ze zijn ongelijkmatig verdeeld over het maag-darmstelsel. Deze distributie naar verschillende niches in de darm wordt gemedieerd door verschillende signaalcascades.[37] Bij mensen is ongeveer 70% van het Maag-darmstelsel ILC's NCR+ en 15% NCR-.[38]

ILC3's interacteren rechtstreeks met de darmflora en creëren een netwerk tussen de microbiota en de gastheer, wat de homeostase bevordert. ILC3's beperken de kolonisatie van meerdere ongunstige bacteriën in de darm door secretie van IL-22, waardoor epitheelcellen worden gestimuleerd om antimicrobiële peptiden te produceren.[39] De IL-22-productie wordt geïnduceerd door de productie van IL-23 en IL-1β door macrofagen en dendritische cellen, en het bevordert de genezing van de slijmvlieslaag.[3] IL-22 kan bijvoorbeeld het herstel van darmschade na chemotherapie of radiotherapie bevorderen. ILC3's reguleren de insluiting van commensale bacteriën in het lumen, waardoor het kan worden blootgesteld aan lamina propria-fagocyten, wat leidt tot T-celpriming. Hoewel ze antigenen kunnen presenteren, via MHC-klasse II-receptoren, missen ILC's co-stimulerende moleculen en spelen ze daarom een rol bij T-celanergie (anergie: afwezigheid van reactie), waardoor de tolerantie voor gunstige commensalen wordt bevorderd.[38] De relatie tussen ILC3's en T-cellen in de darm is daarom cruciaal voor het handhaven van homeostase, aangezien er bij afwezigheid van ILC3's ongecontroleerde T-celactivering zou kunnen zijn. Bovendien spelen microbiota een rol bij het nauwkeurig regelen van de IL-22-productie door ILC3's; gesegmenteerde draadvormige bacteriën in de kronkeldarm reguleren bijvoorbeeld de IL-22-productie en maken de differentiatie van Th17-cellen mogelijk..[40][41]
ILC3's werken samen met het enterisch zenuwstelsel om de maag-darmhomeostase te handhaven, aangezien gliacellen in de lamina propria als reactie op bacteriën neurotrofe factoren afscheiden, die via de neuroregulerende receptor RET de productie van IL-22 door ILC3's induceren.[42] Dendritische cellen kunnen ook IL-23 produceren tijdens door pathogenen geïnduceerde stress, waardoor ILC3's ook worden geactiveerd en de productie van IL-22 mogelijk wordt. Een van de mechanismen waarmee IL-22 de microbiota in de darm reguleert, is via de glycosyleringspatronen van epitheelcellen. IL-22 en de expressie van lymfotoxinen door ILC3's controleren de expressie van fucosyltransferase 2, wat fucosylering van epitheelcellen mogelijk maakt en zo een voedingsbron biedt voor de darmbacteriën.[43]
AHR-liganden uit voeding of microbiota worden herkend door immuuncellen en reguleren de ontwikkeling van ILC's en de functies van NK-cellen in de darm. Als reactie op tryptofaanmetabolieten handhaaft AhR-signalering de expressie van IL-22 en de homeostase van de darmen. Retinezuur, geproduceerd door dendritische cellen, bevordert de expressie van darm-homing receptoren op ILC1's en ILC3's en verbetert de ILC3-functie door RORγt en IL-22 te verhogen.[6] Er is ook wederzijdse beïnvloeding tussen macrofagen en ILC3's, via RORγt-gedreven granulocyt-macrofaag koloniestimulerende factor-productie, die afhankelijk is van microbiële signalering, en de productie van IL-1β door macrofagen. Een tekort aan vitamine A in de voeding resulteert in abnormaal kleine aantallen ILC3's, en daarom een vermindering van de IL-22-productie, en een hogere vatbaarheid voor infectie. Omgekeerd onderdrukt retinezuur de proliferatie van ILC2 door IL-7Ra te onderdrukken, en is aangetoond dat een vitamine A tekort de door ILC2 veroorzaakte resistentie tegen wormparasietinfecties bij muizen versterkt.[38] ILC3's vormen daarom een netwerk van interacties om de maag-darmhomeostase te handhaven, tussen het microbioom, darmepitheel, gliacellen en andere immuuncellen.
LTi-cellen zijn aanwezig in de Peyerse platen en lymfoïde follikels en interageren met B-cellen, waardoor de productie van IgA wordt gefaciliteerd, wat de commensalisatie van de gastheer met de lokale microbiota bevordert.[44] ILC1's en NK-cellen produceren IFN-γ om intracellulaire pathogenen te bestrijden. Na infectie met Clostridioides difficile werken ILC1's en ILC3's samen om de infectie te bestrijden.[45] ILC2's induceren de differentiatie van slijmbekercellen en de productie van slijm in de darmen om weefselschade bij een parasitaire infectie te voorkomen.
Tumormicro-omgeving
Verschillende groepen aangeboren lymfoïde cellen kunnen tumorvorming op verschillende manieren beïnvloeden.[46][47]
Groep 1 ILC's vormen de populatie ILC's met het meest significante antitumorogene potentieel. NK-cellen bezitten het vermogen om ontbrekende MHC-klasse I-cellen op het oppervlak van tumorcellen te herkennen.[48] Op deze manier werken ze complementair met de cytotoxische T-cellen die tumorcellen herkennen en doden die een vreemd antigeen op MHC-klasse I presenteren.[49][50] NK-cellen brengen een aantal celoppervlakactiverende NK-celreceptoren tot expressie met specificiteit voor stressgeïnduceerde liganden met een verhoogde expressie op tumorcellen.
ILC1's beïnvloeden de tumormicro-omgeving door de productie van de cytokinen IFN-γ en TNF-α. Deze cytokinen polariseren aan het begin van de immuunrespons andere immuuncellen, zoals M1-macrofagen, dendritische cellen en cytotoxische T-cellen, naar de tumorlocatie, waardoor een ontstekingsomgeving ontstaat.[51] Indien succesvol, zal de rekrutering van deze cellen de tumorvormende cellen doden. In sommige gevallen kunnen IFN-γ en TNF-α echter een rol spelen bij de inductie van immunosuppressieve immuuncellen, zoals myeloïde suppressor cellen (MDSC's), en dus ontstekingsremmende cytokinen, waardoor de tumorcellen aan een immuunomgeving kunnen ontsnappen.[52][53][47]
De rol van ILC2's en ILC3's bij tumorbewaking is afhankelijk van de micro-omgeving in hun aanwezige weefsels.
ILC2's produceren cytokinen die een ontstekingsremmende immuunrespons bevorderen, bijvoorbeeld IL-13, IL-4 en amfireguline, wat tumorgroei bevordert.[54] In sommige situaties kunnen ILC2's echter IL-5 produceren, wat een cytotoxische reactie van eosinofiele granulocyten en daarmee een antitumorreactie bevordert.[55][56]
ILC3's kunnen ook betrokken zijn bij pro- of antitumorogene omgevingen. De productie van IL-17 kan de groei van tumoren en metastasering ondersteunen, omdat het de permeabiliteit van bloedvaten induceert. De upregulatie van MHC-klasse II op hun oppervlak kan echter T-helpercellen activeren, wat een antitumorogene werking heeft.[57] Daarnaast is gerapporteerd dat ILC3's de vorming van tertiaire lymfoïde structuren bij longkanker bevorderen en een beschermende rol spelen.[58]
Lever en metabolisme

Alle ILC-subgroepen zijn aanwezig in de lever en reguleren de immuunrespons om het weefsel te beschermen tegen virale en bacteriële infecties.[59] ILC1's zijn de dominante ILC-subgroep in de lever. Hun productie van IFN-γ bevordert de overleving van hepatocyten. De productie van IFN-γ door ILC1's is afhankelijk van de expressie van de NK-celreceptor CD226.[60] De door IL-12 aangestuurde IFN-γ-productie door ILC1's wordt versneld door extracellulaire ATP, en IFN-γ verhoogt de overlevingskans van de moleculen Bcl-2 en Bcl-xL in hepatocyten.[60]
NK-cellen spelen een rol in de immuunrespons tegen virale hepatitis B en hepatitis C en beperken leverfibrose en leverkanker. Ze elimineren levercellen in een fibrotische lever via TRAIL en/of NKG2D.
ILC's spelen een belangrijke rol bij het handhaven van voedingsstress en metabole homeostase. De productie van tryptofaanmetabolieten zorgt ervoor dat de AhR-transcriptiefactor de expressie van IL-22 induceert, waardoor het aantal aanwezige ILC3's en daarmee de maag-darmhomeostase behouden blijft.[6] De vitamine A-metaboliet, retinezuur, verhoogt ook de expressie van IL-22, en daarom resulteert de afwezigheid van de AhR-signaalroute en van retinezuur in een verminderde immuniteit tegen bacteriële infecties, zoals de gastro-intestinale Citrobacter rodentium-infectie.[6] Retinezuur verhoogt ook de expressie van maag-darm-homing markers op ILC1's en ILC3's. De beschikbaarheid van voedingsstoffen beïnvloedt daarom de immuunreactie van ILC op infecties en ontstekingen, wat het belang van een evenwichtig en gezond dieet benadrukt.
ILC2's ondersteunen een type-2 immuunomgeving in het vetweefsel, via de productie van IL-5, IL-4 en IL-13. Dit reguleert adipositas, insulineresistentie en calorieverbruik.[6] Ontregeling hiervan veroorzaakt aanhoudende type-1-ontsteking, wat leidt tot obesitas. ILC2's bevorderen de beigekleuring van adipocyten en daardoor een verhoogd energieverbruik. Daarom zijn verminderde reacties van ILC2's in het weefsel een kenmerk van obesitas, omdat dit hun cruciale rol in de energiehomeostase onderbreekt, wat resulteert in een verminderd energieverbruik en een verhoogde adipositas.[61] Naast ILC2's dragen ILC1's bij aan de homeostase van macrofagen in vetweefsel, zowel in magere als obese omstandigheden, en vormen 5-10% van de residentiële lymfocytenpopulatie in menselijke magere vetdepots.[10] Een vetrijk dieet verhoogt het aantal ILC1's en de activering van vetweefsel, waardoor de niveaus van IFN-γ en TNF-α toenemen. ILC1's produceren de macrofaag-chemo-attractant CCL2, en daarom is ILC1-macrofaagsignalering een belangrijke regulator van vetweefsel.[62] Deze stofwisselingsroute zou een potentieel doelwit kunnen zijn voor de behandeling van patiënten met een leverziekte.
Luchtweginfectie
ILC2's bevorderen de proliferatie van epitheelcellen en slijmbekercellen, en daarmee de slijmproductie in de luchtwegen. Deze functies dragen bij aan het herstel en behoud van de integriteit van het epitheel. ILC2's bieden een verdediging tegen wormparasiet-infecties in de longen, via de productie van AhR, IL-9 en IL-13.[63] Aangenomen wordt dat deze ILC2's in de darm ontstaan en naar de longen migreren om de wormparasiet-infectie te bestrijden.[64]
ILC1's en NK-cellen scheiden IFN-γ af als reactie op virale infecties in de longen, waaronder het rinovirus en respiratoir syncytieel virus (RSV).[3]
ILC3's spelen ook een rol bij longinfecties, via de secretie van IL-17 en IL-22, bijvoorbeeld bij een infectie met pneumokokken.[65]
Huidherstel

Er zijn aanwijzingen dat ILC3's en ILC2's bij zowel muizen als mensen naar de gewonde dermis worden gestuurd via epidermale Notch1-signalering. De ILC3's scheiden IL-17F uit, dat een rol speelt in de immuun- en epitheliale cellulaire reacties tijdens wondgenezing, door macrofagen naar de wondplek te lokken. De expressie van TNF speelt ook een rol bij wondgenezing, omdat het de lokalisatie van ILC3's naar de beschadigde opperhuid stuurt. Als reactie op de afgifte van IL-33 door de opperhuid scheiden ILC2's hoge niveaus amfireguline af, een cruciale epidermalegroeifactor, die daardoor bijdraagt aan de genezing van huidwonden.[38]
Mondslijmvlies
Het mondslijmvlies is gekoloniseerd met commensalen en wordt blootgesteld aan voedingsantigenen en pathogenen. De ILC's in het mondslijmvlies helpen de barrière te behouden en beschermen tegen infecties. ILC3's en intra-epitheliale ILC1's werden aanvankelijk geïdentificeerd in amandelen en aangetroffen in menselijk tandvlees. Ongeveer 10-15% van de lymfocyten werd geïdentificeerd als ILC's, waarvan de meeste IFN-γ ILC1's produceren. ILC3's in de orofaryngeale zone beschermen tegen infecties met Candida albicans, die IL-17A en IL-17F produceren, geïnduceerd door IL-23. Muizen zonder ILC3's als gevolg van deletie van RORγt liepen ernstige infecties op met Candida albicans.[66]
Luchtwegen
Het is aangetoond dat ILC's neurotransmitters en neuropeptiden in de longen kunnen afscheiden. ILC2's interageren met zenuwcellen in de luchtwegen door de nabijheid van axonen, en in de longen aanwezige IL-5-producerende ILC2's worden aangetroffen in collageenrijke gebieden dicht bij de samenvloeiing van middelgrote bloedvaten en luchtwegen. Daarnaast worden IL-5-producerende ILC2's aangetroffen in neuro-endocriene cellen van de longen in de verbindingspunten van de luchtwegen, waar deeltjes die de luchtwegen binnendringen zich concentreren. De lokalisatie van ILC2 in de luchtwegen suggereert dat de aanwezigheid van ILC2 wordt bepaald door micro-omgevingen in verschillende zones van het weefsel.[67]
Circadiaan ritme
De interacties tussen de circadiaan klok en ILC zijn aangetoond door de regulatie van het hoofdgen (Arntl) te bestuderen. De deletie ervan resulteerde in de ontreguling van ILC3, veroorzaakt door epigenetische veranderingen, wat de expressie van IL-22 aanstuurde en bijdroeg aan de verandering van het microbioom, epitheelcellen en een verstoorde opname van lipiden in de darm. Aan de andere kant resulteerde de deletie van Nr1d1, een eiwit dat betrokken is bij de regulatie van circadiane metabole reacties, in een afname van NCR+ (NK-celreceptoren) ILC3 en een toename van de IL-17-productie, terwijl het LTi-achtige ILC3 niet werd beïnvloed.[68]
Plasticiteit

De classificatie van ILC's in subsets biedt een vereenvoudigd raamwerk. Verschillende studies suggereren dat hun ontwikkeling en fenotypisch behoud veel complexer is, met een hoge mate van plasticiteit tussen de subsets. Studies hebben bevestigd dat sommige ILC-subsets in staat zijn om in aanwezigheid van specifieke cytokinen te transformeren in een andere subset.[13][46] Dit is ook een veelvoorkomend kenmerk in T-cellen, en men gelooft dat deze plasticiteit cruciaal is om ons immuunsysteem in staat te stellen de reacties op zoveel verschillende pathogenen nauwkeurig af te stemmen.[13] ILC-plasticiteit vereist cytokinereceptoren, hun transcriptiefactoren en toegang van gedefinieerde chromatineregio's tot de transcriptiefactoren. Het blijft echter onduidelijk waar deze cytokinen worden geproduceerd en waar de differentiatie in vivo plaatsvindt.[6]
De ILC's bij patiënten met COPD zijn een prototypisch voorbeeld van ILC-plasticiteit. Studies bij zowel mensen als muizen hebben aangetoond dat in de longen aanwezige ILC2's een ILC1-fenotype verkrijgen tijdens COPD, waardoor de IFN-γ-secretie en daarmee de ontsteking toenemen.[69] Verschillende triggers, waaronder sigarettenrook, veroorzaken de secretie van IL-12 en IL-18, wat leidt tot de differentiatie van ILC2's naar ILC1's. GATA3 is downgereguleerd en de T-bet-expressie (T-box-expressie in T-cellen) is upgereguleerd. Patiënten hebben daarom een hogere ILC1:ILC2-ratio in het bloed, waarbij de hoeveelheid aanwezige ILC1's correleert met de ernst van de ziekte.[69]
Het vermogen van ILC3's om te transformeren in ILC1-achtige cellen is in vitro en in vivo aangetoond.[70][71][46] Wanneer ILC3's worden gekweekt met IL-2 en IL-15, veroorzaakt dit de upregulering van T-bet en de IL-12-receptor (IL-12R) β2, waardoor de conversie van ILC3's naar ILC1's mogelijk wordt. Bovendien suggereren studies dat IL-23 de conversie van ILC1's naar ILC3's kan bevorderen.[71]
Er is steeds meer bewijs dat ILC2's ook een zekere mate van plasticiteit hebben. Studies bevestigen hun vermogen om te transformeren in ILC1's en ILC3's na blootstelling aan specifieke omgevingsstimuli zoals cytokinen of Notch-liganden.[72][46]
De signalering die door de cytokinen wordt geïnduceerd, reguleert de plasticiteit tussen ILC3 en ILC1 en induceert de expressie van T-bet. Bij patiënten met de ziekte van Crohn kan de toename van ILC1 ten koste gaan van ILC3, mogelijk door de productie van IL-2 door regulerende T-cellen, leiden tot een pathogene toestand en ontstekingsreacties. Hoewel de plasticiteit omkeerbaar is, is de modulatie van de T-bet-expressie tijdens de differentiatie van NKp46+ ILC3's naar ILC1 afhankelijk van IL-23, IL-2 en IL-1b en wordt deze verbeterd door retinezuur. De plasticiteit van ILC3 naar ILC1 is daarom afhankelijk van dendritische cellen die deze cytokinen produceren. Hoewel de onderlinge verwisselbaarheid van ILC1 en ILC3 wordt gemoduleerd door de differentiële expressie van RORγt en T-bet, blijven er verschillende vragen openstaan om de door deze cellen veroorzaakte ontsteking te begrijpen.[73]
In het geval van ILC2 kan Gata3 worden onderdrukt door blootstelling aan infectieuze agentia zoals het influenzavirus, respiratoir syncytieel virus en Staphylococcus aureus, waardoor de expressie van IL-12Rb2, IL-18Ra en T-bet toeneemt. De differentiatie van ILC2 naar ILC1 kan ook omkeerbaar zijn, hoewel het mechanisme nog niet bekend is.[73]
In bepaalde omgevingen, zoals ontstekingen, chronische ziekten of tumormicro-omgevingen, kunnen geactiveerde NK-cellen CD49a en CXCR6, veelvoorkomende ILC1-markers, gaan vormen, waardoor hun plastische eigenschappen worden versterkt.[74][75]
Het bepalen van de mate van ILC-plasticiteit tijdens ziekte kan nuttig zijn om de omzetting ervan in andere subgroepen die mogelijk bijdragen aan de pathogeniteit te voorkomen of te versterken.[46][76]
Pathologie
Astma



ILC2's spelen een pathogene rol tijdens een longontsteking. Epitheelcellen in de longen produceren de cytokinen IL-33 en IL-25, oftewel TSLP, als reactie op verschillende allergenen, schimmels en virussen. Deze cytokinen activeren ILC2's, waardoor er een verhoogd aantal ILC2's en type 2 cytokinen (IL-4/5/13) aanwezig is bij patiënten met allergisch astma.[3] Ze scheiden IL-13 af, wat allergische longontsteking initieert, en bevorderen bovendien de Th2-differentiatie, waardoor de productie van IL-13 toeneemt en de allergische reactie wordt versterkt.[77]
De productie van IL-5 door ILC2's in de longen leidt tot de rekrutering van eosinofiele granulocyten, en het is bekend dat andere celpopulaties interacteren en de aanwezigheid van long-ILC2's beïnvloeden bij luchtwegontsteking bij astmapatiënten. Daarnaast bevorderen ze ook de proliferatie van B-cellen. Aangenomen wordt dat de toename van het aantal aanwezige ILC2's correleert met de ernst van de ziekte, en er zijn aanwijzingen dat sommige allergeen-meegemaakte ILC2's blijven bestaan na het verdwijnen van de initiële ontsteking, wat overeenkomsten vertoont met T-geheugencellen. De aanwezigheid van de allergeen meegemaakte ILC2's kan de reden zijn dat astmapatiënten vaak gevoelig zijn voor verschillende allergenen.[38]
Deze allergische immuunreactie lijkt onafhankelijk te zijn van T- en B-cellen. Er zijn aanwijzingen dat allergische reacties die lijken op astma-achtige symptomen kunnen worden geïnduceerd bij muizen zonder T- en B-cellen, met behulp van IL-33.[78][79]
Hoe andere ILC's astma beïnvloeden, is minder duidelijk. Studies tonen echter een correlatie aan tussen het aantal IL-17-producerende ILC3's en de ernst van de ziekte. Bij muizen is aangetoond dat NK-cellen en ILC1's de ILC2-expansie remmen door de productie van IFN-γ, en daarom mogelijk kunnen helpen de ziekte onder controle te houden.[80]
Auto-immuunziekte
NK-cellen brengen veel celoppervlakreceptoren tot expressie die activerend, remmend, adhesief, cytokine- of chemotactisch kunnen zijn. De integratie van informatie die via deze talrijke inputs wordt verzameld, stelt NK-cellen in staat om zelftolerant te blijven en stresssignalen van eigen cellen te herkennen..[81] Als de genuanceerde, dynamische regulatie van NK-celactivering uit balans raakt ten gunste van aanvallen op eigen cellen, kan dit leiden tot een auto-immuunziekte. Ontregeling van NK-cellen is in verband gebracht met een aantal auto-immuunziekten, waaronder multiple sclerose, systemische lupus erythematodes en diabetes type 1.[82]
Er zijn aanwijzingen dat het richten op ILC's nuttig kan zijn bij het ontwerpen van therapieën voor auto-immuunziekten. Omdat ILC's en T-cellen veel redundante functies hebben, is het richten op en neutraliseren van hun effectorcytokinen mogelijk een betere optie. Als alternatief zou het richten op hun activerende upregulatie mediatoren (IL-23, IL-1B of IL-6) of hun overlevingsfactoren (IL-7) gebruikt kunnen worden als een aanpak om ontstekingsziekten te behandelen.[21]
Allergische rinitis
De frequentie van ILC2's is ook verhoogd gebleken in andere weefsels met allergische symptomen, zoals de neuspoliepen van patiënten met chronische bijholteontsteking en bij patiënten met een door aspirine verergerde luchtwegaandoening.[3] De concentratie van ILC2's correleert positief met de ernst van de ziekte.
ILC2's worden geactiveerd door de aanwezigheid van TSLP en IL-4, respectievelijk geproduceerd door epitheelcellen en eosinofiele granulocyten. Vervolgens produceren ze IL-4, IL-5 en IL-13, wat eosinofiele granulocyten verder activeert in een positieve terugkoppelingslus, waardoor ontstekingen worden bevorderd. Het verstoren van deze lus zou een potentiële therapie voor rinitis kunnen zijn. NK-cellen lijken een gunstige rol te spelen; bij mensen met allergische rinitis zijn er minder aanwezig.[83]
Inflammatory bowel disease (IBD) en darmkanker
Onderzoek suggereert dat IL-17-producerende NCR-ILC3's (NCR: NK-celreceptoren) bijdragen aan de pathofysiologie van IBD vanwege hun verhoogde aanwezigheid in de darm van patiënten met de ziekte van Crohn. Bovendien neemt het aantal ILC1's in het darmslijmvlies van patiënten met de ziekte van Crohn toe van ongeveer 10% tot 40% van het totale aantal aanwezige ILC's. De toename van het aantal aanwezige ILC's correleert met de ernst van de ziekte. Er zijn aanwijzingen dat de plasticiteit tussen ILC3's en ILC1's in de darm een belangrijke factor is bij de ziekte van Crohn, waarbij ILC3's differentiëren tot ILC1's bij blootstelling aan IL-12, geproduceerd door dendritische cellen.[39] IL-23, IL-1B en retinezuur in de darm kunnen echter de differentiatie van ILC1's terug naar ILC3's aanjagen. Er zijn ook aanwijzingen dat ILC2's het pro-inflammatoire fenotype kunnen verkrijgen, waarbij ILC2's IFN-γ produceren, aanwezig in de darm van patiënten met de ziekte van Crohn, als reactie op bepaalde omgevingsfactoren zoals cytokines.[38]
Patiënten met inflammatoire darmziekten (IBD) hebben een verhoogd risico op darmkanker als gevolg van chronische ontsteking, wanneer de ILC3's het pro-inflammatoire ILC1-fenotype verkrijgen tijdens chronische ontsteking. Omdat ILC's zich ophopen in de darm van IBD-patiënten, wordt aangenomen dat ze een pro-tumorogene rol spelen. Studies tonen een toename aan van de hoeveelheid effectorcytokinen IL-23, IL-17 en IL-22 in de tumormicro-omgeving van darmkanker, wat dit ondersteunt.[84][85][86]
NK-cellen scheiden IFN-γ af, wat anti-tumorogene effecten heeft. Meerdere studies tonen een verminderde frequentie aan van NK-cellen en IFN-γ in de darm of het perifere bloed van patiënten met darmkanker.[87][88] Verder onderzoek is nodig om hun exacte rol in de darmkankeromgeving te achterhalen.
Leverkanker en obesitas
Lever ILC1's dragen bij aan de pathogenese van chronische hepatitis B door de productie van IFN-γ en TNF-α. Verstoring van het epitheel van het galkanaal wordt vaak waargenomen als reactie op chronische leverontsteking, en een verhoogde proliferatie van deze galwegen wordt geassocieerd met leverkanker.[60] Er zijn aanwijzingen dat de verhoogde proliferatie wordt veroorzaakt door IL-13, dat wordt geproduceerd door de door IL-33 geïnduceerde productie van ILC2-cellen. Van ILC2's is ook aangetoond dat ze de progressie van leverfibrose bevorderen, wat op zijn beurt de ontwikkeling van leverkanker bevordert.[59]
De beschikbaarheid van specifieke voedingsstoffen kan de immuunhomeostase van ILC beïnvloeden door de energie die in het vetweefsel is opgeslagen te veranderen. Vetweefsel handhaaft de metabole homeostase en wordt nu beschouwd als een volledig immuuncompetent orgaan. Ondervoeding en vraatzucht kunnen de ILC-reacties ontregelen via veranderingen in voedingsstoffen, met directe effecten op de energie die in het vetweefsel is opgeslagen.[10] Obesitas wordt geassocieerd met veranderingen in de maag-darmflora, verhoogde toestroom van vrije vetzuren uit vetweefsel naar de lever en verhoogde darmpermeabiliteit.[10] Wanneer vetzuren circuleren in het plasma (plasmavetzuren), en niet in hun ester, staan ze bekend als vrije vetzuren. Vrije vetzuren zijn altijd gebonden aan een transporteiwit, zoals albumine. De nauwe anatomische nabijheid van het maag-darmkanaal en de lever betekent dat transport van bacteriële metabolieten door de poortader ontsteking veroorzaakt, die inwerkt op aangeboren immuuncellen, waaronder ILC1's, en daarom een belangrijke rol speelt bij de activering van een ontstekingstoestand in de lever. Daarom kan ontsteking geassocieerd met obesitas de progressie van leverziekte beïnvloeden, vanwege de ontwikkeling van insulineresistentie en metabole ontregeling.[10] ILC1's zijn een belangrijke regulator van ontstekingen in vetweefsel en vormen daarom een potentieel therapeutisch doelwit voor de behandeling van mensen met leveraandoeningen of het metabool syndroom.
ILC2's zijn ook geïdentificeerd in wit vetweefsel van mensen en muizen en dragen bij aan de ontwikkeling van obesitas. Bij ontregeling van de homeostase in het vetweefsel zijn de verminderde reacties van ILC2's kenmerkend voor obesitas, omdat dit hun cruciale rol in de energiehomeostase verstoort, wat resulteert in een lager energieverbruik en een toename van de vetopslag.[61]
Huidontsteking
De frequentie van ILC2's is hoger in de ontstoken huid van patiënten met constitutioneel eczeem dan bij gezonde patiënten.[38] De ILC2's in de huid van de patiënten vertoonden een upregulatie van de IL-25-, IL-33-, TSLP- en PGD2-receptoren, wat suggereert dat ze een rol spelen bij de activering van ILC2's. Basofiele granulocyten en mestcellen zijn ook aanwezig in deze huidlaesies en produceren IL-4 en PGD2, wat de ILC2's verder activeert.
 |
 |
Psoriasis, een andere huidziekte, veroorzaakt verdikking van de opperhuid en de vorming van plaques die voornamelijk bestaan uit T-cellen en dendritische cellen. De T-cellen vertonen een type 1 immuunrespons; de verdikking en ontsteking van de opperhuid worden echter vermoedelijk veroorzaakt door de productie van IL-22, IL-17A en IL-17F door andere T-cellen, zoals Th17 of gamma delta T-cellen.[39] Recentere gegevens suggereren echter dat ILC3's in feite een groot aantal van deze cytokinen produceren, met een toename van het aantal ILC3's in het perifere bloed van patiënten met psoriasis.[38]
Artritis
De ILC's zijn bestudeerd in mucosale barrières en hun interactie met verworven immuniteit, wat ze impliceert bij auto-immuunziekten. Bij artritis die gekenmerkt wordt door de aanwezigheid van auto-antilichamen, is de ontregelde interactie tussen Tfh- en B-cellen betrokken bij de aanmaak van die antilichamen. Interessant is dat er gesuggereerd is dat Th17- en Tfh-ontstekingsreacties worden gegenereerd in het maag-darmkanaal en dat microbiota deze reactie kunnen versterken. De ontwikkeling van ILC's die betrokken zijn bij de regulering van de immuunrespons tegen de microbiota in de darm, is dus in verband gebracht met artritis. In het geval van ILC2 speelt ILC2 een belangrijke rol bij de regulering van ontstekingsreacties door de productie van IL-4, IL-9 en IL-13.[89]
Multiple sclerose
In het geval van ILC3 bij multiple sclerose zijn deze cellen betrokken bij tertiaire lymfoïde aggregaten in de hersenen van patiënten met de progressieve ziekte. Bovendien correleerde de toename van LTi-achtige ILC3 met de auto-antilichamen in de hersenvloeistof.[89]
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Innate lymphoid cell op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- ↑ Spits H, Cupedo T (2012). Innate lymphoid cells: emerging insights in development, lineage relationships, and function. Annual Review of Immunology 30: 647–75. PMID 22224763. DOI: 10.1146/annurev-immunol-020711-075053.
- ↑ Spits H, Artis D, Colonna M, Diefenbach A, Di Santo JP, Eberl G, Koyasu S, Locksley RM, McKenzie AN, Mebius RE, Powrie F, Vivier E (February 2013). Innate lymphoid cells--a proposal for uniform nomenclature. Nature Reviews. Immunology 13 (2): 145–9. PMID 23348417. DOI: 10.1038/nri3365.
- 1 2 3 4 5 6 7 Panda SK, Colonna M (2019). Innate Lymphoid Cells in Mucosal Immunity. Frontiers in Immunology 10. PMID 31134050. PMC 6515929. DOI: 10.3389/fimmu.2019.00861.
- 1 2 Walker JA, Barlow JL, McKenzie AN (February 2013). Innate lymphoid cells--how did we miss them?. Nature Reviews. Immunology 13 (2): 75–87. PMID 23292121. DOI: 10.1038/nri3349.
- 1 2 (February 2013). A T-bet gradient controls the fate and function of CCR6-RORγt+ innate lymphoid cells. Nature 494 (7436): 261–5. PMID 23334414. DOI: 10.1038/nature11813.
- 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 Vivier E, Artis D, Colonna M, Diefenbach A, Di Santo JP, Eberl G, Koyasu S, Locksley RM, McKenzie AN, Mebius RE, Powrie F, Spits H (August 2018). Innate Lymphoid Cells: 10 Years On. Cell 174 (5): 1054–1066. PMID 30142344. DOI: 10.1016/j.cell.2018.07.017.
- ↑ Jowett GM, Norman MD, Yu TT, Rosell Arévalo P, Hoogland D, Lust ST, Read E, Hamrud E, Walters NJ, Niazi U, Chung MW, Marciano D, Omer OS, Zabinski T, Danovi D, Lord GM, Hilborn J, Evans ND, Dreiss CA, Bozec L, Oommen OP, Lorenz CD, da Silva RM, Neves JF, Gentleman E (February 2021). ILC1 drive intestinal epithelial and matrix remodelling. Nature Materials 20 (2): 250–259. PMID 32895507. PMC 7611574. DOI: 10.1038/s41563-020-0783-8.
- ↑ Daussy C, Faure F, Mayol K, Viel S, Gasteiger G, Charrier E, Bienvenu J, Henry T, Debien E, Hasan UA, Marvel J, Yoh K, Takahashi S, Prinz I, de Bernard S, Buffat L, Walzer T (March 2014). T-bet and Eomes instruct the development of two distinct natural killer cell lineages in the liver and in the bone marrow. The Journal of Experimental Medicine 211 (3): 563–77. PMID 24516120. PMC 3949572. DOI: 10.1084/jem.20131560.
- ↑ Simonetta F, Pradier A, Roosnek E (2016). T-bet and Eomesodermin in NK Cell Development, Maturation, and Function. Frontiers in Immunology 7. PMID 27379101. PMC 4913100. DOI: 10.3389/fimmu.2016.00241.
- 1 2 3 4 Luci C, Vieira E, Perchet T, Gual P, Golub R (2019). Natural Killer Cells and Type 1 Innate Lymphoid Cells Are New Actors in Non-alcoholic Fatty Liver Disease. Frontiers in Immunology 10. PMID 31191550. PMC 6546848. DOI: 10.3389/fimmu.2019.01192.
- ↑ Weizman OE, Adams NM, Schuster IS, Krishna C, Pritykin Y, Lau C, Degli-Esposti MA, Leslie CS, Sun JC, O'Sullivan TE (November 2017). ILC1 Confer Early Host Protection at Initial Sites of Viral Infection. Cell 171 (4): 795–808.e12. PMID 29056343. PMC 5687850. DOI: 10.1016/j.cell.2017.09.052.
- ↑ Cortez VS, Fuchs A, Cella M, Gilfillan S, Colonna M (May 2014). Cutting edge: Salivary gland NK cells develop independently of Nfil3 in steady-state. Journal of Immunology 192 (10): 4487–91. PMID 24740507. DOI: 10.4049/jimmunol.1303469.
- 1 2 3 4 Colonna M (June 2018). Innate Lymphoid Cells: Diversity, Plasticity, and Unique Functions in Immunity. Immunity 48 (6): 1104–1117. PMID 29924976. PMC 6344351. DOI: 10.1016/j.immuni.2018.05.013.
- ↑ Kim BS, Siracusa MC, Saenz SA, Noti M, Monticelli LA, Sonnenberg GF, Hepworth MR, Van Voorhees AS, Comeau MR, Artis D (January 2013). TSLP elicits IL-33-independent innate lymphoid cell responses to promote skin inflammation. Science Translational Medicine 5 (170): 170ra16. PMID 23363980. PMC 3637661. DOI: 10.1126/scitranslmed.3005374.
- ↑ Roediger B, Kyle R, Yip KH, Sumaria N, Guy TV, Kim BS, Mitchell AJ, Tay SS, Jain R, Forbes-Blom E, Chen X, Tong PL, Bolton HA, Artis D, Paul WE, Fazekas de St Groth B, Grimbaldeston MA, Le Gros G, Weninger W (June 2013). Cutaneous immunosurveillance and regulation of inflammation by group 2 innate lymphoid cells. Nature Immunology 14 (6): 564–73. PMID 23603794. PMC 4282745. DOI: 10.1038/ni.2584.
- ↑ Neill DR, Wong SH, Bellosi A, Flynn RJ, Daly M, Langford TK, Bucks C, Kane CM, Fallon PG, Pannell R, Jolin HE, McKenzie AN (April 2010). Nuocytes represent a new innate effector leukocyte that mediates type-2 immunity. Nature 464 (7293): 1367–70. PMID 20200518. PMC 2862165. DOI: 10.1038/nature08900.
- ↑ Mjösberg J, Bernink J, Golebski K, Karrich JJ, Peters CP, Blom B, te Velde AA, Fokkens WJ, van Drunen CM, Spits H (October 2012). The transcription factor GATA3 is essential for the function of human type 2 innate lymphoid cells. Immunity 37 (4): 649–59. PMID 23063330. DOI: 10.1016/j.immuni.2012.08.015.
- ↑ Juelke K, Romagnani C (February 2016). Differentiation of human innate lymphoid cells (ILCs). Current Opinion in Immunology 38: 75–85. PMID 26707651. DOI: 10.1016/j.coi.2015.11.005.
- ↑ Buonocore S, Ahern PP, Uhlig HH, Ivanov II, Littman DR, Maloy KJ, Powrie F (April 2010). Innate lymphoid cells drive interleukin-23-dependent innate intestinal pathology. Nature 464 (7293): 1371–5. PMID 20393462. PMC 3796764. DOI: 10.1038/nature08949.
- ↑ Gaffen SL, Jain R, Garg AV, Cua DJ (September 2014). The IL-23-IL-17 immune axis: from mechanisms to therapeutic testing. Nature Reviews. Immunology 14 (9): 585–600. PMID 25145755. PMC 4281037. DOI: 10.1038/nri3707.
- 1 2 3 4 Pantazi E, Powell N (2019). Group 3 ILCs: Peacekeepers or Troublemakers? What's Your Gut Telling You?!. Frontiers in Immunology 10. PMID 31024537. PMC 6460375. DOI: 10.3389/fimmu.2019.00676.
- ↑ Cupedo T, Crellin NK, Papazian N, Rombouts EJ, Weijer K, Grogan JL, Fibbe WE, Cornelissen JJ, Spits H (January 2009). Human fetal lymphoid tissue-inducer cells are interleukin 17-producing precursors to RORC+ CD127+ natural killer-like cells. Nature Immunology 10 (1): 66–74. PMID 19029905. DOI: 10.1038/ni.1668.
- 1 2 3 Withers DR (May 2011). Lymphoid tissue inducer cells. Current Biology 21 (10): R381-2. PMID 21601793. DOI: 10.1016/j.cub.2011.03.022.
- ↑ Mebius RE, Rennert P, Weissman IL (October 1997). Developing lymph nodes collect CD4+CD3- LTbeta+ cells that can differentiate to APC, NK cells, and follicular cells but not T or B cells. Immunity 7 (4): 493–504. PMID 9354470. DOI: 10.1016/S1074-7613(00)80371-4.
- ↑ Strober W (November 2010). The LTi cell, an immunologic chameleon. Immunity 33 (5): 650–2. PMID 21094460. PMC 3426921. DOI: 10.1016/j.immuni.2010.11.016.
- 1 2 3 4 5 Eberl G, Colonna M, Di Santo JP, McKenzie AN (May 2015). Innate lymphoid cells. Innate lymphoid cells: a new paradigm in immunology. Science 348 (6237). PMID 25999512. PMC 5658207. DOI: 10.1126/science.aaa6566.
- 1 2 Klose CS, Flach M, Möhle L, Rogell L, Hoyler T, Ebert K, Fabiunke C, Pfeifer D, Sexl V, Fonseca-Pereira D, Domingues RG, Veiga-Fernandes H, Arnold SJ, Busslinger M, Dunay IR, Tanriver Y, Diefenbach A (April 2014). Differentiation of type 1 ILCs from a common progenitor to all helper-like innate lymphoid cell lineages. Cell 157 (2): 340–356. PMID 24725403. DOI: 10.1016/j.cell.2014.03.030.
- ↑ Xu W, Domingues RG, Fonseca-Pereira D, Ferreira M, Ribeiro H, Lopez-Lastra S, Motomura Y, Moreira-Santos L, Bihl F, Braud V, Kee B, Brady H, Coles MC, Vosshenrich C, Kubo M, Di Santo JP, Veiga-Fernandes H (March 2015). NFIL3 orchestrates the emergence of common helper innate lymphoid cell precursors. Cell Reports 10 (12): 2043–54. PMID 25801035. DOI: 10.1016/j.celrep.2015.02.057.
- 1 2 Bando JK, Liang HE, Locksley RM (February 2015). Identification and distribution of developing innate lymphoid cells in the fetal mouse intestine. Nature Immunology 16 (2): 153–60. PMID 25501629. PMC 4297560. DOI: 10.1038/ni.3057.
- ↑ Lee JS, Cella M, McDonald KG, Garlanda C, Kennedy GD, Nukaya M, Mantovani A, Kopan R, Bradfield CA, Newberry RD, Colonna M (November 2011). AHR drives the development of gut ILC22 cells and postnatal lymphoid tissues via pathways dependent on and independent of Notch. Nature Immunology 13 (2): 144–51. PMID 22101730. PMC 3468413. DOI: 10.1038/ni.2187.
- ↑ Kotas ME, Locksley RM (June 2018). Why Innate Lymphoid Cells?. Immunity 48 (6): 1081–1090. PMID 29924974. PMC 6145487. DOI: 10.1016/j.immuni.2018.06.002.
- ↑ Löser S, Smith KA, Maizels RM (2019). Innate Lymphoid Cells in Helminth Infections-Obligatory or Accessory?. Frontiers in Immunology 10. PMID 31024526. PMC 6467944. DOI: 10.3389/fimmu.2019.00620.
- 1 2 Palm NW, Rosenstein RK, Medzhitov R (April 2012). Allergic host defences. Nature 484 (7395): 465–72. PMID 22538607. PMC 3596087. DOI: 10.1038/nature11047.
- ↑ Dahlgren MW, Jones SW, Cautivo KM, Dubinin A, Ortiz-Carpena JF, Farhat S, Yu KS, Lee K, Wang C, Molofsky AV, Tward AD, Krummel MF, Peng T, Molofsky AB (March 2019). Adventitial Stromal Cells Define Group 2 Innate Lymphoid Cell Tissue Niches. Immunity 50 (3): 707–722.e6. PMID 30824323. PMC 6553479. DOI: 10.1016/j.immuni.2019.02.002.
- ↑ Sui P, Wiesner DL, Xu J, Zhang Y, Lee J, Van Dyken S, Lashua A, Yu C, Klein BS, Locksley RM, Deutsch G, Sun X (June 2018). Pulmonary neuroendocrine cells amplify allergic asthma responses. Science 360 (6393). PMID 29599193. PMC 6387886. DOI: 10.1126/science.aan8546.
- ↑ Bernink JH, Peters CP, Munneke M, te Velde AA, Meijer SL, Weijer K, Hreggvidsdottir HS, Heinsbroek SE, Legrand N, Buskens CJ, Bemelman WA, Mjösberg JM, Spits H (March 2013). Human type 1 innate lymphoid cells accumulate in inflamed mucosal tissues. Nature Immunology 14 (3): 221–9. PMID 23334791. DOI: 10.1038/ni.2534.
- ↑ Willinger T (2019). Metabolic Control of Innate Lymphoid Cell Migration. Frontiers in Immunology 10. PMID 31507605. PMC 6713999. DOI: 10.3389/fimmu.2019.02010.
- 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Ebbo M, Crinier A, Vély F, Vivier E (November 2017). Innate lymphoid cells: major players in inflammatory diseases. Nature Reviews. Immunology 17 (11): 665–678. PMID 28804130. DOI: 10.1038/nri.2017.86.
- ↑ Zheng Y, Valdez PA, Danilenko DM, Hu Y, Sa SM, Gong Q, Abbas AR, Modrusan Z, Ghilardi N, de Sauvage FJ, Ouyang W (March 2008). Interleukin-22 mediates early host defense against attaching and effacing bacterial pathogens. Nature Medicine 14 (3): 282–9. PMID 18264109. DOI: 10.1038/nm1720.
- ↑ Ivanov II, McKenzie BS, Zhou L, Tadokoro CE, Lepelley A, Lafaille JJ, Cua DJ, Littman DR (September 2006). The orphan nuclear receptor RORgammat directs the differentiation program of proinflammatory IL-17+ T helper cells. Cell 126 (6): 1121–33. PMID 16990136. DOI: 10.1016/j.cell.2006.07.035.
- ↑ Zhou L, Ivanov II, Spolski R, Min R, Shenderov K, Egawa T, Levy DE, Leonard WJ, Littman DR (September 2007). IL-6 programs T(H)-17 cell differentiation by promoting sequential engagement of the IL-21 and IL-23 pathways. Nature Immunology 8 (9): 967–74. PMID 17581537. DOI: 10.1038/ni1488.
- ↑ Ibiza S, García-Cassani B, Ribeiro H, Carvalho T, Almeida L, Marques R, Misic AM, Bartow-McKenney C, Larson DM, Pavan WJ, Eberl G, Grice EA, Veiga-Fernandes H (July 2016). Glial-cell-derived neuroregulators control type 3 innate lymphoid cells and gut defence. Nature 535 (7612): 440–443. PMID 27409807. PMC 4962913. DOI: 10.1038/nature18644.
- ↑ Goto Y, Obata T, Kunisawa J, Sato S, Ivanov II, Lamichhane A, Takeyama N, Kamioka M, Sakamoto M, Matsuki T, Setoyama H, Imaoka A, Uematsu S, Akira S, Domino SE, Kulig P, Becher B, Renauld JC, Sasakawa C, Umesaki Y, Benno Y, Kiyono H (September 2014). Innate lymphoid cells regulate intestinal epithelial cell glycosylation. Science 345 (6202). PMID 25214634. PMC 4774895. DOI: 10.1126/science.1254009.
- ↑ Macpherson AJ, Yilmaz B, Limenitakis JP, Ganal-Vonarburg SC (April 2018). IgA Function in Relation to the Intestinal Microbiota. Annual Review of Immunology 36 (1): 359–381. PMID 29400985. DOI: 10.1146/annurev-immunol-042617-053238.
- ↑ Abt MC, Lewis BB, Caballero S, Xiong H, Carter RA, Sušac B, Ling L, Leiner I, Pamer EG (July 2015). Innate Immune Defenses Mediated by Two ILC Subsets Are Critical for Protection against Acute Clostridium difficile Infection. Cell Host & Microbe 18 (1): 27–37. PMID 26159718. PMC 4537644. DOI: 10.1016/j.chom.2015.06.011.
- 1 2 3 4 5 Wagner M, Moro K, Koyasu S (May 2017). Plastic Heterogeneity of Innate Lymphoid Cells in Cancer. Trends in Cancer 3 (5): 326–335. PMID 28718410. DOI: 10.1016/j.trecan.2017.03.008.
- 1 2 Wagner M, Koyasu S (May 2019). Cancer Immunoediting by Innate Lymphoid Cells. Trends in Immunology 40 (5): 415–430. PMID 30992189. DOI: 10.1016/j.it.2019.03.004.
- ↑ Dadi S, Chhangawala S, Whitlock BM, Franklin RA, Luo CT, Oh SA, Toure A, Pritykin Y, Huse M, Leslie CS, Li MO (January 2016). Cancer Immunosurveillance by Tissue-Resident Innate Lymphoid Cells and Innate-like T Cells. Cell 164 (3): 365–77. PMID 26806130. PMC 4733424. DOI: 10.1016/j.cell.2016.01.002.
- ↑ Cerwenka A, Lanier LL (October 2001). Natural killer cells, viruses and cancer. Nature Reviews. Immunology 1 (1): 41–9. PMID 11905813. DOI: 10.1038/35095564.
- ↑ Smyth MJ, Godfrey DI, Trapani JA (April 2001). A fresh look at tumor immunosurveillance and immunotherapy. Nature Immunology 2 (4): 293–9. PMID 11276199. DOI: 10.1038/86297.
- ↑ Fuchs A, Vermi W, Lee JS, Lonardi S, Gilfillan S, Newberry RD, Cella M, Colonna M (April 2013). Intraepithelial type 1 innate lymphoid cells are a unique subset of IL-12- and IL-15-responsive IFN-γ-producing cells. Immunity 38 (4): 769–81. PMID 23453631. PMC 3634355. DOI: 10.1016/j.immuni.2013.02.010.
- ↑ Lechner MG, Liebertz DJ, Epstein AL (August 2010). Characterization of cytokine-induced myeloid-derived suppressor cells from normal human peripheral blood mononuclear cells. Journal of Immunology 185 (4): 2273–84. PMID 20644162. PMC 2923483. DOI: 10.4049/jimmunol.1000901.
- ↑ Heeren, A. Marijne, et al. "High and interrelated rates of PD-L1+ CD14+ antigen-presenting cells and regulatory T cells mark the microenvironment of metastatic lymph nodes from patients with cervical cancer." Cancer immunology research (2014): canimm-0149.
- ↑ Zhu J (September 2015). T helper 2 (Th2) cell differentiation, type 2 innate lymphoid cell (ILC2) development and regulation of interleukin-4 (IL-4) and IL-13 production. Cytokine 75 (1): 14–24. PMID 26044597. PMC 4532589. DOI: 10.1016/j.cyto.2015.05.010.
- ↑ Ikutani M, Yanagibashi T, Ogasawara M, Tsuneyama K, Yamamoto S, Hattori Y, Kouro T, Itakura A, Nagai Y, Takaki S, Takatsu K (January 2012). Identification of innate IL-5-producing cells and their role in lung eosinophil regulation and antitumor immunity. Journal of Immunology 188 (2): 703–13. PMID 22174445. DOI: 10.4049/jimmunol.1101270.
- ↑ Wagner M, Ealey KN, Tetsu H, Kiniwa T, Motomura Y, Moro K, Koyasu S (February 2020). Tumor-Derived Lactic Acid Contributes to the Paucity of Intratumoral ILC2s. Cell Reports 30 (8): 2743–2757.e5. PMID 32101749. DOI: 10.1016/j.celrep.2020.01.103.
- ↑ Ducimetière L, Vermeer M, Tugues S (2019). The Interplay Between Innate Lymphoid Cells and the Tumor Microenvironment. Frontiers in Immunology 10. PMID 31921156. PMC 6923277. DOI: 10.3389/fimmu.2019.02895.
- ↑ Carrega P, Loiacono F, Di Carlo E, Scaramuccia A, Mora M, Conte R, Benelli R, Spaggiari GM, Cantoni C, Campana S, Bonaccorsi I, Morandi B, Truini M, Mingari MC, Moretta L, Ferlazzo G (September 2015). NCR(+)ILC3 concentrate in human lung cancer and associate with intratumoral lymphoid structures. Nature Communications 6 (1). PMID 26395069. DOI: 10.1038/ncomms9280.
- 1 2 Ochel A, Tiegs G, Neumann K (April 2019). Type 2 Innate Lymphoid Cells in Liver and Gut: From Current Knowledge to Future Perspectives. International Journal of Molecular Sciences 20 (8). PMID 30999584. PMC 6514972. DOI: 10.3390/ijms20081896.
- 1 2 Nabekura T, Riggan L, Hildreth AD, O'Sullivan TE, Shibuya A (January 2020). Type 1 Innate Lymphoid Cells Protect Mice from Acute Liver Injury via Interferon-γ Secretion for Upregulating Bcl-xL Expression in Hepatocytes. Immunity 52 (1): 96–108.e9. PMID 31810881. PMC 8108607. DOI: 10.1016/j.immuni.2019.11.004.
- 1 2 (en) Brestoff JR, Kim BS, Saenz SA, Stine RR, Monticelli LA, Sonnenberg GF, Thome JJ, Farber DL, Lutfy K, Seale P, Artis D (March 2015). Group 2 innate lymphoid cells promote beiging of white adipose tissue and limit obesity. Nature 519 (7542): 242–6. PMID 25533952. PMC 4447235. DOI: 10.1038/nature14115.
- ↑ Lee BC, Kim MS, Pae M, Yamamoto Y, Eberlé D, Shimada T, Kamei N, Park HS, Sasorith S, Woo JR, You J, Mosher W, Brady HJ, Shoelson SE, Lee J (April 2016). Adipose Natural Killer Cells Regulate Adipose Tissue Macrophages to Promote Insulin Resistance in Obesity. Cell Metabolism 23 (4): 685–98. PMID 27050305. PMC 4833527. DOI: 10.1016/j.cmet.2016.03.002.
- ↑ Turner JE, Morrison PJ, Wilhelm C, Wilson M, Ahlfors H, Renauld JC, Panzer U, Helmby H, Stockinger B (December 2013). IL-9-mediated survival of type 2 innate lymphoid cells promotes damage control in helminth-induced lung inflammation. The Journal of Experimental Medicine 210 (13): 2951–65. PMID 24249111. PMC 3865473. DOI: 10.1084/jem.20130071.
- ↑ Huang Y, Mao K, Chen X, Sun MA, Kawabe T, Li W, Usher N, Zhu J, Urban JF, Paul WE, Germain RN (January 2018). S1P-dependent interorgan trafficking of group 2 innate lymphoid cells supports host defense. Science 359 (6371): 114–119. PMID 29302015. PMC 6956613. DOI: 10.1126/science.aam5809.
- ↑ Van Maele L, Carnoy C, Cayet D, Ivanov S, Porte R, Deruy E, Chabalgoity JA, Renauld JC, Eberl G, Benecke AG, Trottein F, Faveeuw C, Sirard JC (August 2014). Activation of Type 3 innate lymphoid cells and interleukin 22 secretion in the lungs during Streptococcus pneumoniae infection. The Journal of Infectious Diseases 210 (3): 493–503. PMID 24577508. DOI: 10.1093/infdis/jiu106.
- ↑ Panda SK, Colonna M (7 mei 2019). Innate Lymphoid Cells in Mucosal Immunity. Frontiers in Immunology 10. PMID 31134050. PMC 6515929. DOI: 10.3389/fimmu.2019.00861.
- ↑ Vivier E, Artis D, Colonna M, Diefenbach A, Di Santo JP, Eberl G, Koyasu S, Locksley RM, McKenzie AN, Mebius RE, Powrie F, Spits H (August 2018). Innate Lymphoid Cells: 10 Years On. Cell 174 (5): 1054–1066. PMID 30142344. DOI: 10.1016/j.cell.2018.07.017.
- ↑ Domingues RG, Hepworth MR (6 februari 2020). Immunoregulatory Sensory Circuits in Group 3 Innate Lymphoid Cell (ILC3) Function and Tissue Homeostasis. Frontiers in Immunology 11. PMID 32117267. PMC 7015949. DOI: 10.3389/fimmu.2020.00116.
- 1 2 Bal SM, Bernink JH, Nagasawa M, Groot J, Shikhagaie MM, Golebski K, van Drunen CM, Lutter R, Jonkers RE, Hombrink P, Bruchard M, Villaudy J, Munneke JM, Fokkens W, Erjefält JS, Spits H, Ros XR (June 2016). IL-1β, IL-4 and IL-12 control the fate of group 2 innate lymphoid cells in human airway inflammation in the lungs. Nature Immunology 17 (6): 636–45. PMID 27111145. DOI: 10.1038/ni.3444.
- ↑ Cella M, Otero K, Colonna M (June 2010). Expansion of human NK-22 cells with IL-7, IL-2, and IL-1beta reveals intrinsic functional plasticity. Proceedings of the National Academy of Sciences of the United States of America 107 (24): 10961–6. PMID 20534450. PMC 2890739. DOI: 10.1073/pnas.1005641107.
- 1 2 Bernink JH, Krabbendam L, Germar K, de Jong E, Gronke K, Kofoed-Nielsen M, Munneke JM, Hazenberg MD, Villaudy J, Buskens CJ, Bemelman WA, Diefenbach A, Blom B, Spits H (July 2015). Interleukin-12 and -23 Control Plasticity of CD127(+) Group 1 and Group 3 Innate Lymphoid Cells in the Intestinal Lamina Propria. Immunity 43 (1): 146–60. PMID 26187413. DOI: 10.1016/j.immuni.2015.06.019.
- ↑ Zhang K, Xu X, Pasha MA, Siebel CW, Costello A, Haczku A, MacNamara K, Liang T, Zhu J, Bhandoola A, Maillard I, Yang Q (March 2017). Cutting Edge: Notch Signaling Promotes the Plasticity of Group-2 Innate Lymphoid Cells. Journal of Immunology 198 (5): 1798–1803. PMID 28115527. PMC 5321819. DOI: 10.4049/jimmunol.1601421.
- 1 2 Meininger I, Carrasco A, Rao A, Soini T, Kokkinou E, Mjösberg J (October 2020). Tissue-Specific Features of Innate Lymphoid Cells. Trends in Immunology 41 (10): 902–917. PMID 32917510. DOI: 10.1016/j.it.2020.08.009.
- ↑ Gao Y, Souza-Fonseca-Guimaraes F, Bald T, Ng SS, Young A, Ngiow SF, Rautela J, Straube J, Waddell N, Blake SJ, Yan J, Bartholin L, Lee JS, Vivier E, Takeda K, Messaoudene M, Zitvogel L, Teng MW, Belz GT, Engwerda CR, Huntington ND, Nakamura K, Hölzel M, Smyth MJ (September 2017). Tumor immunoevasion by the conversion of effector NK cells into type 1 innate lymphoid cells. Nature Immunology 18 (9): 1004–1015. PMID 28759001. DOI: 10.1038/ni.3800.
- ↑ Cortez VS, Ulland TK, Cervantes-Barragan L, Bando JK, Robinette ML, Wang Q, White AJ, Gilfillan S, Cella M, Colonna M (September 2017). SMAD4 impedes the conversion of NK cells into ILC1-like cells by curtailing non-canonical TGF-β signaling. Nature Immunology 18 (9): 995–1003. PMID 28759002. PMC 5712491. DOI: 10.1038/ni.3809.
- ↑ Bald T, Wagner M, Gao Y, Koyasu S, Smyth MJ (February 2019). Hide and seek: Plasticity of innate lymphoid cells in cancer. Seminars in Immunology 41. PMID 30979591. DOI: 10.1016/j.smim.2019.04.001.
- ↑ Halim TY, Steer CA, Mathä L, Gold MJ, Martinez-Gonzalez I, McNagny KM, McKenzie AN, Takei F (March 2014). Group 2 innate lymphoid cells are critical for the initiation of adaptive T helper 2 cell-mediated allergic lung inflammation. Immunity 40 (3): 425–35. PMID 24613091. PMC 4210641. DOI: 10.1016/j.immuni.2014.01.011.
- ↑ Oboki K, Nakae S, Matsumoto K, Saito H (April 2011). IL-33 and Airway Inflammation. Allergy, Asthma & Immunology Research 3 (2): 81–8. PMID 21461246. PMC 3062800. DOI: 10.4168/aair.2011.3.2.81.
- ↑ Kondo H, Ichikawa Y, Imokawa G (March 1998). Percutaneous sensitization with allergens through barrier-disrupted skin elicits a Th2-dominant cytokine response. European Journal of Immunology 28 (3): 769–79. PMID 9541570. DOI: <769::AID-IMMU769>3.0.CO;2-H 10.1002/(SICI)1521-4141(199803)28:03<769::AID-IMMU769>3.0.CO;2-H.
- ↑ Kim HY, Lee HJ, Chang YJ, Pichavant M, Shore SA, Fitzgerald KA, Iwakura Y, Israel E, Bolger K, Faul J, DeKruyff RH, Umetsu DT (January 2014). Interleukin-17-producing innate lymphoid cells and the NLRP3 inflammasome facilitate obesity-associated airway hyperreactivity. Nature Medicine 20 (1): 54–61. PMID 24336249. PMC 3912313. DOI: 10.1038/nm.3423.
- ↑ Vivier E, Raulet DH, Moretta A, Caligiuri MA, Zitvogel L, Lanier LL, Yokoyama WM, Ugolini S (January 2011). Innate or adaptive immunity? The example of natural killer cells. Science 331 (6013): 44–9. PMID 21212348. PMC 3089969. DOI: 10.1126/science.1198687.
- ↑ Baxter AG, Smyth MJ (February 2002). The role of NK cells in autoimmune disease. Autoimmunity 35 (1): 1–14. PMID 11908701. DOI: 10.1080/08916930290005864.
- ↑ Scordamaglia F, Balsamo M, Scordamaglia A, Moretta A, Mingari MC, Canonica GW, Moretta L, Vitale M (February 2008). Perturbations of natural killer cell regulatory functions in respiratory allergic diseases. The Journal of Allergy and Clinical Immunology 121 (2): 479–85. PMID 18061653. DOI: 10.1016/j.jaci.2007.09.047.
- ↑ Langowski JL, Zhang X, Wu L, Mattson JD, Chen T, Smith K, Basham B, McClanahan T, Kastelein RA, Oft M (July 2006). IL-23 promotes tumour incidence and growth. Nature 442 (7101): 461–5. PMID 16688182. DOI: 10.1038/nature04808.
- ↑ Wu S, Rhee KJ, Albesiano E, Rabizadeh S, Wu X, Yen HR, Huso DL, Brancati FL, Wick E, McAllister F, Housseau F, Pardoll DM, Sears CL (September 2009). A human colonic commensal promotes colon tumorigenesis via activation of T helper type 17 T cell responses. Nature Medicine 15 (9): 1016–22. PMID 19701202. PMC 3034219. DOI: 10.1038/nm.2015.
- ↑ Grivennikov SI, Wang K, Mucida D, Stewart CA, Schnabl B, Jauch D, Taniguchi K, Yu GY, Osterreicher CH, Hung KE, Datz C, Feng Y, Fearon ER, Oukka M, Tessarollo L, Coppola V, Yarovinsky F, Cheroutre H, Eckmann L, Trinchieri G, Karin M (November 2012). Adenoma-linked barrier defects and microbial products drive IL-23/IL-17-mediated tumour growth. Nature 491 (7423): 254–8. PMID 23034650. PMC 3601659. DOI: 10.1038/nature11465.
- ↑ Bie Q, Zhang P, Su Z, Zheng D, Ying X, Wu Y, Yang H, Chen D, Wang S, Xu H (2014). Polarization of ILC2s in peripheral blood might contribute to immunosuppressive microenvironment in patients with gastric cancer. Journal of Immunology Research 2014. PMID 24741632. PMC 3987940. DOI: 10.1155/2014/923135.
- ↑ Lee J, Park KH, Ryu JH, Bae HJ, Choi A, Lee H, Lim J, Han K, Park CH, Jung ES, Oh EJ (September 2017). Natural killer cell activity for IFN-gamma production as a supportive diagnostic marker for gastric cancer. Oncotarget 8 (41): 70431–70440. PMID 29050291. PMC 5642566. DOI: 10.18632/oncotarget.19712.
- 1 2 Sonnenberg GF, Hepworth MR (October 2019). Functional interactions between innate lymphoid cells and adaptive immunity. Nature Reviews. Immunology 19 (10): 599–613. PMID 31350531. PMC 6982279. DOI: 10.1038/s41577-019-0194-8.