Tumorgeassocieerde neutrofiele granulocyt

Tumorgeassocieerde neutrofiele granulocyten (Engels: Tumor Associated Neutrophils (TANs)) zijn neutrofiele granulocyten. Ze kunnen de tumorprogressie en groeicontrole reguleren.
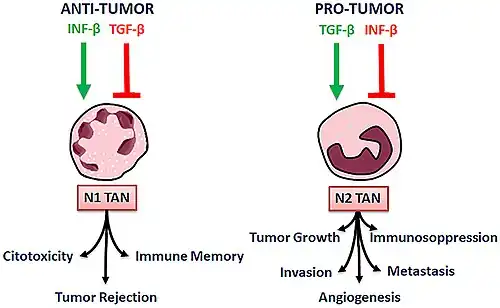
Net als macrofagen kunnen TAN's een antitumoractiviteit (N1-neutrofielen) of een protumoractiviteit (N2-neutrofielen) verwerven. N1-activiteit tegen tumorgroei en metastasering wordt uitgeoefend door directe of antilichaamafhankelijke cytotoxiciteit, evenals door de activering van verschillende aangeboren en verworven immuuncellen, waaronder T-cellen, B-cellen, NK-cellen en dendritische cellen.[1]
Wanneer TGF-β-activiteit wordt geblokkeerd, worden N1-TAN's cytotoxisch voor tumorcellen en activeren ze cytotoxische T-cellen, terwijl N2-TAN's dominant zijn in de controlegroep. TGF-β bevordert op zichzelf het pro-tumorigene N2-fenotype in TAN's bij muizen. Naast TGF-β wordt de polarisatie van TAN's ook bevorderd door de cytokines IFN-β. IFN-β stimuleert N1- en remt de N2-polarisatie, terwijl TGF-β juist N2 stimuleert en de fenotypische N1-polarisatie remt. Door TGF-β te blokkeren, wordt een significante vertraging van de tumorgroei bereikt via vele mechanismen, waaronder de activering van cytotoxische T-cellen en macrofagen.
N1-TAN's vertonen een verhoogde NADPH-oxidaseactiviteit, wat leidt tot de productie van reactieve zuurstofcomponenten, die op hun beurt cytotoxisch zijn voor tumorcellen. N2-TAN's daarentegen bevorderen, direct of indirect, tumorgroei en de verspreiding van tumorcellen door de secretie van extracellulaire matrix-hervormde enzymen en pro-angiogene factoren die metastasering en angiogenese bevorderen. De meeste studies naar TAN's zijn uitgevoerd in muizenmodellen, vanwege de technische beperkingen bij het verkrijgen van TAN's uit menselijk tumorweefsel. Helaas verschillen muis- en menselijke neutrofiele granulocyten sterk in hun biologie en functies. De tumorgroei in muizenmodellen geeft dus geen accuraat beeld van de geleidelijke ontwikkeling van tumoren en de complexe interacties tussen tumorcellen en tumormicro-omgevingscellen die bij mensen voorkomen. Bovendien, hoewel experimentele studies met muizen de protumor- en antitumorfuncties van neutrofiele granulocyten bij kanker aantonen, is er geen direct bewijs voor protumorale activiteit van neutrofiele granulocyten in menselijke tumorweefsels en blijft de N1/N2-polarisatie van TAN's bij mensen tot nu toe onzeker.[1]
Het immuunprofiel van N1-TAN's wordt gekenmerkt door hoge niveaus van TNF-α, CCL3, ICAM-1 en lage niveaus van de arginase-as, terwijl N2-TAN's worden gekenmerkt door een upregulatie van de chemokines CCL2, CCL3, CCL4, CCL8, CCL12 en CCL17, en CXCL1, CXCL2, IL-8/CXCL8 en CXCL16.[1]
Longkanker
TAN's kunnen een verhoogde extracellulaire verzuringssnelheid vertonen wanneer er sprake is van een toename in glycolyseniveaus.[2] Wanneer er een metabole verschuiving optreedt in TAN's, kan dit leiden tot tumorprogressie in bepaalde delen van het lichaam, zoals de longen. N2-TAN's ondersteunen de groei en progressie van tumoren, in tegenstelling tot normale neutrofiele granulocyten, die tumorprogressie zouden remmen door fagocytose van tumorcellen. Met behulp van een muismodel ontdekten ze dat zowel het GLUT-1- als het glucosemetabolisme verhoogden in N2-TAN's die werden aangetroffen in een muis met longkanker.[2] Een onderzoek toonde aan dat longtumorcellen op afstand osteoblasten kunnen initiëren en dat deze osteoblasten tumoren op twee manieren kunnen verergeren. Ten eerste kunnen ze de vorming van SiglecFhigh-expressieve neutrofiele granulocyten induceren, wat op zijn beurt de groei en progressie van longtumoren bevordert. Ten tweede kunnen osteoblasten de botgroei bevorderen en zo een gunstige omgeving creëren voor tumorcellen om te groeien en botmetastasen te vormen.[3]
- 1 2 3 Masucci MT, Minopoli M, Carriero MV (2019 Nov 15 volume=9). Tumor Associated Neutrophils. Their Role in Tumorigenesis, Metastasis, Prognosis and Therapy. Front Oncol.: 1146. PMID 31799175. PMC 6874146. DOI: 10.3389/fonc.2019.01146. Open Access. CC-BY 4.0
- 1 2 Ancey PB, Contat C, Boivin G, Sabatino S, Pascual J, Zangger N, Perentes JY, Peters S, Abel ED, Kirsch DG, Rathmell JC, Vozenin MC, Meylan E (May 2021). GLUT1 Expression in Tumor-Associated Neutrophils Promotes Lung Cancer Growth and Resistance to Radiotherapy. Cancer Research 81 (9): 2345–2357. PMID 33753374. PMC 8137580. DOI: 10.1158/0008-5472.CAN-20-2870.
- ↑ Azevedo PO, Paiva AE, Santos GS, Lousado L, Andreotti JP, Sena IF, Tagliati CA, Mintz A, Birbrair A (December 2018). Cross-talk between lung cancer and bones results in neutrophils that promote tumor progression. Cancer and Metastasis Reviews 37 (4): 779–790. PMID 30203108. PMC 6358512. DOI: 10.1007/s10555-018-9759-4.