Regulerende B-cel

Regulerende B-cellen (Engels: B regulatory cells, Bregs of Breg-cells) vormen een kleine populatie B-cellen die betrokken is bij immunomodulatie en de onderdrukking van immuunreacties. De populatie Bregs is zeer heterogeen en kan worden onderverdeeld in verschillende subgroepen, zoals B10-cellen, B-geheugencellen, transitionele B-cellen, marginale zone B-cellen, Br1-cellen, GrB+-B-cellen, CD9+-B-cellen en zelfs enkele plasmablasten of plasmacellen, waarbij fenotypische verschillen tussen de subgroepen zijn beschreven bij mensen en muizen.[1] Plasmablasten scheiden meer antilichamen uit dan B-cellen, maar minder dan plasmacellen.[1] Ze delen zich snel en zijn nog steeds in staat antigenen op te nemen en deze aan T-cellen te presenteren. Een cel kan enkele dagen in deze toestand blijven en vervolgens afsterven of onherroepelijk differentiëren. in een volwassen, volledig gedifferentieerde plasmacel.[1]
Bregs reguleren het immuunsysteem via verschillende mechanismen. Een van de belangrijkste mechanismen is de productie van ontstekingsremmende cytokinen zoals IL-10, IL-35 of TGF-β. Een ander bekend mechanisme is de productie van cytotoxisch granzyme B (GrB). Bregs brengen ook verschillende remmende oppervlaktemarkers tot expressie, zoals PD-L1, CD39, CD73 en arylhydrocarbonreceptor. De regulerende effecten van Bregs zijn beschreven in verschillende modellen van ontsteking, auto-immuunziekten, transplantatiereacties en in antitumor-immuniteit.[2][3][4]
Ontwikkeling en populaties
Bregs kunnen zich ontwikkelen uit verschillende subsets van B-cellen, zoals onrijpe en rijpe B-cellen of plasmablasten. Of Bregs uniek afkomstig zijn van een specifieke voorlopercel of ontstaan binnen conventionele B-celsubsets, is nog steeds een open vraag.[2][5] Helaas zijn Bregs moeilijker te definiëren dan regulatoire T-cellen (Tregs), omdat ze geen afstammings-marker hebben die analoog is aan de Treg-celmarker - FOXP3.[6] Bregs delen veel markers met verschillende B-celsubsets vanwege hun oorsprong. Menselijke en muizen-Bregs kunnen verder worden onderverdeeld in vele subsets vanwege hun verschillende werkingsmechanismen en de verschillende expressie van belangrijke oppervlaktemarkers (zie onderstaande tabel). Naar schatting kunnen IL-10-producerende B-celsubpopulaties tot 10% van de circulerende menselijke B-cellen uitmaken.[7] Er is nog steeds geen duidelijke consensus over de classificatie en definitie van Bregs.[2] Muizen-Bregs waren voornamelijk CD5- en CD1d-positief in het EAE-model of na blootstelling aan Leishmania major.[8][9] Daarentegen waren muizen-Bregs in het collageen-geïnduceerde artritismodel (CIA) voornamelijk CD21- en CD23-positief.[10] Bregs werden ook bij mensen gevonden. Markers voor perifeer bloed-Bregs waren de moleculen CD24 en CD38.[11] Perifeer bloed-Bregs waren echter voornamelijk CD24- en CD27-positief na kweek met anti-CD40-antilichaam en CpG-bacterieel DNA.[12] Ze waren ook positief voor CD25, CD71 en PD-L1 na stimulatie met CpG-bacterieel DNA en via TLR9.[13]
| Subgroep | Soort | Fenotype | Functie |
|---|---|---|---|
| B10-cellen | mens, muis | CD24hoogCD27+ (mens), CD5+CD1dhoog (muis) | productie van IL-10, onderdrukking van effector CD4+ T-cellen, monocyten en dendritische cellen[2][3] |
| Plasmablasten | mens, muis | CD19+CD24hoogCD27intermediair (mens), CD138+CD44hoog (muis) | productie van IL-10 en TGF-β, onderdrukking van dendritische cellen en effector T-helpercellen[2][3][4] Een effector T-helpercel is een geactiveerde cel die cytokinen uitscheidt. |
| Plasmacellen | muis | CD138+MHC-11laagB220+ | productie van IL-10 en IL-35, onderdrukking van NK-cellen, neutrofiele granulocyten en effector T-helpercellen[2][3][4] |
| Marginale zone B-cellen | mens, muis | CD19+CD21hoogCD23− | productie van IL-10, inductie van regulatoire T-cellen, onderdrukking van effector T-helpercellen en cytotoxische T-cellen[2][3][4][7] |
| Br1-cellen | mens | CD19+CD25hoogCD71hoog CD73− | productie van IL-10, onderdrukking van ontstekingsreacties, inductie van regulerende T-cellen en bevordering van IgG4-productie[2] |
| GrB+B-cellen | mens | CD19+CD38+CD1d+IgM+CD147+ | productie van granzyme B, afbraak van de T-celreceptor, remming van T-helpercelproliferatie en Th1- en Th17-cel-reacties[2][4] |
| CD9+B-cellen | mens, muis | CD19+CD9+ | productie van IL-10, onderdrukking van Th2- en Th17-cel-ontsteking[2] |
| CD5+CD1d+ cellen | mens | CD19+CD5+CD1dhoog | productie van IL-10, onderdrukking van Th17-cel-respons[2] |
| B1a-cellen | muis | CD19+CD5+ | productie van IL-10, onderdrukking van Toll-like receptor-gemedieerde ontsteking[2] |
| Killer B-cellen | muis | CD19+CD5+FasL+ | inductie van T-celdood[2] |
| Tim-1+ B-cellen | muis | Tim-1+CD19+ | productie van IL-10, versterking van Th2- en regulatoire T-cel-responsen, regulatie van Th1- en Th17-cellen tijdens ontsteking[2][3][14] |
| T2-MZP-cellen | muis | CD19+CD21hoogCD23hoog | productie van IL-10, onderdrukking van effector T-helpercellen, cytotoxische T-cellen en inductie van regulatoire T-cellen[2][3][14] |
Werkingsmechanismen
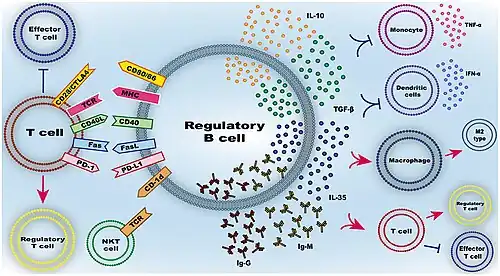
Er zijn verschillende werkingsmechanismen van Breg. Het meest onderzochte mechanisme is echter de productie van IL-10. IL-10 heeft sterke ontstekingsremmende effecten.[15][16] Het remt (of onderdrukt) ontstekingsreacties die worden gemedieerd door T-cellen, met name Th1- en Th17-celtype immuunreacties. Dit is bijvoorbeeld aangetoond in modellen van EAE (auto-immuunencefalomyelitis,[17] CCIA (chronische collageen-geïnduceerde artritis)[18] of contactovergevoeligheid.[19] Evenzo is aangetoond dat regulerende B-celsubtypen Th1-reacties remmen door IL-10-productie tijdens chronische infectieziekten zoals viscerale (ingewanden) leishmaniasis.[20] Door de productie van IL-10 zijn Bregs ook in staat om naïeve T-helpercellen om te zetten in regulatoire T-cellen en IL-10-afscheidende type 1 regulatoire T-cellen. Dit is waargenomen in verschillende experimentele modellen en bij chronisch virusgeïnfecteerde patiënten.[4] Een ander mechanisme van Breg-onderdrukking is de productie van TGF-β, een anti-inflammatoire cytokine.[15] De rol van TGF-β-producerende Bregs werd gevonden in muismodellen van SLE[21] en diabetes.[22] De laatste anti-inflammatoire cytokine die alleen door sommige Bregs wordt geproduceerd, is IL-35, die een rol speelt bij de regulatoire T-cellenconversie. Breg-cellen zijn in staat om IL-35-bevattende exosomen vrij te geven. Het is nog niet duidelijk of IL-10- en IL-35-producerende Bregs overeenkomen met afzonderlijke populaties of een zekere mate van overlap vertonen.[4] Naast de productie van immunomodulerende cytokines geven Bregs ook cytotoxisch granzyme B vrij, dat betrokken is bij de afbraak van de T-celreceptor en T-celapoptose.[7] Een ander mechanisme voor de onderdrukking van Breg-cellen omvat oppervlaktemoleculen zoals FasL, dat T-celdood induceert,[23] of PD-1 en PD-L1. Er is aangetoond dat PD-1+ Bregs de activiteit van T-helpercellen en cytotoxische T-cellen onderdrukken en type 1 regulatoire T-cellen induceren, terwijl van PD-L1 Bregs is gemeld dat ze de cytotoxiciteit van NK-cellen en cytotoxische T-cellen remmen.[4] Sommige Bregs brengen ook aanvullende onderdrukkende moleculen tot expressie, zoals CD39, CD73 en de arylhydrocarbonreceptor.[2]
Activering
Rustende B-cellen produceren geen cytokinen. Na een reactie op een antigeen of verschillende stimuli zoals lipopolysaccharide (LPS) worden pro- en anti-inflammatoire cytokinen TNFα, IL-1β, IL-10 en IL-6 geproduceerd. Dit betekent dat de Breg gestimuleerd moet worden om onderdrukkende cytokinen te produceren. Er zijn twee soorten signalen die Breg activeren, namelijk signalen gegenereerd door externe pathogenen (PAMPs) en endogene signalen geproduceerd door de werking van lichaamscellen. PAMPs worden herkend door Toll-like receptoren (TLR's). TLR's triggeren een signaalcascade aan het einde waarvan de productie van effectorcytokinen plaatsvindt. Breg's worden voornamelijk gegenereerd na herkenning van TLR4- of TLR9-liganden - LPS en CpG. Het belangrijkste endogene signaal is de stimulatie van het oppervlaktemolecuul CD40.[2][3] Er is ook gesuggereerd dat sommige ontstekingsremmende factoren, zoals IL-35 en retinezuur, het Breg-fenotype kunnen induceren. Bovendien is aangetoond dat cytokine IL-21, samen met CD40-ligand en/of TLR9-signalen, de aanmaak van B10-cellen en het ontstaan van IL-10-producerende plasmablasten tijdens ontstekingsprocessen induceert.[4] Verder is de behandeling van primaire humane B-cellen met een combinatie van CD40L, CpG en IL-21 bijzonder effectief voor het in vitro induceren van functioneel actieve transitionele (CD24hoogCD27+) en geheugen (CD24hoogCD27+) Breg-subtypen, wat omstandigheden creëert die nuttig kunnen zijn voor potentiële adoptieve overdracht van Bregs.[24]
Geschiedenis
De geschiedenis van het Breg-onderzoek kan worden beschreven als een ontwikkeling in vier tijdperken: vroege functionele ontdekkingen (jaren 60-90), terminologie en initiële fenotypische karakterisering (jaren 2000), mechanistische en therapeutische uitbreiding (jaren 2010) en de huidige, door omics gedreven fase (jaren 2020-heden).[25] In de jaren 60 en 70 werd opgemerkt dat B-cellen immuunreacties konden onderdrukken die verder gingen dan de productie van antilichamen.[26][27] In 1996 observeerde de groep van Janeway een immunomodulatie van experimentele auto-immuunencefalomyelitis (EAE) door B-cellen.[28] Soortgelijke resultaten werden een jaar later aangetoond in een model van chronische colitis.[29] Vervolgens werd een rol van Bregs gevonden in veel muismodellen van auto-immuunziekten zoals reumatoïde artritis[30] of systemische lupus erythematosus (SLE).[21]
Tumoren

Tumor-infiltrerende B-cellen bestaan uit verschillende fenotypen, waaronder zowel effector- als regulatoire B-cellen. IL-10- of granzyme B-producerende Bregs zijn aangetroffen in diverse menselijke kankers. Bovendien hebben de meeste studies een positieve correlatie gerapporteerd tussen Breg-cellen en Treg-cellen, wat wijst op een interactie tussen deze subgroepen.[31] Er is waargenomen dat er hogere frequenties van IL-10-producerende B-cellen werden gevonden in monsters van slokdarmkanker in een laat stadium dan in monsters van slokdarmkanker in een vroeg stadium.[31] Leukemie-B-cellen produceren spontaan grote hoeveelheden IL-10.[32] Bovendien werden verhoogde niveaus van Bregs aangetroffen in het perifeer bloed en beenmerg van patiënten met acute myeloïde leukemie. IL-10-producerende Bregs zijn ook aanwezig in maagkanker, borstkanker, plaveiselcelcarcinoom van hoofd en hals en plaveiselcelcarcinoom van de slokdarm. Het bewijs suggereert een immunosuppressieve rol van Breg bij kanker en het is mogelijk dat kankercellen Bregs gebruiken om aan de immuunrespons te ontsnappen.[31]
In de tumoromgeving onderdrukken Bregs effector-T-cellen, induceren ze regulatoire T-cellen (Tregs) en richten ze zich op andere tumorinfiltrerende immuuncellen, zoals myeloïde suppressorcellen, NK-cellen en macrofagen, om de antitumorimmuniteit te belemmeren. Tegelijkertijd leidt de onderlinge regulatie tussen Bregs en tumorcellen er vaak toe dat de tumor ontsnapt aan immuunbewaking.[33]
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Regulatory B cell op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
Referenties
- 1 2 3 Walport M, Murphy K, Janeway C, Travers PJ (2008). Janeway's immunobiology. Garland Science, New York, 387–388. ISBN 978-0-8153-4123-9.
- 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 (en) Jansen, Kirstin, Cevhertas, Lacin, Ma, Siyuan, Satitsuksanoa, Pattraporn, Akdis, Mübeccel (September 2021). O'Hehir, Robyn (red.). Regulatory B cells, A to Z. Allergy 76 (9): 2699–2715. ISSN: 0105-4538. PMID 33544905. DOI: 10.1111/all.14763.
- 1 2 3 4 5 6 7 8 (April 2015). Regulatory B cells: origin, phenotype, and function. Immunity 42 (4): 607–12. PMID 25902480. DOI: 10.1016/j.immuni.2015.04.005.
- 1 2 3 4 5 6 7 8 9 Catalán, Diego, Mansilla, Miguel Andrés, Ferrier, Ashley, Soto, Lilian, Oleinika, Kristine (2021). Immunosuppressive Mechanisms of Regulatory B Cells. Frontiers in Immunology 12. ISSN: 1664-3224. PMID 33995344. PMC 8118522. DOI: 10.3389/fimmu.2021.611795.
- ↑ Vitale G, Mion F, Pucillo C (Nov–Dec 2010). Regulatory B cells: evidence, developmental origin and population diversity. Molecular Immunology 48 (1–3): 1–8. PMID 20950861. DOI: 10.1016/j.molimm.2010.09.010.
- ↑ (en) Laumont, Céline M., Banville, Allyson C., Gilardi, Mara, Hollern, Daniel P., Nelson, Brad H. (July 2022). Tumour-infiltrating B cells: immunological mechanisms, clinical impact and therapeutic opportunities. Nature Reviews Cancer 22 (7): 414–430. ISSN: 1474-175X. PMID 35393541. PMC 9678336. DOI: 10.1038/s41568-022-00466-1.
- 1 2 3 (en) Menon, Madhvi, Hussell, Tracy, Ali Shuwa, Halima (January 2021). Regulatory B cells in respiratory health and diseases. Immunological Reviews 299 (1): 61–73. ISSN: 0105-2896. PMID 33410165. PMC 7986090. DOI: 10.1111/imr.12941.
- ↑ Matsushita T, Yanaba K, Bouaziz JD, Fujimoto M, Tedder TF (October 2008). Regulatory B cells inhibit EAE initiation in mice while other B cells promote disease progression. The Journal of Clinical Investigation 118 (10): 3420–30. PMID 18802481. PMC 2542851. DOI: 10.1172/JCI36030.
- ↑ Ronet C, Hauyon-La Torre Y, Revaz-Breton M, Mastelic B, Tacchini-Cottier F, Louis J, Launois P (January 2010). Regulatory B cells shape the development of Th2 immune responses in BALB/c mice infected with Leishmania major through IL-10 production. Journal of Immunology 184 (2): 886–94. PMID 19966209. DOI: 10.4049/jimmunol.0901114.
- ↑ Evans JG, Chavez-Rueda KA, Eddaoudi A, Meyer-Bahlburg A, Rawlings DJ, Ehrenstein MR, Mauri C (June 2007). Novel suppressive function of transitional 2 B cells in experimental arthritis. Journal of Immunology 178 (12): 7868–78. PMID 17548625. DOI: 10.4049/jimmunol.178.12.7868.
- ↑ Blair PA, Noreña LY, Flores-Borja F, Rawlings DJ, Isenberg DA, Ehrenstein MR, Mauri C (January 2010). CD19(+)CD24(hi)CD38(hi) B cells exhibit regulatory capacity in healthy individuals but are functionally impaired in systemic Lupus Erythematosus patients. Immunity 32 (1): 129–40. PMID 20079667. DOI: 10.1016/j.immuni.2009.11.009.
- ↑ Iwata Y, Matsushita T, Horikawa M, Dilillo DJ, Yanaba K, Venturi GM, Szabolcs PM, Bernstein SH, Magro CM, Williams AD, Hall RP, St Clair EW, Tedder TF (January 2011). Characterization of a rare IL-10-competent B-cell subset in humans that parallels mouse regulatory B10 cells. Blood 117 (2): 530–41. PMID 20962324. PMC 3031478. DOI: 10.1182/blood-2010-07-294249.
- ↑ van de Veen W, Stanic B, Yaman G, Wawrzyniak M, Söllner S, Akdis DG, Rückert B, Akdis CA, Akdis M (April 2013). IgG4 production is confined to human IL-10-producing regulatory B cells that suppress antigen-specific immune responses. The Journal of Allergy and Clinical Immunology 131 (4): 1204–12. PMID 23453135. DOI: 10.1016/j.jaci.2013.01.014.
- 1 2 (en) Ben Nasr, Moufida, Usuelli, Vera, Seelam, Andy Joe, D'Addio, Francesca, Abdi, Reza (15 March 2021). Regulatory B Cells in Autoimmune Diabetes. Journal of Immunology 206 (6): 1117-1125. ISSN: 1550-6606. PMID 33685919. DOI: 10.4049/jimmunol.2001127. Gearchiveerd op 2 februari 2023. Geraadpleegd op 22 August 2023.
- 1 2 Berthelot JM, Jamin C, Amrouche K, Le Goff B, Maugars Y, Youinou P (January 2013). Regulatory B cells play a key role in immune system balance. Joint, Bone, Spine 80 (1): 18–22. PMID 22858147. DOI: 10.1016/j.jbspin.2012.04.010.
- ↑ Asseman C, Mauze S, Leach MW, Coffman RL, Powrie F (October 1999). An essential role for interleukin 10 in the function of regulatory T cells that inhibit intestinal inflammation. The Journal of Experimental Medicine 190 (7): 995–1004. PMID 10510089. PMC 2195650. DOI: 10.1084/jem.190.7.995.
- ↑ Fillatreau S, Sweenie CH, McGeachy MJ, Gray D, Anderton SM (October 2002). B cells regulate autoimmunity by provision of IL-10. Nature Immunology 3 (10): 944–50. PMID 12244307. DOI: 10.1038/ni833.
- ↑ Mauri C, Gray D, Mushtaq N, Londei M (February 2003). Prevention of arthritis by interleukin 10-producing B cells. The Journal of Experimental Medicine 197 (4): 489–501. PMID 12591906. PMC 2193864. DOI: 10.1084/jem.20021293.
- ↑ Yanaba K, Bouaziz JD, Haas KM, Poe JC, Fujimoto M, Tedder TF (May 2008). A regulatory B cell subset with a unique CD1dhiCD5+ phenotype controls T cell-dependent inflammatory responses. Immunity 28 (5): 639–50. PMID 18482568. DOI: 10.1016/j.immuni.2008.03.017.
- ↑ Schaut RG, Lamb IM, Toepp AJ, Scott B, Mendes-Aguiar CO, Coutinho JF, Jeronimo SM, Wilson ME, Harty JT, Waldschmidt TJ, Petersen CA (May 2016). Regulatory IgDhi B Cells Suppress T Cell Function via IL-10 and PD-L1 during Progressive Visceral Leishmaniasis. Journal of Immunology 196 (10): 4100–9. PMID 27076677. PMC 4868652. DOI: 10.4049/jimmunol.1502678.
- 1 2 Douglas RS, Woo EY, Capocasale RJ, Tarshis AD, Nowell PC, Moore JS (August 1997). Altered response to and production of TGF-beta by B cells from autoimmune NZB mice. Cellular Immunology 179 (2): 126–37. PMID 9268496. DOI: 10.1006/cimm.1997.1149.
- ↑ Tian J, Zekzer D, Hanssen L, Lu Y, Olcott A, Kaufman DL (July 2001). Lipopolysaccharide-activated B cells down-regulate Th1 immunity and prevent autoimmune diabetes in nonobese diabetic mice. Journal of Immunology 167 (2): 1081–9. PMID 11441119. DOI: 10.4049/jimmunol.167.2.1081.
- ↑ Lundy SK, Boros DL (February 2002). Fas ligand-expressing B-1a lymphocytes mediate CD4(+)-T-cell apoptosis during schistosomal infection: induction by interleukin 4 (IL-4) and IL-10. Infection and Immunity 70 (2): 812–9. PMID 11796615. PMC 127725. DOI: 10.1128/iai.70.2.812-819.2002.
- ↑ Zheremyan, EA, Ustiugova, AS, Uvarova, AN, Karamushka, NM, Stasevich, EM (2023). Differentially activated B cells develop regulatory phenotype and show varying immunosuppressive features: a comparative study.. Frontiers in Immunology 14. PMID 37731503. PMC 10509016. DOI: 10.3389/fimmu.2023.1178445.
- ↑ Zheremyan, EA, Kon, NR, Ustiugova, AS, Stasevich, EM, Bogomolova, EA (2025). The half-century odyssey of regulatory B cells: from Breg discovery to emerging frontiers.. Frontiers in Immunology 16. PMID 41080554. PMC 12507930. DOI: 10.3389/fimmu.2025.1681082.
- ↑ Morris, Alan, Möller, Göran (1 september 1968). Regulation of Cellular Antibody Synthesis. The Journal of Immunology 101 (3): 439–445. DOI: 10.4049/jimmunol.101.3.439.
- ↑ Katz SI, Parker D, Turk JL (October 1974). B-cell suppression of delayed hypersensitivity reactions. Nature 251 (5475): 550–1. PMID 4547522. DOI: 10.1038/251550a0.
- ↑ Wolf SD, Dittel BN, Hardardottir F, Janeway CA (December 1996). Experimental autoimmune encephalomyelitis induction in genetically B cell-deficient mice. The Journal of Experimental Medicine 184 (6): 2271–8. PMID 8976182. PMC 2196394. DOI: 10.1084/jem.184.6.2271.
- ↑ Mizoguchi A, Mizoguchi E, Smith RN, Preffer FI, Bhan AK (November 1997). Suppressive role of B cells in chronic colitis of T cell receptor alpha mutant mice. The Journal of Experimental Medicine 186 (10): 1749–56. PMID 9362534. PMC 2199135. DOI: 10.1084/jem.186.10.1749.
- ↑ Korganow AS, Ji H, Mangialaio S, Duchatelle V, Pelanda R, Martin T, Degott C, Kikutani H, Rajewsky K, Pasquali JL, Benoist C, Mathis D (April 1999). From systemic T cell self-reactivity to organ-specific autoimmune disease via immunoglobulins. Immunity 10 (4): 451–61. PMID 10229188. DOI: 10.1016/s1074-7613(00)80045-x.
- 1 2 3 (en) Michaud, Daniel, Steward, Colleen R., Mirlekar, Bhalchandra, Pylayeva-Gupta, Yuliya (January 2021). Regulatory B cells in cancer. Immunological Reviews 299 (1): 74–92. ISSN: 0105-2896. PMID 33368346. PMC 7965344. DOI: 10.1111/imr.12939.
- ↑ Wang X, Yuling H, Yanping J, Xinti T, Yaofang Y, Feng Y, Ruijin X, Li W, Lang C, Jingyi L, Zhiqing T, Jingping O, Bing X, Li Q, Chang AE, Sun Z, Youxin J, Jinquan T (September 2007). CCL19 and CXCL13 synergistically regulate interaction between B cell acute lymphocytic leukemia CD23+CD5+ B Cells and CD8+ T cells. Journal of Immunology 179 (5): 2880–8. PMID 17709502. DOI: 10.4049/jimmunol.179.5.2880.
- ↑ Shang J, Zha H and Sun Y (2020) Phenotypes, Functions, and Clinical Relevance of Regulatory B Cells in Cancer. Front. Immunol. 11:582657. doi: 10.3389/fimmu.2020.582657