Folliculaire helper-T-cel
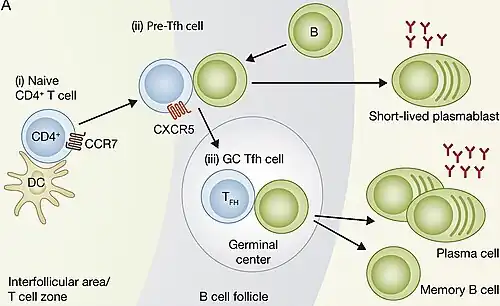

Folliculaire helper-T-cellen (ook bekend als T-folliculaire helpercellen en afgekort als TFH (Engels: T follicular helper cells)) zijn T-helpercel die in contazt zijn geweest met antigenen en die zich in de periferie bevinden in B-cel follikels van secundaire lymfoïde organen zoals lymfeklieren, milt en Peyerse platen, en worden geïdentificeerd door hun genexpressie van CXCR5.[1] Na cellulaire interactie en kruissignalering met hun verwante folliculaire (Fo B) B-cellen, triggeren TFH-cellen de vorming en het onderhoud van kiemcentra (door sterke celdeling gekenmerkt centrum van de lymfefollikel, waar de centroblasten en centrocyten in contact worden gebracht met antigenen) door de expressie van CD40-ligand (CD40L) en de secretie van IL-21[2] en IL-4.[3] TFH-cellen migreren ook vanuit T-celzones naar deze kiemcentra, die voornamelijk bestaan uit snel delende B-cellen die hun Ig-genen muteren. Binnen de kiemcentra spelen TFH-cellen een cruciale rol bij de selectie en overleving van B-cellen die zich differentiëren tot ofwel langlevende plasmacellen die in staat zijn antilichamen met een hoge affiniteit tegen vreemde antigenen te produceren, ofwel kiemcentrumafhankelijke geheugen-B-cellen die in staat zijn tot snelle immuunreactivering in de toekomst als hetzelfde antigeen opnieuw wordt aangetroffen.[4] Er wordt ook gedacht dat TFH-cellen de negatieve selectie van potentieel auto-immuun-veroorzakende gemuteerde B-cellen in het kiemcentrum faciliteren. De biomechanismen waarmee TFH-cellen tolerantie in het kiemcentrum bewerkstelligen, zijn echter nog niet volledig begrepen.
Het is mogelijk dat TFH-cellen ontstaan als vertakkingen in de Th1- en Th2-differentiatiepaden, maar hun precieze verwantschap met de andere effector-T-helpercelsubtypen is nog onduidelijk. Uit onderzoek is echter gebleken dat TFH een eigen genexpressieprofiel hebben, wat de theorie ondersteunt dat TFH een subgroep van T-helpercellen vormen die verschillen van Th1-cellen, Th2-cellen, Th17-cellen of regulatoire T-cellen.[5][6]
Na interactie met B-cellen nemen folliculaire helper T-cellen hun meest gepolariseerde vorm aan en betreden ze de kiemcentra.[7][8] Dit proces omvat een verminderde expressie van EBI2 en een verhoogde expressie van S1PR2, waardoor folliculaire helper-T-cellen in het centrum van de follikels kunnen worden vastgehouden.[8][9] Binnen de kiemcentra zijn folliculaire helper-T-cellen zeer beweeglijk en verkennen ze actief antigeenpresenterende B-cellen. Het PD-L1-eiwit dat door folliculaire mantel-B-cellen wordt geproduceerd, voorkomt dat folliculaire helper-T-cellen naar de periferie ontsnappen, wat de rol van PD-1 bij het vasthouden van folliculaire helper-T-cellen in het kiemcentrum benadrukt.[10]
Biomoleculaire karakterisering
Het is bewezen dat de induceerbare T-cel co-stimulator (CD278 of ICOS) een bijzonder cruciaal signaal levert voor TFH-cellen, aangezien experimentele muizen met een ICOS-deficiëntie geen TFH kunnen ontwikkelen.[11] Bovendien is aangetoond dat ICOS de secretie van het cytokine IL-21 door geactiveerde T-helpercellen induceert en dat IL-21 een cruciale rol speelt in de ontwikkeling van TFH-cellen en kiemcentra.[12][13] Ook Bcl-6 is een transcriptiefactor die in TFH-cellen is geïdentificeerd, maar de rol ervan reikt mogelijk verder dan deze subgroep, omdat het ook betrokken is bij de ontwikkeling van geheugen-cytotoxische T-cellen.[14]
In kiemcentra verhogen TFH-cellen die in contact zijn geweest met antigenen snel de expressie van CD40L, dat bindt aan en de B-celoppervlakreceptor CD40 stimuleert.[15] TFH-celafhankelijke paracriene activering van B-cel-CD40 resulteert in overleving en differentiatie van B-cellen, inclusief de inductie van AID.[16] AID-expressie (gecodeerd door het AICDA-gen) zorgt ervoor dat B-cel-antilichamen van klasse wisselen van IgM/IgD naar andere antilichaamisotypen en drijft somatische hypermutatie aan tijdens klonale proliferatie. De gewisselde antilichamen verkrijgen betere effectorfuncties en hypergemuteerde antilichamen vertonen een grotere affiniteit voor antigenen.
Klassen van TFH-cellen
TFH-cellen die vroeg in de beginfase van een kiemcentrumreactie worden gevormd, worden formeel pre-TFH-cellen genoemd. Ze bevinden zich voornamelijk aan de rand van de T-celzone die overgaat in de B-celfollikels en kiemcentra. Pre-TFH-cellen lijken functioneel sterk op andere TFH-cellen in het faciliteren van B-celreacties in het kiemcentrum; ze zijn echter ook in staat de ontwikkeling van folliculaire B-cellen aan te sturen, zowel naast als buiten de kiemcentra, om snel reagerende maar niet-duurzame, door plasmacellen gedreven antilichaamreacties te produceren (bekend als de extrafolliculaire respons).
Die TFH-cellen die zich specifiek in een volwassen kiemcentrum bevinden, worden soms GC TFH-cellen genoemd (voor germinal center TFH cells) om ze te onderscheiden van pre-TFH-cellen.[17][18] Er is ook een kleine subklasse binnen deze populatie GC TFH-cellen die het gen Foxp3 tot expressie brengen, dat codeert voor een transcriptiefactor. Deze kleine, afzonderlijke subpopulatie van cellen, TFR-cellen (T-folliculaire regulatoire cellen genoemd. T-folliculaire regulatoire cellen zijn een herkenbare populatie van regulatoire T-cellen die migreren naar de B-cel follikel en het kiemcentrum na een immuunuitdaging), is belangrijk voor het beheersen en beperken van de omvang van normale reacties in het kiemcentrum, zodat ze de potentiële productie van abnormaal gemuteerde of zelfreactieve auto-immuun-geassocieerde antilichamen vermijden.[19] Daarom hebben TFR-cellen een unieke remmende invloed tijdens een reactie in het kiemcentrum.
Hoewel TFH-cellen voornamelijk in de secundaire lymfoïde organen voorkomen, circuleert een klein deel ervan in het bloed en worden ze "perifere" T-folliculaire helpercellen (pTFH) genoemd. Deze cellen kunnen worden geïdentificeerd aan de hand van hun expressie van IL-21 na stimulatie.[20]
Klinische betekenis
Het genereren van een blijvend immuungeheugen
TFH-cellen worden beschouwd als een onmisbare subgroep van T-cellen bij de generatie en het behoud van kiemcentrumreacties. Daarom wordt, bij afwezigheid van TFH-cellen, net als bij B-celactivering door T-celonafhankelijke antigenen, een snelle piek in de productie van plasmacellen met lage affiniteit gevormd. Dit leidt echter niet tot inductie van kiemcentra, noch tot rijping van de antilichaamaffiniteit of de differentiatie van effectieve B-geheugencellen, die essentieel zijn voor het versterken van het lichaam tegen latere infecties. Specifiek zijn kiemcentrumafhankelijke B-geheugencellen de drijvende kracht achter de productie van geheugen-antilichamen tijdens een secundaire immuunrespons. Daarom is de juiste activering en ontwikkeling van TFH-cellen cruciaal voor de effectiviteit van immunisering en het ontwerp van vaccins voor het induceren van langdurige immuniteit. In een onderzoek onder de Bengalese bevolking met patiënten die geïnfecteerd waren met Vibrio cholerae en gezonde vrijwilligers die een bestaand choleravaccin kregen toegediend,[20] bleek een geheugen-TFH-respons specifiek tegen cholera-antigeen gecorreleerd te zijn met verdere antilichaamproductie door B-cellen.
Het beheersen van leeftijdsgebonden immuunafname
Met het normale verouderingsproces neemt het immuunsysteem van het lichaam geleidelijk af. Dit fenomeen, immunosenescentie genoemd, is grotendeels te wijten aan een afname van de T-celfunctie, inclusief het vermogen van TFH-cellen om de kiemcentrumreacties adequaat te ondersteunen.[21] Dit kan gedeeltelijk te wijten zijn aan lagere CD40L-niveaus op het celoppervlak van TFH-cellen bij ouderen.[22]
Het voorkomen van auto-immuniteit
Ongecontroleerde of overactieve immuunreacties van TFH-cellen kunnen leiden tot ongewenste kiemcentra, bestaande uit abnormaal gemuteerde B-cellen die antilichaamgemedieerde auto-immuunziekten kunnen veroorzaken. Verhoogde niveaus van TFH-achtige cellen kunnen worden gedetecteerd in het bloed van een subset van menselijke patiënten met systemische lupus erythematodes (SLE) en het syndroom van Sjögren.[23] Het wetenschappelijk bewijs dat TFH-cellen definitief auto-immuniteit bij mensen kunnen veroorzaken, is echter nog niet volledig.
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Follicular helper T cells op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
Referenties
- ↑ Fazilleau (March 2009). Follicular helper T cells: lineage and location. Immunity 30 (3): 324–35. PMID 19303387. PMC 2731675. DOI: 10.1016/j.immuni.2009.03.003.
- ↑ Seo (May 2009). IL-21 ensures TGF-beta 1-induced IgA isotype expression in mouse Peyer's patches. J Leukoc Biol 85 (5): 744–50. PMID 19168593. DOI: 10.1189/jlb.0708450.
- ↑ Zaretsky (May 2009). T follicular helper cells differentiate from Th2 cells in response to helminth antigens. J Exp Med 206 (5): 991–9. PMID 19380637. PMC 2715032. DOI: 10.1084/jem.20090303.
- ↑ Kurosaki (March 2015). Memory B cells. Nat Rev Immunol 15 (3): 149–59. PMID 25677494. DOI: 10.1038/nri3802.
- ↑ Chtanova (July 2004). T follicular helper cells express a distinctive transcriptional profile, reflecting their role as non-Th1/Th2 effector cells that provide help for B cells. J Immunol 173 (1): 68–78. PMID 15210760. DOI: 10.4049/jimmunol.173.1.68.
- ↑ Nurieva RI, Chung Y, Hwang D, Yang XO, Kang HS, Ma L, Wang YH, Watowich SS, Jetten AM, Tian Q, Dong C (2008). Generation of T follicular helper cells is mediated by interleukin-21 but independent of T helper 1, 2, or 17 cell lineages. Immunity 29 (1): 138–49. PMID 18599325. PMC 2556461. DOI: 10.1016/j.immuni.2008.05.009.
- ↑ Ziv Shulman, Alexander D. Gitlin, Sasha Targ et Mila Jankovic, « T Follicular Helper Cell Dynamics in Germinal Centers », Science, vol. 341, no 6146, 9 août 2013, p. 673–677 (ISSN 0036-8075 et 1095-9203, PMID 23887872, PMCID 3941467, DOI 10.1126/science.1241680, lire en ligne [archive], consulté le 6 décembre 2025
- 1 2 Dan Suan, Akira Nguyen, Imogen Moran et Katherine Bourne, « T Follicular Helper Cells Have Distinct Modes of Migration and Molecular Signatures in Naive and Memory Immune Responses », Immunity, vol. 42, no 4, avril 2015, p. 704–718 (DOI 10.1016/j.immuni.2015.03.002, lire en ligne [archive], consulté le 6 décembre 2025)
- ↑ Saya Moriyama, Noriko Takahashi, Jesse A. Green et Shohei Hori, « Sphingosine-1-phosphate receptor 2 is critical for follicular helper T cell retention in germinal centers », Journal of Experimental Medicine, vol. 211, no 7, 30 juin 2014, p. 1297–1305 (ISSN 1540-9538 et 0022-1007, PMID 24913235, PMCID 4076581, DOI 10.1084/jem.20131666, lire en ligne [archive], consulté le 6 décembre 2025)
- ↑ Jingwen Shi, Shiyue Hou, Qian Fang et Xin Liu, « PD-1 Controls Follicular T Helper Cell Positioning and Function », Immunity, vol. 49, no 2, août 2018, p. 264–274.e4 (PMID 30076099, PMCID 6104813, DOI 10.1016/j.immuni.2018.06.012, lire en ligne [archive], consulté le 6 décembre 2025)
- ↑ Akiba (Aug 2005). The role of ICOS in the CXCR5+ follicular B helper T cell maintenance in vivo. J Immunol 175 (4): 2340–8. PMID 16081804. DOI: 10.4049/jimmunol.175.4.2340.
- ↑ Bauquet (Feb 2009). The costimulatory molecule ICOS regulates the expression of c-Maf and IL-21 in the development of follicular T helper cells and TH-17 cells. Nat Immunol 10 (2): 167–75. PMID 19098919. PMC 2742982. DOI: 10.1038/ni.1690.
- ↑ Vogelzang (July 2008). A fundamental role for interleukin-21 in the generation of T follicular helper cells. Immunity 29 (1): 127–37. PMID 18602282. DOI: 10.1016/j.immuni.2008.06.001.
- ↑ Ichii (June 2002). Role for Bcl-6 in the generation and maintenance of memory CD8+ T cells. Nat Immunol 3 (6): 558–63. PMID 12021781. DOI: 10.1038/ni802.
- ↑ Kim, JR, Lim, HW, Kang, SG (4 februari 2005). Human CD57+ germinal center-T cells are the major helpers for GC-B cells and induce class switch recombination.. BMC Immunology 6: 3. PMID 15694005. PMC 548684. DOI: 10.1186/1471-2172-6-3.
- ↑ McHeyzer-Williams, M, Okitsu, S, Wang, N (9 december 2011). Molecular programming of B cell memory.. Nature Reviews. Immunology 12 (1): 24–34. PMID 22158414. PMC 3947622. DOI: 10.1038/nri3128.
- ↑ Yusuf I, Kageyama R, Monticelli L, Johnston RJ, Ditoro D, Hansen K, Barnett B, Crotty S (July 2010). Germinal center T follicular helper cell IL-4 production is dependent on signaling lymphocytic activation molecule receptor (CD150).. J. Immunol. 185 (1): 190–202. PMID 20525889. PMC 2913439. DOI: 10.4049/jimmunol.0903505.
- ↑ Ramiscal RR, Vinuesa CG (March 2013). T-cell subsets in the germinal center.. Immunol. Rev. 252 (1): 146–55. PMID 23405902. DOI: 10.1111/imr.12031.
- ↑ Wollenberg I, Agua-Doce A, Hernández A, Almeida C, Oliveira VG, Faro J, Graca L (November 2011). Regulation of the germinal center reaction by Foxp3+ follicular regulatory T cells.. J. Immunol. 187 (9): 4553–60. PMID 21984700. DOI: 10.4049/jimmunol.1101328.
- 1 2 Schultz, Bruce T., Teigler, Jeffrey E., Pissani, Franco, Oster, Alexander F., Kranias, Gregory (19 januari 2016). Circulating HIV-Specific Interleukin-21(+)CD4(+) T Cells Represent Peripheral Tfh Cells with Antigen-Dependent Helper Functions. Immunity 44 (1): 167–178. ISSN: 1097-4180. PMID 26795249. DOI: 10.1016/j.immuni.2015.12.011.
- ↑ Lefebvre JS, Maue AC, Eaton SM, Lanthier PA, Tighe M, Haynes L (2012). The aged microenvironment contributes to the age-related functional defects of CD4 T cells in mice.. Aging Cell 11 (5): 732–40. PMID 22607653. PMC 3444657. DOI: 10.1111/j.1474-9726.2012.00836.x.
- ↑ Perkey E, Miller RA, Garcia GG (2012). Ex vivo enzymatic treatment of aged CD4 T cells restores cognate T cell helper function and enhances antibody production in mice.. J Immunol 189 (12): 5582–9. PMID 23136198. PMC 3518580. DOI: 10.4049/jimmunol.1200487.
- ↑ Craft JE. (2012). Follicular helper T cells in immunity and systemic autoimmunity.. Nat Rev Rheumatol 8 (6): 337–47. PMID 22549246. PMC 3604997. DOI: 10.1038/nrrheum.2012.58.