Basale cel
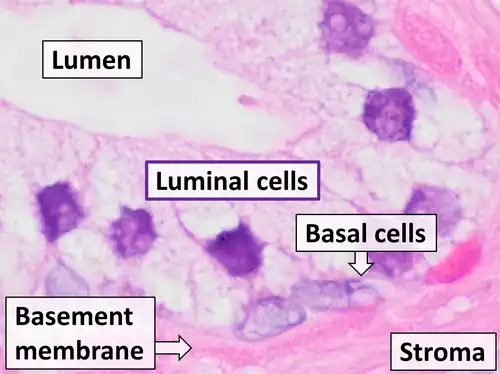

Een basale cel is een stamcel die aanwezig is in vele vormen van epitheelweefsel in het lichaam. Basale cellen bevinden zich tussen het basaal membraan en de rest van het epitheel en functioneren effectief als anker voor de epitheellaag en als een belangrijk mechanisme bij het handhaven van de homeostase binnen organen.
Basale cellen kunnen interageren met omliggende cellen, waaronder zenuwcellen, het basaal membraan, cilindrisch epitheel en onderliggende mesenchymale stamcellen. Ze gaan ook interacties aan met dendritische cellen, lymfocyten en andere witte bloedcellen, waarbij de meeste van deze interacties plaatsvinden in de laterale intercellulaire ruimte tussen basale cellen.[1]
Basale cellen hebben een belangrijke rol in de gezondheid, aangezien de meest voorkomende vormen van huidkanker basocellulair carcinoom en plaveiselcelcarcinoom zijn. In de Verenigde Staten worden jaarlijks meer dan 1 miljoen gevallen van deze kankers, ook wel niet-melanoom huidkankers (NMSC) genoemd, gediagnosticeerd en de incidentie neemt snel toe. In Nederland krijgt 1 op de 5 mensen een basaalcelcarcinoom en 1 op de 15 mensen krijgt een plaveiselcelcarcinoom van de huid.[2]
Basale en plaveiselcelkankers kunnen, hoewel ze zelden metastatisch zijn, aanzienlijke lokale schade en misvorming veroorzaken, waarbij grote delen van de weke delen, het kraakbeen en het bot worden aangetast.[3]
Structuur

Ongeacht hun specifieke locatie hebben basale cellen over het algemeen een vergelijkbare basisstructuur. Het zijn meestal allemaal kubusvormige, polyhedrale of piramidevormige cellen met vergrote kernen en minimaal cytoplasma.[4] Basale cellen zijn aan elkaar verbonden door desmosomen en aan de basale lamina van het basaal membraan door hemidesmosomen. Deze verbindingen helpen om één strak verbonden, ononderbroken weefsellaag te creëren die mechanische spanning kan weerstaan en effectief functioneert als een verbinding tussen het basaal membraan en het resterende epitheelweefsel.[5]
Functie
Basale cellen vervullen twee hoofdfuncties in cellen. Ze dienen:
- Het verankeren en verbinden van het epitheel met het basaalmembraan.
- Als de belangrijkste stamcelpopulatie voor het weefsel waarin ze zich bevinden, reageren ze op stimuli om de homeostase in dat weefsel te handhaven.
Hoewel alle basale cellen, ongeacht hun locatie, een vergelijkbare functie hebben wat betreft het verankeren van het epitheel, variëren de specifieke functie en mechanismen van basale cellen als stamcellen per locatie. Over het algemeen kunnen basale cellen functioneren als unipotente of multipotente stamcellen.
Epidermale basale cellen of huidstamcellen
Huidstamcellen, epidermale stamcellen of epidermale basale cellen zijn pluripotente stamcellen in de huid en zorgen voor vernieuwing van de huid en het herstel na beschadiging. De continue deling van epidermale basale cellen leidt tot een volledige epidermale turnover elke 40-56 dagen bij mensen en elke 8-10 dagen bij muizen.[6]
Luchtwegbasale cellen of longstamcellen
In de luchtwegen functioneren basale cellen als multipotente longstamcellen, die in staat zijn alle epitheelceltypen aan te vullen, inclusief secretoire, trilhaar- en intermediaire cellen. Ze bevinden zich in de slijmlaag van het ademhalingsepitheel en blijven over het algemeen inactief. Wanneer een functionele epitheelcel echter beschadigd raakt, wordt een longstamcel geactiveerd om via longbasale cellen te differentiëren tot het juiste celtype en de beschadigde cel te vervangen.[7][8]
Basale cellen van het maag-darmstelsel
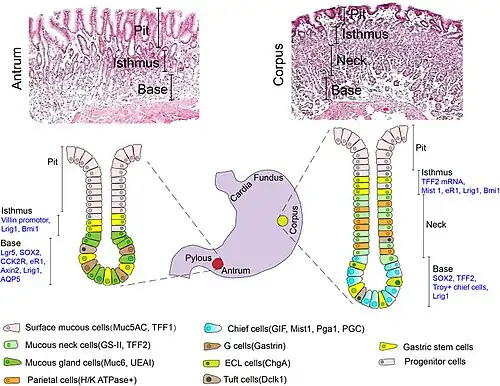
Het maag-darmstelsel bestaat uit de slokdarm, maag, dunne darm en dikke darm, en elke laag is bekleed met een apart maar vergelijkbaar epitheel dat noodzakelijkerwijs basale cellen bevat. Hoewel de algemene functie van deze basale cellen in het hele stelsel vergelijkbaar is, kunnen de specifieke mechanismen, functies en producten van deze cellen variëren, afhankelijk van de laag waarin de cellen zich bevinden. Zo functioneren basale cellen in zowel de slokdarm als de maag als multipotente voorlopercellen, maar zijn ze fundamenteel verschillend omdat de basale cellen van de slokdarm deel uitmaken van een meerlagig plaveiselepitheel, terwijl de basale cellen van de maag deel uitmaken van een enkelvoudig cilindrisch epitheel. Functioneel betekent dit dat, aangezien een enkelvoudig epitheel slechts één cel dik is, gedifferentieerde cellen langs het vlak van het basaal membraan moeten diffunderen in plaats van verticaal door de rest van het epitheel. Bovendien variëren de werkelijke producten van deze cellen aanzienlijk, aangezien de basale cellen van de slokdarm voornamelijk plaveiselepitheelcellen produceren, die functioneren als een passieve fysieke barrière tussen het lumen van de slokdarm en de onderliggende weefsels, terwijl de basale cellen van de maag zich differentiëren tot een verscheidenheid aan secretoire en absorberende cellen die de belangrijkste functies van de maag verzorgen, waaronder enterocyten, maaghoofdcellen en pariëtale cellen.[9]
Maag
In de maag bevinden basale cellen zich over het algemeen in de istmus, of nabij de bovenkant, van de maagklieren. Deze locatie maakt het mogelijk dat ze zich gemakkelijk binnen de klier kunnen differentiëren en vervolgens bidirectioneel kunnen diffunderen terwijl ze differentiëren, waarbij ze ofwel naar de maagholte erboven ofwel naar de basis van de maagklier gaan om beschadigde cellen aan te vullen. Door de barre omgeving die wordt gecreëerd door het zure binnenste van de maag, vermeerderen de basale cellen zich continu, waarbij ze vertrouwen op een verscheidenheid aan routes en signaalmoleculen om te communiceren welk type cellen beschadigd is en vervangen moet worden. Deze regulatoren van proliferatie en differentiatie omvatten het eiwit Sox9, de Wnt- en Notch-signaalroutes, BMP's 2, 4 en 7 (die allemaal kunnen functioneren als tumorsuppressoren en EGF.[10][11][12][13] Deze processen bevinden zich in een delicate toestand en eventuele fouten in of verstoringen van deze routes kunnen diverse aandoeningen veroorzaken. Een infectie met Helicobacter pylori kan bijvoorbeeld een overexpressie van EGF veroorzaken, wat leidt tot overmatige differentiatie van basale cellen tot gastrinecellen, wat op zijn beurt kan leiden tot atrofische gastritis, een goed bestudeerde voorloper van maagkanker.[14] Bovendien kan mutatie of verwijdering van de genen die coderen voor Jag1 of Jag2 leiden tot een verstoring van de cruciale Notch-signaalroute, wat op zijn beurt kan leiden tot ongecontroleerde en ongereguleerde groei en differentiatie, wat leidt tot tumorvorming.[15]
Darm
_Differentiation_of_Paneth_cells.jpg)
Net als basale cellen in de maag, vermeerderen basale cellen in de darm zich continu. Sterker nog, vanwege de cruciale rol die de dunne darm speelt bij de opname van voedingsstoffen, vertonen basale cellen in de dunne darm de hoogste turnoversnelheid van alle cellen in het lichaam, waarbij ongeveer elke 5-7 dagen een geheel nieuw epitheel wordt gevormd.[16][17] In de darmen bevinden basale cellen zich aan de basis van darminstulpingen, bekend als crypten, waar ze gevoed en beschermd worden door pariëtale cellen en de omliggende micro-omgeving. Deze basale cellen functioneren vervolgens als multipotente voorlopercellen, die in staat zijn tot differentiatie in zes verschillende celtypen, gereguleerd door mechanismen die sterk lijken op die in andere maag-darm basale cellen.[18] Naarmate de cellen differentiëren, migreren ze vanuit de crypte naar het lumen, totdat ze uiteindelijk afsterven en in het darmlumen worden vrijgelaten, om al snel vervangen te worden door een nieuwe cel.
Zie ook
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Basal cell op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- ↑ (en) What Are Basal and Squamous Cell Skin Cancers? | Types of Skin Cancer. www.cancer.org. Geraadpleegd op 27 maart 2024.
- ↑ kanker.nl, Stichting, Huidkanker | Kanker.nl. www.kanker.nl. Geraadpleegd op 17 oktober 2025.
- ↑ (en) Miller, Stanley J., Alam, Murad, Andersen, James, Berg, Daniel, Bichakjian, Christopher K. (August 2010). Basal Cell and Squamous Cell Skin Cancers. Journal of the National Comprehensive Cancer Network 8 (8): 836–864. ISSN: 1540-1405. PMID 20870631. DOI: 10.6004/jnccn.2010.0062.
- ↑ Haschek, Wanda M., Witschi, Hanspeter R., Nikula, Kristen J. (1 januari 2002). 28 - Respiratory System. Academic Press, San Diego. DOI:10.1016/b978-012330215-1/50029-6, 3–83. ISBN 978-0-12-330215-1. Geraadpleegd op 26 november 2024.
- ↑ Cote, Lauren E., Feldman, Jessica L. (21 juni 2022). Won't You be My Neighbor: How Epithelial Cells Connect Together to Build Global Tissue Polarity. Frontiers in Cell and Developmental Biology 10. ISSN: 2296-634X. PMID 35800889. PMC 9253303. DOI: 10.3389/fcell.2022.887107.
- ↑ (en) Koster, Maranke I. (July 2009). Making an Epidermis. Annals of the New York Academy of Sciences 1170 (1): 7–10. ISSN: 0077-8923. PMID 19686098. PMC 2861991. DOI: 10.1111/j.1749-6632.2009.04363.x.
- ↑ Hong, Kyung U., Reynolds, Susan D., Watkins, Simon, Fuchs, Elaine, Stripp, Barry R. (April 2004). In vivo differentiation potential of tracheal basal cells: evidence for multipotent and unipotent subpopulations. American Journal of Physiology. Lung Cellular and Molecular Physiology 286 (4): L643–L649. ISSN: 1040-0605. PMID 12871857. DOI: 10.1152/ajplung.00155.2003.
- ↑ (en) Hong, Kyung U., Reynolds, Susan D., Watkins, Simon, Fuchs, Elaine, Stripp, Barry R. (February 2004). Basal Cells Are a Multipotent Progenitor Capable of Renewing the Bronchial Epithelium. The American Journal of Pathology 164 (2): 577–588. PMID 14742263. PMC 1602270. DOI: 10.1016/S0002-9440(10)63147-1.
- ↑ (en) Hayakawa, Yoku, Nakagawa, Hiroshi, Rustgi, Anil K., Que, Jianwen, Wang, Timothy C. (5 augustus 2021). Stem cells and origins of cancer in the upper gastrointestinal tract. Cell Stem Cell 28 (8): 1343–1361. ISSN: 1934-5909. PMID 34129814. PMC 8844710. DOI: 10.1016/j.stem.2021.05.012.
- ↑ (en) Willet, Spencer G., Thanintorn, Nattapon, McNeill, Helen, Huh, Sung-Ho, Ornitz, David M. (2023). SOX9 Governs Gastric Mucous Neck Cell Identity and Is Required for Injury-Induced Metaplasia. Cellular and Molecular Gastroenterology and Hepatology 16 (3): 325–339. PMID 37270061. PMC 10444955. DOI: 10.1016/j.jcmgh.2023.05.009.
- ↑ (en) Kapalczynska, Marta, Lin, Manqiang, Maertzdorf, Jeroen, Heuberger, Julian, Muellerke, Stefanie (24 maart 2022). BMP feed-forward loop promotes terminal differentiation in gastric glands and is interrupted by H. pylori-driven inflammation. Nature Communications 13 (1). ISSN: 2041-1723. PMID 35332152. PMC 8948225. DOI: 10.1038/s41467-022-29176-w.
- ↑ Wölffling, Sarah, Daddi, Alice Anna, Imai-Matsushima, Aki, Fritsche, Kristin, Goosmann, Christian (August 2021). EGF and BMPs Govern Differentiation and Patterning in Human Gastric Glands. Gastroenterology 161 (2): 623–636.e16. ISSN: 0016-5085. PMID 33957136. DOI: 10.1053/j.gastro.2021.04.062.
- ↑ (en) Shirai, Yo-taro, Ehata, Shogo, Yashiro, Masakazu, Yanagihara, Kazuyoshi, Hirakawa, Kosei (December 2011). Bone Morphogenetic Protein-2 and -4 Play Tumor Suppressive Roles in Human Diffuse-Type Gastric Carcinoma. The American Journal of Pathology 179 (6): 2920–2930. PMID 21996676. PMC 3260801. DOI: 10.1016/j.ajpath.2011.08.022.
- ↑ (en) Uemura, Naomi, Okamoto, Shiro, Yamamoto, Soichiro, Matsumura, Nobutoshi, Yamaguchi, Shuji (13 september 2001). Helicobacter pylori Infection and the Development of Gastric Cancer. New England Journal of Medicine 345 (11): 784–789. ISSN: 0028-4793. PMID 11556297. DOI: 10.1056/NEJMoa001999.
- ↑ (en) Huang, Haidi, Jiang, Yu, Liu, Jiangying, Luo, Dan, Yuan, Jianghong (15 mei 2024). Jag1/2 maintain esophageal homeostasis and suppress foregut tumorigenesis by restricting the basal progenitor cell pool. Nature Communications 15 (1): 4124. ISSN: 2041-1723. PMID 38750026. PMC 11096375. DOI: 10.1038/s41467-024-48347-5.
- ↑ (en) van der Flier, Laurens G., Clevers, Hans (1 maart 2009). Stem Cells, Self-Renewal, and Differentiation in the Intestinal Epithelium. Annual Review of Physiology 71 (1): 241–260. ISSN: 0066-4278. PMID 18808327. DOI: 10.1146/annurev.physiol.010908.163145.
- ↑ (en) Understanding how the intestine replaces and repairs itself. hsci.harvard.edu. Geraadpleegd op 6 december 2024.
- ↑ (en) Gehart, Helmuth, Clevers, Hans (January 2019). Tales from the crypt: new insights into intestinal stem cells. Nature Reviews Gastroenterology & Hepatology 16 (1): 19–34. ISSN: 1759-5053. PMID 30429586. DOI: 10.1038/s41575-018-0081-y.