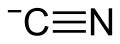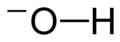Polyatomisch ion
Een polyatomisch ion (poly is Grieks voor veel) ook bekend als moleculair ion, is een geladen chemische verbinding: een ion dat wordt gevormd door de covalente binding tussen minstens twee atomen. Dat zijn meestal atomen van verschillende elementen. Bekende voorbeelden van polyatomische ionen zijn het hydroxideanion (OH−) en ammonium (NH4+). Ammonium is een kation.
Een polyatomisch ion kan vaak beschouwd worden als het geconjugeerde zuur of de geconjugeerde base van een neutraal molecuul. Het sulfaation (SO42−) is hiervan een voorbeeld: het is afgeleid van zwavelzuur (H2SO4), dat zelf als het hydraat van zwaveltrioxide kan worden beschouwd.
Een ion met maar één atoom is een monoatomisch ion.
Nomenclatuur
Er bestaan in de scheikundige nomenclatuur twee regels die kunnen worden toegepast om polyatomische ionen te benoemen. Wanneer het prefix bi- in de naam van een ion voorkomt, dan is aan de brutoformule van dat ion een waterstofion, een proton toegevoegd.[1] De lading van het ion stijgt met een elementaire lading. Als alternatief voor bi- wordt meestal waterstof- als prefix toegevoegd. Een voorbeeld is carbonaat (CO32−): wanneer hieraan een waterstof wordt toegevoegd, ontstaat waterstofcarbonaat met als brutoformule HCO3−.
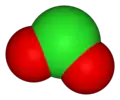
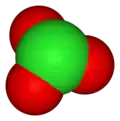
De tweede regel betreft het aantal zuurstofatomen in het ion en is meestal van toepassing bij oxoanionen. Een voorbeeld vormen de (oxo)anionen van chloor:
| oxidatietoestand | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| naam | chloride | hypochloriet | chloriet | chloraat | perchloraat |
| brutoformule | Cl− | OCl− | ClO2− | ClO3− | ClO4− |
| molecuulmodel |  |
 |
 |
 |
 |
De achtervoegsels -ide, -iet en -aat slaan op de verschillende oxidatietoestanden die chloor kan aannemen.
Meestvoorkomende polyatomische ionen
Onderstaande tabel geeft een overzicht van veel voorkomende polyatomische ionen met hun brutoformule, structuurformule en molaire massa.
Anionen
| Anion | Molaire massa (g/mol) | Brutoformule | Structuurformule |
|---|---|---|---|
| Acetaat | 59,04402 | C2H3O2− | 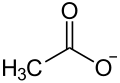 |
| Benzoaat | 121,1134 | C7H5O2− |  |
| Waterstofcarbonaat of bicarbonaat | 61,01684 | HCO3− |  |
| Carbonaat | 60,0089 | CO32− |  |
| Azide | 42,02065 | N3− | |
| Cyanide | 26,0174 | CN− | |
| Hydroxide | 17,00734 | OH− | |
| Nitraat | 62,0049 | NO3− | 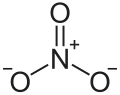 |
| Fosfaat | 94,971362 | PO43− | 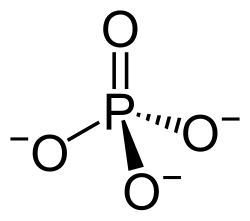 |
| Sulfaat | 96,0626 | SO42− |  |
| Chloraat | 83,4512 | ClO3− |  |
| Bromaat | 127,9022 | BrO3− | 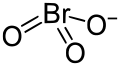 |
| Cyclopentadiënyl | 52,07511 | C5H5− | 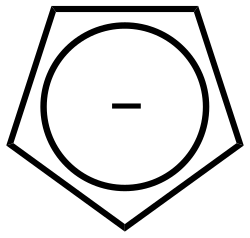 |
Kationen
| Kation | Molaire massa (g/mol) | Brutoformule | Structuurformule |
|---|---|---|---|
| Ammonium | 18,03846 | NH4+ | 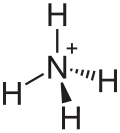 |
| Oxonium | 19,02322 | H3O+ |  |
| Dikwik(2+) | 401,18 | Hg22+ | |
| Tropylium | 91,13048 | C7H7+ | 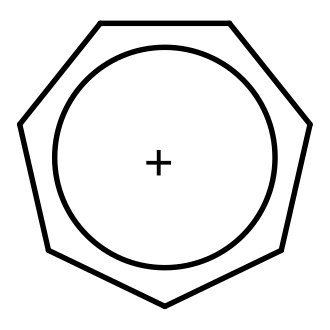 |
- voetnoten
- ↑ Dat wordt protonering genoemd.
- bronvermelding
- De sectie Nomenclatuur of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Polyatomic ion op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.