In-situhybridisatie

In-situhybridisatie (ISH) is een laboratoriumtechniek waarmee men specifieke DNA- of RNA-sequenties in intacte cellen of weefsels zichtbaar kan maken. Daarbij wordt een korte, gelabelde nucleïnezuurprobe gebruikt die bindt aan een complementaire doelsequentie. Omdat deze binding plaatsvindt in het oorspronkelijke materiaal (in situ), blijft de ruimtelijke organisatie van het aangetoonde nucleïnezuur behouden. ISH verschilt van immunohistochemie, dat zich richt op het detecteren van eiwitten door middel van gelabelde antilichamen.
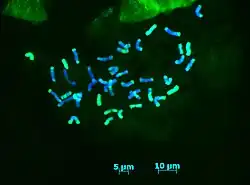
De techniek wordt toegepast om de ligging, organisatie en expressie van genen te onderzoeken. ISH kan worden uitgevoerd op weefselcoupes, hele kleine organismen of embryo's (zoals Drosophila), of op individuele cellen. Een van de belangrijkste variante technieken is fluorescentie-in-situhybridisatie (FISH), waarbij fluorescent gelabelde probes worden gebruikt om chromosomale sequenties zichtbaar te maken. FISH wordt onder andere toegepast in de diagnostiek om chromosoomafwijkingen op te sporen en de genetische veranderingen te beoordelen.
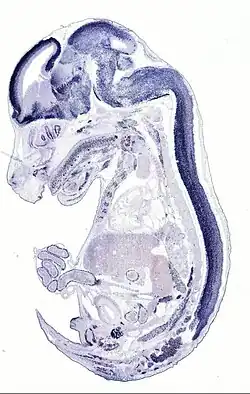
In-situhybridisatie werd in de jaren 1960 ontwikkeld door de Amerikaanse biologen Mary-Lou Pardue en Joseph G. Gall.[1][2] De techniek wordt in de moderne biologie voornamelijk toegepast om genexpressie ruimtelijk te analyseren, bijvoorbeeld tijdens de embryonale ontwikkeling, in hersenweefsels of in tumoren. Daarnaast wordt de techniek ingezet bij tumorprofilering, bijvoorbeeld het aantonen van virale nucleïnezuren in tumorweefsel.
Geschiedenis
In-situhybridisatie werd eind jaren zestig ontwikkeld door de Amerikaanse biologen Mary-Lou Pardue en Joseph G. Gall.[1][2] Ze gebruikten radioactief gelabelde probes (isotope labeling). De preparaten moesten vervolgens op een röntgenfilm worden geplaatst en werden voorzien van een foto-emulsie voor een betere resolutie met behulp van een microscoop. Naast de algemene problemen die met radioactiviteit gepaard gaan, was de ruimtelijke resolutie slecht vergeleken met de huidige technieken. Daarom werden probes die covalent aan de labelende moleculen waren gebonden later populair.
Voorbereiding voor de hybridisatie
Het doel van in-situhybridisatie is het detecteren van specifieke DNA- of RNA-sequenties en het bepalen waar deze zich bevinden in cellen of op chromosomen.[3] Optimale omstandigheden voor de hybridisatie van gezuiverde DNA- of RNA-extracten op vaste dragers hangen af van: monstervoorbereiding (weefsel of cel), constructie van de probe, labeling van de probe en de gevoeligheid van de voor detectie gebruikte methode.[4]
Preparaatvoorbereiding
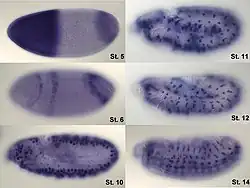
Voorafgaand aan de hybridisatie kan het weefsel of de cellen worden voorbehandeld om de efficiëntie te verhogen en niet-specifieke binding van probes te verminderen. Behandeling met proteasen, zoals proteïnase K, maakt de doel-DNA- of RNA-sequentie beter toegankelijk. Acetylering met 0,25% azijnzuuranhydride of 0,1 M tri-ethanolamine vermindert daarnaast de niet-specifieke binding van probes.
Fixatie is essentieel om de structuur van DNA, RNA en de morfologie van het weefsel te behouden. Tegelijk moeten de processen van DNA- en RNA-synthese of -afbraak stabiel blijven. Omdat mRNA vaak een korte levensduur heeft, moet weefsel zo snel mogelijk na excisie worden ingevroren. Voor fixatie wordt meestal paraformaldehyde gebruikt, soms in combinatie met glutaaraldehyde. Andere fixatieven bestaan uit mengsels van azijnzuur en alcohol. De oplossing van Bouin is een combinatiefixatief bestaande uit picrinezuur, formaldehyde en ijsazijn.[5][4]
Ontwerp van de probe
Probes kunnen bestaan uit cDNA, complementair RNA (cRNA) of synthetische oligonucleotiden. De keuze hangt af van gevoeligheid, specificiteit, productiegemak, weefselpenetratie en reproduceerbaarheid van de methode. Het gebruik van cDNA-probes is relatief populair, omdat dit stabieler is dan RNA en gemakkelijk kan worden vermenigvuldigd. Voor RNA-detectie worden riboprobes (complementair RNA) gebruikt, die met hoge specificiteit sense- en antisense-monsters kunnen produceren via in-vitro-transcriptie. Een ander voordeel is dat niet-gehybridiseerd RNA kan worden afgebroken met behulp van RNase en weggewassen. Over het algemeen zijn probes van 50–300 nucleotiden optimaal.[3]
Probes kunnen gelabeld worden met radioactieve isotopen (zoals 3H, 32P, 35S, 14C, 125I) of met niet-radioactieve markers, zoals biotine of specifieke antilichamen. Radioactieve labels zijn zeer gevoelig en kunnen zichtbaar worden gemaakt met autoradiografie of emulsies. Fluorescente of enzymatische labels bieden alternatieve detectiemethoden.[4]
Werkwijze van de techniek
Het principe van in-situhybridisatie is gebaseerd op complementaire basenparing: adenine bindt aan thymine (of uracil bij RNA), en guanine aan cytosine. De probe, die vooraf is gelabeld, zoekt in het preparaat naar exact overeenkomende sequenties en bindt daaraan. Alleen exacte of bijna exacte matches blijven stabiel gebonden, waardoor de techniek specifiek is. Dit proces kan in cellen, weefselcoupes of geïsoleerde chromosomen plaatsvinden.
Denaturatie
Omdat DNA meestal dubbelstrengs is, moet het eerst worden uiteengesmolten in enkelstrengse ketens (gedenatureerd). Denaturatie kan plaatsvinden door hitte of door pH-veranderingen. Formamide wordt vaak toegevoegd, omdat dit de waterstofbruggen tussen de strengen verzwakt, waardoor denaturatie bij lagere temperaturen (70–75 °C) mogelijk is en de chromosomale structuur beter behouden blijft. Ook technieken zoals moleculair combing kunnen het dubbelstrengse DNA denatureren.
Hybridisatie
De gelabelde probe wordt toegevoegd aan het preparaat en bindt aan de complementaire sequenties. De hybridisatietijd varieert van enkele uren tot meerdere dagen, afhankelijk van probe en doelsequentie. Gedurende deze tijd kan de probe door het weefsel diffunderen en aan complementaire sequenties hechten. Lange incubaties verhogen de gevoeligheid, maar verhogen uiteindelijk ook de kans op achtergrondsignaal. Parameters zoals zoutconcentratie en detergenten kunnen worden aangepast om niet-specifieke binding te minimaliseren.
Detectie van gebonden probes
Na hybridisatie worden de ongebonden probes, of niet-specifiek gebonden probes, weggewassen. Afhankelijk van het label worden de gebonden probes gedetecteerd via: autoradiografie bij radioactieve probes, fluorescentiemicroscopie bij fluorescerende labels, of immunohistochemie bij enzymatische of antigeen-gelabelde probes. Bij indirecte labeling bindt een antilichaam (of avidine, in geval van biotine) aan de probe, waarna een enzym een kleurstof vormt uit toegevoegde chromogene substraten. Hierdoor wordt de exacte locatie van de doelsequentie zichtbaar onder de microscoop.
Hierdoor worden alleen die cellen zichtbaar waarin het doel-RNA aanwezig is. Dit betekent dat alleen actieve genexpressie wordt gemarkeerd. Deze methode wordt veel toegepast in ontwikkelingsbiologie om de activiteit van specifieke genen te volgen, bijvoorbeeld tijdens embryogenese. Omdat het weefsel vooraf gefixeerd moet worden, geeft de kleuring geen informatie over dynamische processen; het is een momentopname van de toestand van het weefsel op het moment van fixatie.
Chromogene in-situhybridisatie
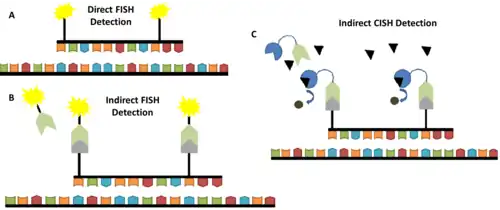

Bij chromogene in-situhybridisatie (CISH) worden peroxidase- of alkalische fosfatase-reacties gebruikt met behulp van helderveldmicroscopie in weefsels gefixeerd met formaline en ingebed in paraffine. Bij deze techniek worden antilichamen geconjugeerd met een enzym dat reacties van chromogene substraten katalyseert.[6] De resulterende chromogenen slaan neer op de doellocatie van de probe en kunnen worden gedetecteerd met helderveldmicroscopie.
Deze techniek biedt niet alleen een eenvoudig te gebruiken, economisch alternatief voor FISH, maar heeft ook het voordeel dat hiermee het weefsel zichtbaar gemaakt kan worden, inclusief de celkern en de vorm van de cel, samen met het signaal. In tegenstelling tot de meeste fluorescent detectiereagentia, zijn chromogene middelen die in de meeste CISH-methoden worden gebruikt, chemisch stabiel en vervagen ze niet na verloop van tijd, waardoor ze gemakkelijk kunnen worden bewaard en monsters opnieuw kunnen worden onderzocht.[7] De afbeelding toont de verschillen tussen fluorescentie-in-situhybridisatie (FISH) en chromogene in-situhybridisatie (CISH). Een van de toepassingen van CISH is dat de techniek ons in staat stelt de deletie van een gen, chromosomale translocaties en het chromosoom-nummer te onderzoeken.
Zilver-verbeterde in-situhybridisatie
Zilver-verbeterde in-situhybridisatie (Silver-enhanced in situ Hybridization (SISH)) is een variant van in-situhybridisatietechnieken, die gebruik maakt van metallografische detectie. Hier is de hybridisatieprobe gekoppeld aan een enzym dat neutraliseert en zorgt voor afzetting van metaal – meestal zilver – uit de oplossing op de doellocatie van de probe. De coupe wordt zwart gekleurd en is in het algemeen dicht, fijnkorrelig en absoluut stabiel.[7]
Genoom-in-situhybridisatie
Genoom-in-situhybridisatie (GISH) wordt op grote schaal gebruikt bij de moleculaire cytogenetica.[8]
Het belangrijkste kenmerk van deze techniek is dat terwijl FISH specifieke DNA-sequenties als probes gebruikt, GISH genoom-DNA van een soort als probe gebruikt. Met behulp van GISH is het mogelijk om de genomen in een hybride van elkaar te onderscheiden. De techniek werd aanvankelijk ontwikkeld voor hybride dierlijke cellijnen (1986) en later voor planten door het Plant Breeding Institute, Cambridge (1987), waar het zijn naam aan ontleent. De techniek omvat extractie, gevolgd door het labelen van DNA met een radioactieve isotoop uit het organisme dat als probe wordt gebruikt om het betreffende genoom te identificeren. Delen van het genoom die vergelijkbaar zijn met de probe hybridiseren en vormen een complex, dat vervolgens wordt gelabeld. De resterende ongehybridiseerde delen van het genoom worden via kleuring zichtbaar gemaakt.
De grote vooruitgang van deze techniek in relatie tot FISH is het labelen van volledige genomen, waardoor deze in veel onderzoeken voordelig wordt, bijvoorbeeld bij de identificatie van genomen en bij meiotische analyse.[9]
GISH wordt ook gebruikt bij de studie van nakomelingen van plantenhybriden, genetische plantenverbeteringsprogramma's en naar de evolutie van polyploïden. Ook kan GISH worden toegepast bij het onderzoek naar de relatie tussen plantensoorten.[10]
Polymerasekettingreactie met in-situhybridisatie
De polymerasekettingreactie (PCR) wordt gebruikt voor de amplificatie van specifieke DNA- of RNA-sequenties in cellen of weefselcoupes, zodat het aantal kopieën bij in-situ-PCR wordt verhoogd tot niveaus die detecteerbaar zijn met standaard in-situhybridisatiemethoden. Het belangrijkste nut ervan is het identificeren van DNA-sequenties die niet gemakkelijk te detecteren zijn met behulp van standaard in-situhybridisatie. Deze techniek heeft echter een lage amplificatie-efficiëntie en een slechte reproduceerbaarheid.[11] Direct in situ PCR resulteert vaak in vals positieven vanwege de opname van specifieke ongelabelde oligonucleotiden in DNA-fragmenten. Deze artefacten geven nucleaire signalen en zijn duidelijk zichtbaar in apoptotische cellen. De artefacten die het gevolg zijn van de techniek worden verminderd door de werking van een exonuclease of door reparatie van deze DNA-fragmenten met T4 DNA-ligase of door het gebruik van cycli met gelabelde probes. Vals positieven worden niet volledig geëlimineerd, maar de mate van specifieke detectie neemt toe.
Indirecte methoden bieden maximale specificiteit. Meestal worden lange complete probes of genomische probes gebruikt die het aantal reportermoleculen verhogen om een goed signaal te verkrijgen. De aard van de reportersystemen beïnvloedt de specificiteit van de techniek. Radioactieve sondes hebben een hoge stabiliteit, maar zijn erg duur. Colorimetrische systemen op basis van alkalische fosfatase of peroxiden resulteren in een slecht signaal. Op fluorescentie gebaseerde detectiesystemen worden niet aanbevolen omdat ze de weefselmorfologie niet behouden.[12]
- 1 2 O'Connor, Clare, Fluorescence In Situ Hybridization (FISH). Nature Education.
- 1 2 Gall, JG, Pardue, ML (June 1969). Formation and detection of RNA-DNA hybrid molecules in cytological preparations.. Proceedings of the National Academy of Sciences of the United States of America 63 (2): 378–83. PMID 4895535. PMC 223575. DOI: 10.1073/pnas.63.2.378.
- 1 2 Jensen, E. (2014). Technical Review: In Situ Hybridization. The Anatomical Record 297 (8): 1349–1353. DOI: 10.1002/ar.22944.
- 1 2 3 Höfler|nombre=Heinz. What's New in in Situ Hybridization, geraadpleegd in juni 1987, Pathology - Research and Practice, 182, 3, 421–430, DOI:10.1016/S0344-0338(87)80080-8
- ↑ Egger D., Troxler M., Bienz K. Light and electron microscopic in situ hybridization: non-radioactive labeling and detection, double hybridization, and combined hybridization-immunocytochemistry. geraadpleegd op 1 juni 1994. The Journal of Histochemistry and Cytochemistry: Official Journal of the Histochemistry Society, 42, 6, 815–822, ISSN 0022-1554, PMID 8189042
- ↑ Jensen, Ellen Technical Review: In Situ Hybridization, geraadpleegd op 1 augustus, The Anatomical Record, 297, 8, 1349–1353, ISSN 1932-8494, DOI:10.1002/ar.22944
- 1 2 Chromogenic in situ -Hybridization (CISH) and Silver enhanced in situ Hybridization (SISH)
- ↑ A. Jauch, C. Daumer, P. Lichter, J. Murken, T. Schroeder-Kurth, and T. Cremer Hum Genet (1990) 85:145-150 9 Springer-Verlag 1990 Chromosomal in situ suppression hybridization of human gonosomes and autosomes and its use in clinical cytogenetics
- ↑ Genomic in situ hybridization in plants, geraadpleegd 24 augustus 2015, Genetics and Molecular Research. Gearchiveerd op 31 maart 2022. Geraadpleegd op 18 april 2024.
- ↑ G.S. Silva and M.M. Souza Genomic in situ hybridization in plants. Genet Mol Res. 2013 Aug 12;12(3):2953-65. DOI:10.4238/2013.August.12.11. PMID 24065651.
- ↑ Qian Xiang, Lloyd Ricardo V. Recent developments in signal amplification methods for in situ hybridization, 1 maart 2003. Diagnostic Molecular Pathology: The American Journal of Surgical Pathology, Part B, 12, 1, 1–13, geraadpleegd op 4 december 2016, ISSN 1052-9551, PMID 12605030
- ↑ Franck Pellestor. PRINS and In Situ PCR Protocols Springer, geraadpleegd op 25 januari 2017