Hersengeslacht
Het hersengeslacht is de geslachtsdifferentiatie van de hersenen. Hoewel er sprake is van verschillen tussen de seksen, overlappen elkaar deze grotendeels en is er geen sprake van seksuele dimorfie zoals bij teelballen en eierstokken. Het is dan ook niet mogelijk om van een vrouwenbrein en een mannenbrein te spreken, of een continuüm daartussen, maar eerder van een mozaïek.[1] Het vasthouden aan de tweedeling van het binair geslachtsmodel kan bijdragen tot inconsistente onderzoeksresultaten of zelfs het achterwege blijven daarvan door publicatiebias. [2]
_for_data_from_human_tissues.png)
Hoewel seksuele selectie via seksueel conflict, interlocus of intralocus, seksuele differentiatie bevordert, kunnen somatische organen zoals hart, lever en nieren bij de mens niet simpelweg als mannelijk of vrouwelijk worden geclassificeerd. De variatie is daarvoor te groot en het geslachtsspecifieke karakter van organen evolueert zeer snel, vooral bij somatische organen.[3]
Zo overlapt 51% van het hersenvolume bij een studie tussen mannen en vrouwen, hoewel dit bij mannen gemiddeld groter is. Mannen hebben een gemiddeld groter lichaamsvolume, zodat het encefalisatiequotiënt dichter bij elkaar ligt. De fysieke verschillen in hersenmorfometrie zijn niet alleen relatief klein, de grote spreiding en multifactoriële overerving met samenwerkende genen maken dat hetzelfde resultaat op verschillende manieren bereikt kan worden (equifinaliteit), zodat de resulterende verschillen in fenotype en gedrag klein zijn en conclusies terughoudend moeten worden getrokken.[4] De verschillen in morfometrie komen niet overeen met de seksuele differentiatie die tot uiting komt in de sensorimotor-associatie-as, maar lijken afhankelijk van de functionele connectiviteit en de netwerktopologie.[5]
Aanvankelijk werd gedacht dat het vooral een hormonaal proces betrof, maar ook onafhankelijke genetische processen spelen een rol. Steeds meer wordt ook duidelijk dat dit niet een volledig deterministisch, maar ook een stochastisch proces is.[6] Daarnaast verschuift de aandacht van het in kaart brengen van componenten met hun functies naar een systeembiologische benadering van dynamische interacties om van een reductionistische visie naar een holistische of emergente visie te komen.[7]
Fysieke verschillen
Hoewel de gehele hersenen bij mannen gemiddeld 9-12% groter zijn, is bij vrouwen de hersenschors relatief groter, vooral in de paralimbische cortex, de staartkern en de voorste gordelwinding. Bij mannen zijn de frontomediale cortex, de hypothalamus, de amygdala, het putamen, de insula en de hoekwinding relatief groter.[8][9]
Vooral het preoptisch gebied in de hypothalamus speelt een grote rol in seksueel gedrag en kent een grote seksuele differentiatie, maar ook daarbuiten is dit te vinden:
- In de hypothalamus:
- Het preoptisch gebied (POA):
- Het mediaal preoptisch gebied (mPOA)
- De nucleus periventricularis anteroventralis (AVPV)
- De zona periventricularis:
- De nucleus suprachiasmaticus (SCN)
- De mediobasale hypothalamus:
- De nucleus ventromedialis (VMN)
- De boogvormige kern
- Het preoptisch gebied (POA):
- In het niet-seksuele deel van de hersenen:
- In de interhemisferische communicatie:
- De anterieure commissuur
- De massa intermedia
- De hersenbalk
- In de amygdala en limbisch systeem:
- Het posterodorsale deel van de mediale amygdala (MePD)[10]
- De bedkern van de stria terminalis (BNST)
- In de hippocampus[11]
- De hersenschors en witte stof
- In de interhemisferische communicatie:
Zoogdieren hebben een seksueel-dimorfe kern (SDN) in het mediaal preoptisch gebied. Deze SDN-POA is bij mannelijke dieren ongeveer twee keer zo groot en het testosteronniveau rond de geboorte is van grote invloed op de mannelijkheid of vrouwelijkheid van de SDN-POA. Bij ratten is het zelfs tot zo'n vijf keer zo groot.[12] Bij de mens werd in 1985 een seksueel-dimorfe kern gevonden, INAH-3.[13] In 1989 werd ook INAH-2 gevonden. De eerste is bij mannen tweemaal zo groot, de tweede 2,8 maal.[14] De vrouwelijke SDN-POA blijft kleiner door de apoptose of celdood van de neuronen.[15] Deze apoptose zet zich bij mensen in vanaf het vierde levensjaar, zodat deze kern zich pas dan seksueel gaat differentiëren. Van 50-60 jaar neemt het sterk af, bij vrouwen in nog grotere mate.[16]
De AVPV is groter bij vrouwen door apoptose bij mannen en is door het stimuleren van het gonadotropine-vrijzettend hormoon (GnRH) betrokken bij de LH-piek voorafgaande aan de ovulatie.
Naast dit volumeverschil zijn er grote verschillen in de ontwikkeling van axonen en dendrieten en het aantal synapsen dat wordt gevormd in de boogvormige kern en ventromediale kern van de hypothalamus en in de amygdala.[17] Zo heeft mannelijke INAH-3 meer neuronen.[18]

2. Oestrogeen
3. Luteïniserend hormoon
4. Progesteron
Geslachtshormonale fluctuaties zijn van invloed op de neurale plasticiteit, vooral in de microstructuren van de paralimbische cortex die een lage laminaire complexiteit kent.[19] Zo hebben fluctuaties van oestradiol en progesteron tijdens de menstruatiecyclus invloed op de neurale plasticiteit, waarbij oestradiol toeneemt tijdens de eerste helft van de cyclus met een piek rond de ovulatie en progesteron tijdens de tweede helft een verhoogd niveau heeft. Delen van de mediale temporale kwabben die van groot belang zijn voor het episodisch geheugen en ruimtelijke cognitie vergroten bij een hoog niveau oestradiol en laag niveau progesteron. Verder heeft een vroege menopause mogelijk een verhoogd risico op verouderende hersenen en dementie. Er is echter nog maar weinig onderzoek gedaan naar hormonale overgangsfases.[20]
Netwerkverschillen
De seksuele differentiatie in de sensorimotor-associatie-as hangen samen met verschillen in functionele connectiviteit en netwerktopologie in associatief netwerken, vooral het defaultnetwerk (DMN), maar ook het frontoparietale netwerk en het ventraal aandachtsnetwerk. Netwerktopologie heeft invloed op onder meer arousal, gewaarzijn en bewustzijn, gedrag en taakprestaties en cognitieve flexibiliteit.[5]
Overgewicht lijkt een ander effect te hebben bij mannen en vrouwen. Bij beiden zijn er aanwijzingen dat de axiale diffusiviteit, de snelheid van diffusie in de zenuwvezels, in de hersenbalk vertraagt, wat een axonale degeneratie, meer specifiek distale axonopathie, betekent. Alleen bij vrouwen was er ook sprake van radiale diffusiviteit waarbij de myeline rond de zenuwvezels afneemt. Deze myelinedegeneratie of demyelinisatie kan het verouderingsproces van de hersenen versnellen.[21]
Vrouwen hebben gemiddeld efficiëntere, minder gescheiden netwerken. Bij mannen hebben veelal een dichter netwerk binnen een gebied, maar minder verbindingen tussen de gebieden. Veroudering gaat in het algemeen gepaard met een vermindering van de netwerkcommunicatie (functionele integratie) en van functionele specialisatie en de functionele scheiding in specifieke gebieden van de hersenen. Veroudering lijkt bij mannen meer van invloed op de hersenen dan bij vrouwen.[22]
Hormonen
Aanvankelijk werden de verschillen vooral toegewezen aan de prenatale invloed van geslachtshormonen. In 1959 werd voor het eerst een organiserend effect op de seksuele ontwikkeling gevonden. De prenatale blootstelling aan testosteron bleek het gedrag van vrouwelijke cavia's te vermannelijken. Testosteron of een metaboliet zou inwerken op het deel van het centrale zenuwstelsel waar seksueel gedrag wordt georganiseerd.[23] Daarna werd ook bij resusapen gevonden dat androgenen het speelgedrag masculiniseren. Dit was de basis voor de organiserende-activerende hypothese, waarbij het organiserende effect tijdens de perinatale periode rond de geboorte – een kritieke periode – permanent en onomkeerbaar zijn, in tegenstelling tot het activerend effect dat tijdelijk en omkeerbaar is. In 1967 werd dit hormonale effect op de seksuele ontwikkeling ook bij mensen vastgesteld.[24]
Naast vermannelijking bleek ontvrouwelijking een apart hormonaal proces.[25][26] Verder bleek niet alleen de perinatale periode, maar ook de puberteit een kritieke periode te zijn waarin organiserende effecten de seksuele ontwikkeling van het neuraal netwerk beïnvloeden.[27][28][29] Ook oestradiol bleek de vermannelijking in gang te zetten, wat leidde tot de theorie van aromatisering waarbij testosteron de bloed-hersenbarrière passeert en daarna in de hersenen door aromatase wordt omgezet naar oestradiol.[30]
Bij primaten bleek aromatisering echter geen vereiste te zijn, aangezien het niet-aromatiseerbare dihydrotestosteron (DHT), dat bij cavia's geen mannelijk gedrag tot gevolg had, dit bij resusaapjes dit wel had. Daarnaast is bij primaten de kritieke periode niet perinataal, maar betreft het de prenatale periode.[31]
Genen
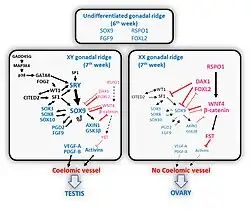
Geruime tijd leek de genetische invloed beperkt tot de rol bij de geslachtsbepaling die de gonadale differentiatie in gang zet, hoewel al wel duidelijk werd dat dit een complex genennetwerk is dat meer omvat dan alleen het SRY-gen. Gaandeweg werd duidelijk dat er behalve de hormonale as ook verschillen in genexpressies zijn die een seksuele differentiatie in gang zetten.[32][33]
Omdat de hormonale en genetische invloeden verweven zijn, moet onderzoek manieren vinden om dit onderscheid te vinden. Zo werd gevonden dat de zebravinken, waarbij alleen het mannetje zingt, bij gebruik van een aromataseremmer bij vrouwtjes deze wel testiculair weefsel ontwikkelen, maar niet gaan zingen.[34] Ook werden bij hersenonderzoek bij embryo's van muizen na 10,5 dagen post coitum (dpc) gevonden dat er al sprake was van differentiële expressie voordat er gonadale differentiatie was.[32]
Bij SF1-knock-out-muizen die zonder gonaden en bijnieren werden geboren en dan ook geen geslachtshormonen produceerden, werden vlak na de geboorte bijnieren getransplanteerd en corticosteroïden toegediend om te voorkomen dat ze stierven door bijnierschorsinsufficiëntie. Uit hersenonderzoek bij tot volwassenheid opgegroeide dieren bleek de expressie van neurale stikstofmonoxidesynthase (nNOS) in de VMN en de expressie van calbindine in de POA en de BNST lager, wat aansloot bij het ontbreken van geslachtshormonen tijdens de prenatale periode. Er bleek echter nog wel een differentiatie te zijn in de expressie van nNOS in de POA, AVPV en BNST en de expressie van calbindine in de VMN, wat een aanwijzing is voor een onafhankelijk genennetwerk.[35]
Voor het onderzoek wordt wel gebruikgemaakt van muismodellen met vier genotypes, vooral het four core genotypes model (FCG) en het XY*-model, waarbij XX- en XY-varianten beide een variant hebben met eierstokken en een met teelballen.[36][37][38]
Chromosomen
Er zijn verschillende chromosomen die genen bevatten die onderdeel uitmaken van genennetwerken die seksuele differentiatie in gang zetten buiten de hormonale as en de rol van SRY-gen bij de geslachtsbepaling.
Y-chromosoom, SRY-gen
Behalve in de gonaden, komt SRY op het Y-chromosoom bij mensen ook tot expressie in de bijnieren, hart en alvleesklier en in de hersenen in de hypothalamus en de frontale en temporale kwab.[39][40]
Bij muizen is gevonden dat Sry een expressie kent in de zwarte kern in de hersenen en daar een rol speelt bij motorische sturing van dopaminergische neuronen. Daarmee heeft Sry een directe invloed op de hersenen, buiten de geslachtshormonen om.[41]
Bij spontaan hypertensieve ratten blijkt Sry1 van invloed op de bloeddruk in de nieren.[42]
Bij de bruine rat heeft ook expressie van Sry in de bijnieren.[43]
X-chromosoom, X-inactivatie
X-inactivatie treedt bij vrouwen op bij een van de twee X-chromosomen. Zo'n 15% van de genen ontsnapt aan inactivatie en blijft dus actief, ongeveer het aantal genen op het Y-chromosoom. Deze dosiscompensatie maakt dat iedereen een gelijke gendosering van actieve geslachtsgenen heeft. Waarschijnlijk is deze dosiscompensatie nodig door het genverlies van het Y-chromosoom.[44] Door deze degeneratie hebben veel genen op het X-chromosoom geen homologon op het Y-chromosoom, wat schadelijke gevolgen kan hebben zonder dosiscompensatie. Mogelijk dragen deze ontsnappende genen bij aan seksuele dimorfie, al spelen autosomen hier de belangrijkste rol.[45][46]
X-chromosoom, imprinting
Bij imprinting of inprenting komt alleen van een van de ouders een allel van een gen tot expressie. Dit is ook het geval bij het X-chromosoom en alleen vrouwen hebben een X-chromosoom van hun vader, zodat alleen bij hen paternale ingeprente allelen voorkomen. In combinatie met X-inactivatie kan dit tot seksuele differentiatie leiden.[47]
Bij het syndroom van Turner (45,X) is er slechts een X-chromosoom en ontbreekt het tweede geslachtschromosoom. Dit leidt tot verschillende symptomen als het chromosoom afkomstig is van de moeder (Xm) of van de vader (Xp). Zo lijken er bij Xm meer sociale problemen op te treden dan bij Xm.[48] Er treedt echter ook hypogonadisme op, waardoor er ook hormonale effecten op kunnen treden tijdens de ontwikkeling van de hersenen.[49]
Autosomale imprinting
Een volledig maternaal (parthenogeen) en een volledig paternaal (androgeen) genoom ontwikkelen zich verschillend, wat een verschil in expressie suggereert.[50] Zo blijkt er bij muizen inderdaad een geslachtelijk verschil bij de autosomale genen Peg3, Zim1, Igf2, H19 en Zac1.[51]
Deze autosomale imprinting kan leiden tot zusteraandoeningen, zoals het syndroom van Prader-Willi en het syndroom van Angelman. Bij beide ontbreekt DNA op de lange arm van chromosoom 15 (15q11-13). Door imprinting worden normaal gesproken genen op deze locus uitgeschakeld. Dit zijn zowel genen die op het paternale allel tot expressie komen (onder meer SNRPN en NDN) als genen die op het maternale allel tot expressie komen (UBE3A). De reden hierachter is dat de paternale genen van SNRPN en NDN belangrijk zijn voor een goede ontwikkeling van de hypothalamus. Bij het syndroom van Prader-Willi worden deze paternale genen ook niet geactiveerd. De maternale genen van UBE3A zijn waarschijnlijk belangrijk voor de ontwikkeling van de hippocampus en de kleine hersenen en bij het syndroom van Angelman worden deze ook niet geactiveerd.
Stochastisch proces
Het aanvankelijke hormonale determinisme werd gaandeweg aangevuld met een genetisch determinisme of zelfs genetisering, dat naast genetisch determinisme waarbij omgevingsinvloeden worden verwaarloosd ook genetisch reductionisme omvat door alles te herleiden naar genetica en op genetisch essentialisme door de genen gelijk te stellen aan de identiteit. Dit deterministische proces waarbij de hormonale en genetische ontwikkeling geheel volgens duidelijke paden verloopt, is steeds meer onder druk komen te staan. Zo spelen bij moleculaire en cel-celinteractie kans en onzekerheid een grote rol, zoals enzymen en substraten met stochastische fluctuaties van chemische bindingen en bindingshoeken. Vooral bij lage concentratie en zeker bij individuele moleculen is er door onder meer de eiwitdynamiek sprake van cellulaire ruis.[6]
Als er sprake is van equifinaliteit kan hetzelfde resultaat op verschillende manieren bereikt worden, er is dus redundantie van ontwikkelingspaden. Multifinaliteit leidt juist vanuit dezelfde basis tot verschillende resultaten. Equifinaliteit betekent dat toeval weinig invloed heeft op de uitkomst, maar deze striktheid gaat ten koste van de robuustheid. Multifinaliteit betekent dat een connectoom een groter potentieel van adaptatie heeft om met onzekerheid om te gaan. Hoewel de ontwikkelingspaden minder redundant zijn en toeval een grotere rol speelt, is het eindresultaat robuuster. Kinderen die opgroeien met een lagere sociaaleconomische status in een veranderlijke omgeving lijken vaker een robuuster netwerk te hebben.[52]
Seksuele geaardheid
De seksuele geaardheid wordt vroeg in de ontwikkeling gevormd en de postnatale sociale omgeving lijkt hierbij geen rol te spelen.[53]
Aandoeningen
Vrouwen hebben een veel grotere kans op depressies die ontstekingsgerelateerd zijn, immuno-metabole depressies, waarbij er een verband is met fluctuaties van vrouwelijke hormonen.[54]
Noten
- ↑ Joel, D. (2020): 'Beyond the binary: Rethinking sex and the brain' in Neuroscience & Biobehavioral Reviews, Volume 122, p. 165-175
- ↑ Wiersch, L.; Weis, S. (2021): 'Sex differences in the brain: More than just male or female' in Cognitive Neuroscience, Volume 12, Issue 3-4, p. 187-188
- ↑ Xie, C.; Künzel, S.; Tautz, D. (2025): 'Fast evolutionary turnover and overlapping variances of sex-biased gene expression patterns defy a simple binary sex classification of somatic tissues' in eLife, 13:RP99602
- ↑ Eliot, L. (2024): 'Remembering the null hypothesis when searching for brain sex differences' in Biology of Sex Differences, Volume 15, Article 14
- 1 2 Serio, B.; Hettwer, M.D.; Wiersch, L.; Bignardi, G.; Sacher, J.; Weis, S.; Eickhoff, S.B.; Valk, S.L. (2024): 'Sex differences in functional cortical organization reflect differences in network topology rather than cortical morphometry' in Nature Communications, Volume 15, Article 7714
- 1 2 Balaban, E. (2006): 'Cognitive developmental biology: History, process and fortune's wheel' in Cognition, Volume 101, Issue 2, p. 298-332
- ↑ Keller, E.F. (2005): 'The century beyond the gene' in Journal of Biosciences, Volume 30, Issue 1, p. 3-10
- ↑ Goldstein, J.M.; Seidman, L.J.; Horton, N.J.; Makris, N.; Kennedy, D.N.; Caviness, V.S. Jr.; Faraone, S.V.; Tsuang, M.T. (2001): 'Normal Sexual Dimorphism of the Adult Human Brain Assessed by In Vivo Magnetic Resonance Imaging' in Cerebral Cortex, Volume 11, Issue 6, p. 490-497
- ↑ Lenroot, R.K.; Giedd, J.N. (2010): 'Sex differences in the adolescent brain' in Brain and Cognition, Volume 72, Issue 1, p. 46-55
- ↑ Zuloaga, D.G.; Puts, D.A.; Jordan, C.L.; Breedlove, S.M. (2008): 'The Role of Androgen Receptors in the Masculinization of Brain and Behavior: What we’ve learned from the Testicular Feminization Mutation' in Hormones and Behavior, Volume 53, Issue 5, p. 613-626
- ↑ Gillies, G.E.; McArthur, S. (2010): 'Estrogen Actions in the Brain and the Basis for Differential Action in Men and Women: A Case for Sex-Specific Medicines' in Pharmacological Reviews, Volume 62, Issue 2, p. 155-198
- ↑ Gorski, R.A.; Gordon, J.H.; Shryne, J.E.; Southam, A.M. (1978): 'Evidence for a morphological sex difference within the medial preoptic area of the rat brain' in Brain Research, Volume 148, Issue 2, p. 333-346
- ↑ Swaab, D.F.; Fliers, E. (1985): 'A sexually dimorphic nucleus in the human brain' in Science, Volume 228, Issue 4703, p. 1112-1115
- ↑ Allen, L.S.; Hines, M.; Shryne, J.E.; Gorski, R.A. (1989): 'Two Sexually Dimorphic Cell Groups in the Human Brain' in The Journal of Neuroscience, Volume 9, Issue 2, p. 497-506
- ↑ Wright, C.L.; Schwarz, J.S.; Dean, S.L.; McCarthy, M.M. (2010): 'Cellular mechanisms of estradiol-mediated sexual differentiation of the brain' in Trends in Endocrinology & Metabolism, Volume 21, Issue 9, p. 553-561
- ↑ Hofman, M.A.; Swaab, D.F. (1989): 'The sexually dimorphic nucleus of the preoptic area in the human brain: a comparative morphometric study' in Journal of Anatomy, Volume 164, p. 55-72
- ↑ Matsumoto, A. (1991): 'Synaptogenic action of sex steroids in developing and adult neuroendocrine brain' in Psychoneuroendocrinology, Volume 16, Issues 1–3, p. 25-40
- ↑ Byne, W.; Tobet, S.; Mattiace, L.A.; Lasco, M.S.; Kemether, E.; Edgar, M.A.; Morgello, S.; Buchsbaum, M.S.; Jones, L.B. (2001): 'The Interstitial Nuclei of the Human Anterior Hypothalamus: An Investigation of Variation with Sex, Sexual Orientation, and HIV Status' in Hormones and Behavior, Volume 40, Issue 2, p. 86-92
- ↑ Küchenhoff, S.; Bayrak, Ş.; Zsido, R.G.; Saberi, A.; Bernhardt, B.C.; Weis, S.; Schaare, H.L.; Sacher, J.; Eickhoff, S.; Valk, S.L. (2024): 'Relating sex-bias in human cortical and hippocampal microstructure to sex hormones' in Nature Communications, Volume 15, Article 7279
- ↑ Zsido, R.G.; Williams, A.N.; Barth, C.; Serio, B.; Kurth, L.; Mildner, T.; Trampel, R.; Beyer, F.; Witte, A.V.; Villringer, A.; Sacher, J. (2023): 'Ultra-high-field 7T MRI reveals changes in human medial temporal lobe volume in female adults during menstrual cycle' in Nature Mental Health, Volume 1, p. 761–771
- ↑ Mueller, K.; Anwander, A,; Möller, H.E.; Horstmann, A.; Lepsien, J.; Busse, F.; Mohammadi, S.; Schroeter, M.L.; Stumvoll, M.; Villringer, A.; Pleger, B. (2011): 'Sex-Dependent Influences of Obesity on Cerebral White Matter Investigated by Diffusion-Tensor Imaging' in PLOS One, Volume 6, Issue 4, e18544
- ↑ Heidi Foo; Anbupalam Thalamuthu; Jiyang Jiang; Forrest Koch; Karen A. Mather; Wei Wen; Perminder S. Sachdev (2021): 'Age- and Sex-Related Topological Organization of Human Brain Functional Networks and Their Relationship to Cognition' in Frontiers in Aging Neuroscience, Volume 13
- ↑ Phoenix, C.H.; Goy, R.W.; Gerall, A.A.; Young, W.C. (1959): 'Organizing action of prenatally administered testosterone propionate on the tissues mediating mating behavior in the female guinea pig' in Endocrinology, Volume 65, Issue 3, p. 369-382
- ↑ Ehrhardt, A. A.; Money, J.W. (1967): 'Progestin-Induced Hermaphroditism: IQ and Psychosexual Identity in a Study of Ten Girls' in Journal of Sex Research, Volume 3, Issue 1, p. 83-100
- ↑ Whalen, R.E. (1968): 'Differentiation of the neural mechanisms which control gonadotrophin secretion and sexual behavior' in Diamond, M. (ed.) Reproduction and Sexual Behavior, Indiana University Press, p. 303–340
- ↑ Vreeburg, J.T.M.; Vaart, P.D.M. van der; Schoot, P. van der (1977): 'Prevention of central defeminization but not masculinization in male rats by inhibition neonatally of oestrogen biosynthesis' in Journal of Endocrinology, Volume 74, Issue 3, p. 375-382
- ↑ Meek, L.R.; Romeo, R.D.; Novak, C.M.; Sisk, C.L. (1997): 'Actions of Testosterone in Prepubertal and Postpubertal Male Hamsters: Dissociation of Effects on Reproductive Behavior and Brain Androgen Receptor Immunoreactivity' in Hormones and Behavior, Volume 31, Issue 1, p. 75-88
- ↑ Sisk, C.L.; Zehr, J.L. (2005): 'Pubertal hormones organize the adolescent brain and behavior' in Frontiers in Neuroendocrinology, Volume 26, Issues 3-4, p. 163-174
- ↑ Schulz, K.M.; Sisk, C.L. (2016): 'The organizing actions of adolescent gonadal steroid hormones on brain and behavioral development' in Neuroscience & Biobehavioral Reviews, Volume 70, p. 148-158
- ↑ McCarthy, M.M.; Wright, C.L.; Schwarz, J.M. (2009): 'New tricks by an old dogma: mechanisms of the Organizational/Activational Hypothesis of steroid-mediated sexual differentiation of brain and behavior' in Hormones and Behavior, Volume 55, Issue 5, p. 655-665
- ↑ Wallen, K. (2005): 'Hormonal influences on sexually differentiated behavior in nonhuman primates' in Frontiers in Neuroendocrinology. Volume 26, Issue 1, p. 7–26
- 1 2 Dewing, P.; Shi, T.; Horvath, S.; Vilain, E. (2003): 'Sexually dimorphic gene expression in mouse brain precedes gonadal differentiation' in Molecular Brain Research, Volume 118, Issues 1–2, p. 82-90
- ↑ Davies, W.; Wilkinson, L.S. (2006): 'It is not all hormones: Alternative explanations for sexual differentiation of the brain' in Brain Research, Volume 1126, Issue 1, p. 36-45
- ↑ Wade, J.; Arnold, A.P. (1996): 'Functional testicular tissue does not masculinize development of the zebra finch song system' in Proceedings of the National Academy of Sciences, Volume 93, No. 11, p. 5264-5268
- ↑ Buedefeld, T.; Grgurevic, N.; Tobet, S.A.; Majdic, G. (2008) 'Sex differences in brain developing in the presence or absence of gonads' in Developmental Neurobiology, Volume 68, Issue 7, p. 981-995
- ↑ Arnold, A.P.; Chen, X. (2012): 'What does the “four core genotypes” mouse model tell us about sex differences in the brain and other tissues?' in Frontiers in Neuroendocrinology, Volume 30, Issue 1, p. 1-9
- ↑ Burgoyne, P.S.; Arnold, A.P. (2016): 'A primer on the use of mouse models for identifying direct sex chromosome effects that cause sex differences in non-gonadal tissues' in Biology of Sex Differences, Volume 7, Article 68
- ↑ Arnold, A.P. (2020): 'Four Core Genotypes and XY* mouse models: Update on impact on SABV research' in Neuroscience & Biobehavioral Reviews, Volume 119, p. 1-8
- ↑ Clépet, C.;Schafer, A.J.; Sinclair, A.H.; Palmer, M.S.; Lovell-Badge, R. Goodfellow, P.N. (1993): 'The human SRY transcript' in Human Molecular Genetics, Volume 2, Issue 12, p. 2007-2012
- ↑ Mayer, A.; Lahr, G.; Swaab, D.F.; Pilgrim, C.; Reisert, I. (1998): 'The Y-chromosomal genes SRY and ZFY are transcribed in adult human brain' in Neurogenetics , Volume 1, Issue 4, p. 281-288
- ↑ Dewing, P.; Chiang, C.W.K.; Sinchak, K.; Sim, H.; Fernagut, P.P.; Kelly, S.; Chesselet, M.F.; Micevych, P.E.; Albrecht, K.H.; Harley, V.R.; Vilain, E. (2006): 'Direct regulation of adult brain function by the male-specific factor SRY' in Current Biology, Volume 16, Issue 4, p. 415-420
- ↑ Ely, D.L.; Milsted, A.; Dunphy, G.; Boehme, S.; Dunmire, J.; Hart, M.; Toot, J.; Martins, A.; Turner, M.E. (2009): 'Delivery of sry1, but not sry2, to the kidney increases blood pressure and sns indices in normotensive wky rats' in BMC Physiology, Volume 9
- ↑ Turner, M.E.; Martin, C.; Martins, A.; Dunmire, J.; Farkas, J.; Ely, D.L.; Milsted, A. (2007): 'Genomic and expression analysis of multiple Sry loci from a single Rattus norvegicus Y chromosome' in BMC Genetics, Volume 8, Issue 1
- ↑ Graves, J.A.M. (2000): 'Human Y chromosome, sex determination, and spermatogenosis—A feminist view' in Biology of Reproduction, Volume 63, Issue 3, p. 667-676
- ↑ Berletch, J.B.; Yang, F.; Xu, J.; Carrel, L.; Disteche, C.M. (2011): 'Genes that escape from X inactivation' in Human Genetics, Volume 130, Issue 2, p. 237-245
- ↑ Deegan, D.F.; Engel, E. (2019): 'Sexual Dimorphism in the Age of Genomics: How, When, Where' in Frontiers in Cell and Developmental Biology, Volume 7
- ↑ Davies, W.; Isles, A.R.; Burgoyne, P.S.; Wilkinson, L.S. (2005): 'X-linked imprinting: effects on brain and behaviour' in BioEssays, Volume 28, Issue 1, p. 35-44
- ↑ Skuse, D.H.; James, R.S.; Bishop, D.V.M.; Coppin, B.; Dalton, P.; Aamodt-Leeper, G.; Bacarese-Hamilton, M.; Creswell, C.; McGurk, R.; Jacobs, P.A. (1997): 'Evidence from Turner's syndrome of an imprinted X-linked locus affecting cognitive function' in Nature, Volume 387, p. 705–708
- ↑ Knickmeyer, R.C.; Davenport, M. (2011): 'Turner syndrome and sexual differentiation of the brain: implications for understanding male-biased neurodevelopmental disorders' in Journal of Neurodevelopmental Disorders, Volume 3, Issue 4, p. 293-306
- ↑ Barton, S.C.; Surani, M.A.H.; Norris, M.L. (1984): 'Role of paternal and maternal genomes in mouse development' in Nature, Volume 311, Issue 5984, p. 374-376
- ↑ Faisal, M.; Kim, H.; Kim, J. (2015): 'Sexual differences of imprinted genes' expression levels' in Gene, Volume 533, Issue 1
- ↑ Carozza, S.; Akarca, D.; Astle, D. (2023): 'The adaptive stochasticity hypothesis: Modeling equifinality, multifinality, and adaptation to adversity' in Proceedings of the National Academy of Sciences , Volume 120, No. 42
- ↑ Bao, A.M.; Swaab, D.F. (2011): 'Sexual differentiation of the human brain: relation to gender identity, sexual orientation and neuropsychiatric disorders' in Frontiers in Neuroendocrinology, Volume 32, Issue 2, p. 214–226
- ↑ Slavich, G. M.; Sacher, J. (2019): 'Stress, sex hormones, inflammation, and major depressive disorder: Extending social signal transduction theory of depression to account for sex differences in mood disorders' in Psychopharmacology, Volume 236, Issue 10, p. 3063-3079
Literatuur
- Mûelenaere, L. de (2011): De invloed van geslachtshormonen op het dimorfisme van de hersenen