Bariumorthotitanaat
| Bariumorthotitanaat | ||||
|---|---|---|---|---|
| Algemeen | ||||
| Chemische formule | ||||
| IUPAC-naam | Dibariumtitaantetraoxide | |||
| Wikidata | Q4860828 | |||
| Beschrijving | hygroscopische, kleurloze vaste stof | |||
| Thermodynamische eigenschappen | ||||
| S |
197[1] J/mol·K | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Bariumorthotitanaat is het orthotitanaat van barium, een anorganische verbinding met de formule . Het is een kleurloze, vaste stof die interessant is in verband met zijn overeenkomst met bariumtitanaat, een elektrokeramische stof.
Structuur
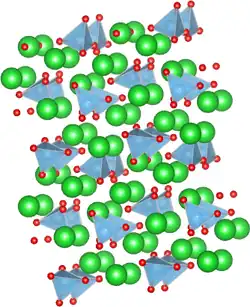
Van de vaste stof zijn twee modificaties bekend: een lage-temperatuur fase (β) met P21/n symmetrie[2] en een die bij hoge temperatuur stabiel is: (α′) met P21nb-symmetrie.[3] De structuur van Ba2TiO4 is in de groep titanaten ongebruikelijk, omdat de titaanatomen in een tetrahedron omringd zijn door vier zuurstofatomen. Een omringing met zes zuurstofatomen in een octahedron is de standaard in die groep.[2][4]
Synthese
Bariumothotitanaat wordt gevormd in een reactie die optreedt als BaCl2, BaCO3 en TiO2 samen tot smelten verhit worden,[5] of door het sinteren van BaCO3 en TiO2.[6] Een andere methode vormt het verwarmen van pellets Ba(OH)2 en TiO2.[1] Daarnaast zijn er syntheses beschreven die gebruik maken van polymere precursors, een sol-gel of micellen.[4] Ba2TiO4 is in de vorm van een dunne film gesynthetiseerd via chemical vapor deposition.[7]
Eigenschappen
- Diëlektrische constante: 20 (bij 100 kHz)[8]
- Bariumorthotitanaat is een hygroscopische vaste stof die in vochtige lucht met zwelling ontleedt.[9]
- Bariumorthotitanaat kan CO2 tot 99,9% verwijderen uit een stroom heet gas.[10] volgens de reactie:
Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Barium orthotitanate op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- 1 2 (en) S.S. Todd. (1952). Heat Capacities at Low Temperatures and Entropies at 298.16°K. of Orthotitanates of Barium and Strontium Journal of the American Chemical Society. 74 pag.: 2043–2045 DOI:10.1021/ja01135a014
- 1 2 (en) Kang Kun Wu, I.D. Brown. (1973). The Crystal Structure of β-Barium Orthotitanate, β-Ba2TiO4, and the Bond Strength-Bond Length Curve of Ti-O Acta Crystallographica. B29 pag.: 2009–2012 DOI:10.1107/S0567740873005959
- ↑ (en) John R. Günter, Geoffrey B. Jameson. (1983). Orthorhombic Barium Orthotitanate, α′-Ba2TiO4 Acta Crystallographica. C40 pag.: 207–210 DOI:10.1107/S0108270184003619
- 1 2 (en) Vishnu Shanker, Tokeer Ahmad, Ashok K. Ganguli. (2004). Investigation of Ba2–xSrxTiO4: Structural aspects and dielectric properties Bulletin of Materials Science. 27 (5): pag.: 421–427 DOI:10.1007/BF02708558
- ↑ (en) J.A. Bland. (1961). The Crystal Structure of Barium Orthotitanate, Ba2TiO4 Acta Crystallographica. 14 pag.: 875–881 DOI:10.1107/S0365110X61002527
- ↑ (en) Ya.S. Bobovich. The Raman Scattering of Barium Orthotitanate Optics and Spectroscopy. 13 pag.: 254–255
- ↑ (en) Dongyun Guo. High-speed growth of (103)-oriented Ba2TiO4 film by laser chemical vapor eposition Materials Letters. 70 pag.: 135–137 DOI:10.1016/j.matlet.2011.11.094
- ↑ (en) Tokeer Ahmad. (2004). Synthesis of nanometer-sized particles of barium orthotitanate prepared through a modified reverse micellar route: Structural characterization, phase stability and dielectric properties Journal of Materials Research. 19 pag.: 2905–2912 DOI:10.1557/JMR.2004.0406
- ↑ (en) Bernard Jaffe, William R. Cook Jr., Hans Jaffe. (1971). Piezoelectric Ceramics , hoofdstuk 5. Barium Titanate pag.: 62 – Academic Press (London and New York) ISBN 0123795508
- ↑ (en) Yoshinori Saito, Hideto Sato, Yukio Sakabe. (2008). CO2 Recovery at High Temperatures Using Ba2TiO4 Journal of Chemical Engineering of Japan. 41 (5): pag.: 441–446 DOI:10.1252/jcej.07WE236