Zirkonium(IV)chloride
| Zirkoontetrachloride | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
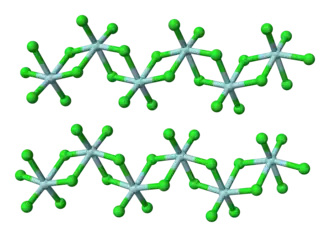 | ||||
| Algemeen | ||||
| Chemische formule | ZrCl4 | |||
| IUPAC-naam | zirkoontetrachloride, zirkoon(IV)chloride | |||
| Andere namen | zirkoniumtetrachloride, zirkonium(IV)chloride | |||
| Molaire massa | 233,04 g/mol | |||
| SMILES | Cl[Zr](Cl)(Cl)Cl | |||
| InChI | 1S/4ClH.Zr/h4*1H;/q;;;;+4/p-4 | |||
| CAS-nummer | 10026-11-6 | |||
| EG-nummer | 233-058-2 | |||
| Wikidata | Q205630 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H302 - H314 | |||
| EUH-zinnen | EUH014 | |||
| P-zinnen | P280 - P305+P351+P338 - P310 | |||
| Hygroscopisch? | ja | |||
| LD50 (ratten) | (oraal) 1690 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit | |||
| Dichtheid | 2,80 g/cm³ | |||
| Thermodynamische eigenschappen | ||||
| S |
181,41 J/mol·K | |||
| C |
125,38 J/mol·K | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Zirkoontetrachloride of zirkoon(IV)chloride is een chloride van zirkoon en bezit als verhoudingsformule ZrCl4. Het is een wit hygroscopisch kristallijn poeder dat snel hydrolyseert wanneer het aan de lucht wordt blootgesteld. De stof is van belang voor de productie van zuiver zirkoon en van andere zirkoonverbindingen en wordt ook gebruikt als katalysator in organische reacties.
Synthese
Zirkoontetrachloride wordt bereid door zirkoondioxide te behandelen met cokes (koolstof) en chloorgas:
Zirkoontetrachloride kan ook bereid worden door de rechtstreekse chlorering van zirkoon met chloorgas bij 650 °C, of met lood(II)chloride bij 500 °C:
Structuur
Net zoals het analoge hafniumtetrachloride bezit ook zirkoontetrachloride een polymere structuur. Daarin neemt zirkoon een octaëdrische moleculaire geometrie aan. Bij toevoeging van lewisbasen worden deze polymere structuren afgebroken en treedt degradatie van het materiaal op.
In tegenstelling tot titaantetrachloride, dat een vloeistof is, is zirkoontetrachloride niet te zuiveren door middel van destillatie.
Toepassingen
De reductie van zirkoontetrachloride levert metallisch zirkoon, dat een belangrijk materiaal is voor nucleaire reactoren.
Met behulp van chemical vapor deposition (CVD) kunnen dunne lagen van zirkoonverbindingen op een substraat aangebracht worden. Voorbeelden zijn:
- Zirkoondioxide (ZrO2) met behulp van zirkoontetrachloride en water[1]
- Zirkooncarbide (ZrC) met zirkoontetrachloride, methaan en waterstofgas als reductor.[2]
Zirkoontetrachloride is een katalysator voor organische reacties. Met zirkoontetrachloride (en andere zirkoonverbindingen) kunnen stereoselectieve syntheses van chirale verbindingen doorgevoerd worden, en dit met goede tot zeer goede opbrengst.[3] Zirkoontetrachloride wordt ook gebruik als lewiszuur in Diels-Alder-reacties.[4]
Met zirkoontetrachloride kunnen diverse organometaalcomplexen van zirkoon gevormd worden.[5] Deze complexen zijn onder meer bruikbaar als katalysator voor polymerisatiereacties.[6]
Externe links
- (en) Gegevens van zirkonium(IV)chloride in de GESTIS-stoffendatabank van het IFA
- (en) MSDS van zirkonium(IV)chloride
- ↑ (en) Michel Cassir, Fabrice Goubin, Cécile Bernay, Philippe Vernoux, Daniel Lincot. "Synthesis of ZrO2 thin films by atomic layer deposition: growth kinetics, structural and electrical properties". Applied Surface Science, 5 juni 2002, vol. 193 nr. 1-4, pp. 120-128. DOI:10.1016/S0169-4332(02)00247-7
- ↑ (en) Sun Wei, Hao Zheng Hua, Xiong Xiang. "Thermodynamic Analysis And Growth Of Zirconium Carbide By Chemical Vapor Deposition." Physics Procedia 2013, vol. 46, pp. 88-101. DOI:10.1016/j.phpro.2013.07.049
- ↑ (en) Sylvie Goncalves, Marc Nicolas, Philippe Maillos, Rachid Baati. "Cationic cyclization of keto-epoxides mediated by zirconium(IV)tetrachloride: diastereoselective synthesis of cis-decalinols." Tetrahedron, oktober 2011, vol. 67 nr. 45, p. 8373. DOI:10.1016/j.tet.2011.08.050
- ↑ (en) Masafumi Hirama, Yuji Kato, Chigusa Seki, Hiroto Nakano, Mitsuhiro Takeshita, Noriko Oshikiri, Masahiko Iyoda, Haruo Matsuyama. "An efficient synthesis of chiral isoquinuclidines by Diels–Alder reaction using Lewis acid catalyst." Tetrahedron, 18 september 2010, vol. 66 nr. 38, pp. 7618-7624. DOI:10.1016/j.tet.2010.07.026
- ↑ (en) A. Clearfield, E.J. Malkiewich. "Complexes formed by the reaction of zirconium tetrachloride with amides." Journal of Inorganic and Nuclear Chemistry, april 1963, vol. 25 nr. 3, pp. 237-240. DOI:10.1016/0022-1902(63)80047-0
- ↑ (en) Carlos Carone, Viviane de Lima, Fernanda Albuquerque, Paula Nunes, Cristóvão de Lemos, João H.Z. dos Santos, Griselda B. Galland, Fernanda C. Stedile, Sandra Einloft, Nara R. de S. Basso. "Zirconium alkoxide complexes as catalysts for ethylene polymerization." Journal of Molecular Catalysis A: Chemical, 2 februari 2004, vol. 208 nr. 1–2, pp. 285-290. DOI:10.1016/S1381-1169(03)00540-5

