Panethcel

_Differentiation_of_Paneth_cells.jpg)
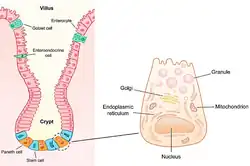
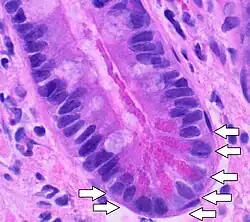
Panethcellen[1] zijn merocriene kliercellen die apicaal sterk eosinofiele granula bevatten en voorkomen in het epitheel aan de basis van de crypten van Lieberkühn in de dunne darm, maar ook in de maag en de endeldarm. Ze bevatten zymogeenkorrels aan de apicale pool. Merocriene kliercellen scheiden via exocytose stoffen af die in de kliercel gemaakt worden en waarbij de kliercel heel blijft. De taak van panethcellen is de secretie van lysozymen, peptidasen, lactoferrine en defensinen. Ze zijn daarom onder andere: verantwoordelijk voor de lokale immuunverdediging. Ze zijn vernoemd naar de Oostenrijkse fysioloog Joseph Paneth (1857-1890).
Er wordt aangenomen dat panethcellen de integriteit van het slijmvlies van de dunne darm helpen behouden, omdat ze zich dicht bij de stamcellen van de dunne darm bevinden. Hier brengen zij onder andere NOD2 tot expressie. Volgens onderzoek zou een verminderde productie van de antibacteriële defensinen de oorzaak kunnen zijn van de ziekte van Crohn.[2])
Als ze in de maag veel voorkomen, bestaat het risico op maagzweren.
Structuur
Panethcellen worden overal in de dunne darm en in de crypten van Lieberkühn aangetroffen.[3] Het aantal panethcellen neemt toe richting het einde van de dunne darm.[4] Net als de andere epitheliale cellijnen in de dunne darm, ontstaan panethcellen in het stamcelgebied nabij de bodem van de crypt.[5] Er zijn gemiddeld 5-12 panethcellen in elke dunne darmcrypte.[6]
In tegenstelling tot de andere epitheliale celtypen migreren panethcellen naar beneden vanuit het stamcelgebied en vestigen zich er vlak naast.[5] Deze nauwe relatie met de stamcelregio suggereert dat panethcellen belangrijk zijn bij het verdedigen van de stamcellen van de klier tegen microbiële schade,[5] hoewel hun functie niet volledig bekend is.[3] Panethcellen leven ongeveer 57 dagen.[7]
Functie

Panethcellen scheiden antimicrobiële peptiden en eiwitten af, die belangrijke mediatoren zijn van gastheer-microbe-interacties, waaronder homeostatisch evenwicht met koloniserende microbiota en aangeboren immuunbescherming tegen darmpathogenen.[8]
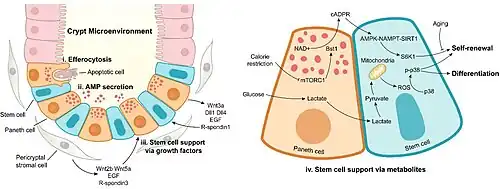
Dunne darmcrypten herbergen stamcellen die dienen om epitheelcellen die afsterven en uit de darmvlokken verdwijnen, voortdurend aan te vullen.[8] Panethcellen ondersteunen de fysieke barrière van het epitheel door essentiële nichesignalen te leveren aan hun aangrenzende intestinale stamcellen. Bescherming en stimulatie van deze stamcellen is essentieel voor het langetermijnonderhoud van het intestinale epitheel, waarin panethcellen een cruciale rol spelen.[9]
Opmerken aanwezigheid van microbiota
Panethcellen worden gestimuleerd om defensinen af te scheiden wanneer ze worden blootgesteld aan bacteriën (zowel gram-positieve als gram-negatieven, of bacteriële producten zoals lipopolysaccharide, lipoteichoïnezuur, muramyldipeptide en endotoxinen.[10] They are also stimulated by cholinergic signaling normally preceding the arrival of food which potentially may contain a new bacterial load.[10] Ze worden ook gestimuleerd door cholinerge signalering die normaal gesproken voorafgaat aan de aankomst van voedsel dat mogelijk een nieuwe bacteriële lading kan bevatten.[10]
Panethcellen nemen bacteriën waar via MyD88-afhankelijke toll-like receptor (TLR)-activering die vervolgens de antimicrobiële werking in gang zet.[11] Onderzoek toonde bijvoorbeeld aan dat in de secretoire korrels, muizen- en menselijke Paneth-cellen hoge niveaus van TLR9 tot expressie brengen. TLR9 reageert op CpG-ODN en ongemethyleerde oligonucleotiden, pathogeen-geassocieerde moleculaire patronen (PAMP's) die typisch zijn voor bacterieel DNA. De reactie van deze PAMP's en het activeren van TLR9 leidt tot degranulatie en afgifte van antimicrobiële peptiden en andere afscheidingen.[12] Verrassend genoeg produceren panethcellen van muizen geen mRNA-transcripten voor TLR4.[6]
Antimicrobiële secreties

De belangrijkste verdedigingsmoleculen die door panethcellen worden afgescheiden, zijn alfa-defensinen, die bij muizen bekend staan als cryptdinen.[13] Deze peptiden hebben hydrofobe en positief geladen domeinen die kunnen interacteren met fosfolipiden in celmembranen. Deze structuur stelt defensinen in staat om zich in membranen te nestelen, waar ze met elkaar interacteren voor het vormen van poriën die de membraanfunctie verstoren, wat leidt tot cellyse. Vanwege de hogere concentratie van negatief geladen fosfolipiden in bacteriële dan in gewervelde celmembranen, binden defensinen zich bij voorkeur aan bacteriële cellen en verstoren ze deze, waardoor de cellen die ze beschermen, worden bespaard.[14]
Menselijke panethcellen produceren twee α-defensinen, bekend als humane α-defensin HD-5 (DEFA5) en HD-6 (DEFA6).[15] HD-5 heeft een breed spectrum aan dodende activiteit tegen zowel gram-positieve als gram-negatieve bacteriën en schimmels (Listeria monocytogenes, Escherichia coli, Salmonella typhimurium en de gist Candida albicans).[6] The antimicrobial activity of HD-6 consists of self-assembling into extracellular nets that entrap bacteria in the intestine and thereby preventing their translocation across the epithelial barrier.[16] De antimicrobiële activiteit van HD-6 bestaat uit het zichzelf assembleren in extracellulaire netten die bacteriën in de darm vangen en zo hun translocatie door de epitheliale barrière voorkomen.[16]
Menselijke panethcellen produceren ook andere AMP's, waaronder lysozym, secretoire fosfolipase A2 en REG3A.[17] Lysozym is een antimicrobieel enzym dat de celwanden van veel bacteriën oplost, en fosfolipase A2 is een enzym dat gespecialiseerd is in de lysis van bacteriële fosfolipiden.[10] Deze batterij van secretoire moleculen geeft panethcellen een krachtig arsenaal tegen een breed spectrum aan middelen, waaronder bacteriën, schimmels en zelfs sommige virussen, die een virusenvelop hebben.[18]
Secretoire autofagie
Tijdens conventionele eiwitsecretie worden eiwitten getransporteerd via het golgicomplex, verpakt in secretoire korrels en vrijgegeven aan de extracellulaire ruimte. Mochten invasieve pathogenen het golgicomplex verstoren, waardoor de secretie van antimicrobiële eiwitten door de panethcel wordt verstoord, dan bestaat er een alternatieve secretieroute: het is aangetoond dat lysozym via secretoire autofagie kan worden omgeleid. Bij secretoire autofagie wordt het product getransporteerd in een MAP1LC3B-blaasje en afgevoerd via het celmembraan, waardoor het golgicomplex wordt omzeild. Niet alle bacteriën veroorzaken secretoire autofagie: commensale bacteriën veroorzaken bijvoorbeeld geen golgicomplex-afbraak en activeren daarom niet de secretoire autofagie van lysozym. Een stoornis in secretoire autofagie wordt beschouwd als een mogelijke bijdragende factor aan de ziekte van Crohn.[19]
Fagocytische functie
Panethcellen houden de gezondheid van de darm in stand door als macrofagen te fungeren; het is aangetoond dat Paneth-cellen stervende cellen opruimen. De fagocytische functie van panethcellen werd ontdekt met behulp van een reeks experimenten, waarvan er één gebruikmaakte van muizen die werden bestraald met een lage dosis Cesium-137 (137Cs), wat chemotherapie nabootst die kankerpatiënten ondergaan.[20] Deze bevindingen kunnen van belang zijn voor het aanpakken van de bijwerkingen die kankerpatiënten ondervinden bij wie de darmgezondheid is beschadigd door chemotherapie: ongeveer 40% van alle kankertherapiepatiënten ervaart mucositis tijdens hun behandeling, waarbij het aantal stijgt tot 80% bij patiënten die buik- of bekkenbestraling krijgen.[21] Mucositis is de pijnlijke ontsteking van de slijmvliezen die het spijsverteringskanaal bekleden en aanleiding kan geven tot een maagzweer.
Epitheelonderhoud
Panethcellen nemen deel aan het Wnt-signaleringspad en het Notch-signaleringspad, die de proliferatie van darm stamcellen en enterocyten reguleren die nodig zijn voor de vernieuwing van epitheelcellen. Ze brengen de canonieke Wnt-liganden tot expressie: Wnt3a, Wnt9b en Wnt11, die zich binden aan Frizzled-receptoren op darmstamcellen om β-catenine/Tcf-signalering aan te sturen. Panethcellen zijn ook een belangrijke bron van Notch-liganden DLL1 en DLL4, die zich binden aan de Notch-receptoren Notch1 en Notch2 op darmstamcellen en enterocyt-voorlopercellen.[9]
Onlangs is echter ontdekt dat het regeneratieve potentieel van intestinale epitheelcellen in de loop van de tijd afneemt als gevolg van het feit dat verouderde panethcellen het eiwit notum afscheiden, wat een extracellulaire remmer is van Wnt-signalering. Als de Notum-secretie wordt geremd, kan het regeneratieve potentieel van het darmepitheel toenemen.[22]
Zink
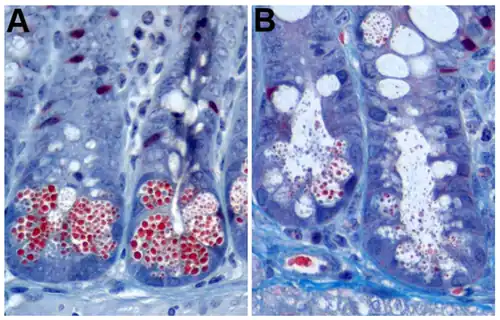
Het is vastgesteld dat zink essentieel is voor de functie van panethcellen. Een defect in de Zink-transporter (ZnT)2 verstoort de functie van panethcellen door ongecoördineerde korrelsecretie te veroorzaken. Muizen zonder de (ZnT)2-transporter vertonen niet alleen een verstoorde korrelsecretie, ze lijden ook aan een verhoogde ontstekingsreactie op lipopolysaccharide en zijn minder in staat tot bacteriedodende activiteit.[23] Normaal gesproken wordt zink opgeslagen in de secretoire korrels en komt het, na degranulatie, vrij in de darm. Er is gespeculeerd dat de opslag van zware metalen bijdraagt aan directe antimicrobiële toxiciteit, aangezien zink vrijkomt bij cholinerge panethcelstimulatie.[24]
Zinktekort is ook betrokken bij alcohol-geïnduceerde panethcel α-defensine-stoornis, wat bijdraagt aan alcoholgerelateerde steatohepatitis. Steatohepatitis (in de volksmond ook wel vette lever-hepatitis genoemd) is een ziekte waarbij ontstekingsveranderingen optreden in een vette lever, hoewel er geen sprake is van een infectieuze oorzaak bijvoorbeeld door virussen. Zink kan de menselijke α-defensine 5 (HD5) stabiliseren, die verantwoordelijk is voor de homeostase van het microbioom. In lijn hiermee kan de toediening van HD5 het microbioom effectief veranderen (vooral door de symbiontische bacterie Akkermansia muciniphila te verhogen) en de schade die aan het microbioom is toegebracht door overmatig alcoholgebruik, ongedaan maken. Een tekort aan zink in de voeding verergert daarentegen het schadelijke effect van alcohol op de bacteriedodende activiteit van panethcellen.[25]
Klinische betekenis
Abnormale panethcellen met verminderde expressie of secretie van defensinen HD-5 en HD-6 (bij mensen) en antimicrobiële peptiden worden geassocieerd met inflammatoire darmziekte.[26][17] Daarnaast worden verschillende van de allelen die het risico op de ziekte van Crohn lopen, geassocieerd met een stoornis van de panethcellen die betrokken zijn bij processen zoals autofagie, de ontvouwde proteïnerespons (UPR) en de regulatie van de mitochondriale functie. De ontvouwde proteïnerespons is een cellulaire stressrespons die verband houdt met de stress van het endoplasmatisch reticulum.[17]
Er wordt aangenomen dat een stoornis van de panethcellen de antimicrobiële peptiden in gevaar brengt, wat leidt tot een verschuiving van de samenstelling van de microbiota en zelfs dysbacteriose.[27] Patiënten met de ziekte van Crohn met een hoger percentage abnormale panethcellen vertoonden een significant verminderde bacteriële diversiteit vergeleken met patiënten met een lager percentage abnormale panethcellen, wat een verminderde overvloed aan ontstekingsremmende microben weerspiegelt.[28] Gezamenlijk ondersteunen deze bevindingen de theorie dat een stoornis van de panethcellen kan leiden tot een dysbacteriotische microbiota die op zijn beurt een individu vatbaar kan maken voor de ontwikkeling van de ziekte van Crohn.[17] Het moet echter nog worden vastgesteld of een stoornis van de panethcellen de oorzaak is van dysbacteriose, of het gelijktijdige effect ervan.[27]
Necrotiserende enterocolitis
Panethcellen ontwikkelen zich geleidelijk tijdens de zwangerschap en daarom hebben te vroeg geboren baby's er mogelijk niet genoeg van. Dit maakt te vroeg geboren baby's kwetsbaar voor necrotiserende enterocolitis. Ongeveer halverwege de ontwikkeling van de dunne darm wordt de secretie van cathelicidine vervangen door de secretie van α-defensine.[29] De dunne darm van de te vroeg geboren baby bevindt zich in deze overgangsfase wanneer de baby wordt geboren, waardoor te vroeg geboren baby's vatbaar zijn voor darmletsel en vervolgens voor necrotiserende enterocolitis.[18] Bovendien moet worden opgemerkt dat vroege panethcellen geen volledig functionele, volwassen korrels bezitten.[30]
Het mechanisme dat panethcellen koppelt aan necrotiserende enterocolitis blijft onduidelijk, maar er is een theorie dat een bloei van Proteobacteriën en, meer specifiek, Enterobacteriaceae-soorten voorafgaat aan de ontwikkeling van de aandoening.[31] Wanneer er vervolgens een ontsteking optreedt, kunnen nitraten worden gefermenteerd door Enterobacteriaceae sp. maar niet door obligate anaeroben, die geen nitraten als groeisubstraat kunnen gebruiken. Proteobacteria zijn dus in staat om deze selectiedruk te gebruiken om de obligate anaerobe Firmicutes en Bacteroidota weg te concurreren, wat resulteert in hun overgroei en daaropvolgende dysbacteriose.[18]
Men denkt dat het proces begint wanneer de te vroeg geboren baby wordt blootgesteld aan vreemde antigenen via flesvoeding. Vervolgens worden ontstekingsbevorderende cytokinen vrijgegeven, waardoor een meer aerobe toestand ontstaat die leidt tot een concurrentievoordeel voor Proteobacteria. Naarmate het microbioom dysbacteriotischer wordt, verzwakken ontstekingsremmende mechanismen, wat bijdraagt aan een cyclus van toenemende darmontsteking. De ontsteking leidt tot een verder verlies van de dichtheid en functie van panethcellen, wat resulteert in de aantasting van de adenosinemonofosfaat-secretie en de vernietiging van de stamcelniche.[18]
Niet-alcoholische leververvetting
Terwijl de rol van panethcellen bij het prikkelbare darmsyndroom en de ziekte van Crohn veel aandacht heeft gekregen,[32][17] is er relatief weinig bekend over het effect dat Paneth-celbeschadiging heeft op het ziekteverloop van niet-alcoholische leververvetting.
Muizenmodellen geven aan dat obesitas de secretie van α-defensine uit panethcellen kan verminderen, wat leidt tot dysbacteriose[33] en ten minste één muizenmodel suggereert dat wanneer α-defensine-niveaus in de darm worden hersteld door intraveneuze toediening van R-Spondin1 om panethcelregeneratie te induceren wordt leverfibrose verbeterd als gevolg van het opheffen van de dysbacteriose-verstoring. Er wordt verondersteld dat selectieve microbicide activiteiten, evenals het verhogen van Muribaculaceae en het verlagen van Harryflintia, bijdragen aan verbetering van de fibrose.[34]
Eén onderzoek beschreef de injectie van dithizon, dat celgranulaten kan verstoren, in muizen die een vetrijk dieet kregen om op panethcellen gerichte microbiële veranderingen te identificeren. De toepassing van dithizon verbeterde de glucose-intolerantie en insulineresistentie van een vetrijk dieet en werd geassocieerd met een verlichting van de ernst van leververvetting bij muizen met een vetrijk dieet, mogelijk door modulatie van het darmmicrobioom met de toename van Bacteroides. Er is daarom gesuggereerd dat op het microbioom gerichte therapieën een rol kunnen spelen bij de behandeling van niet-alcoholische leververvetting.[35]
 |
 |
 |
- voetnoten
- ↑ Everdingen, J.J.E. van, Eerenbeemt, A.M.M. van den (2012). Pinkhof Geneeskundig woordenboek (12de druk). Houten: Bohn Stafleu Van Loghum.
- ↑ Watanabe, T., Kitani, A., Strober, W. (2005-11). NOD2 regulation of Toll-like receptor responses and the pathogenesis of Crohn's disease. Gut 54 (11): 1515–1518. ISSN:0017-5749. PMID: 16227353. PMC: 1774769. DOI:10.1136/gut.2005.071795.
- 1 2 Paneth's cell | anatomy. Britannica.com. Geraadpleegd op 17 september 2016.
- ↑ Wallaeys C, Garcia-Gonzalez N, Libert C (December 2022). Paneth cells as the cornerstones of intestinal and organismal health: a primer. EMBO Molecular Medicine 15 (2): e16427. PMID 36573340. PMC 9906427. DOI: 10.15252/emmm.202216427.
- 1 2 3 Duggan C, Watkins JB, Walker WA (2008). Nutrition in Pediatrics: Basic Science, Clinical Applications. B.C. Decker, p. 244. ISBN 9781550093612. Geraadpleegd op 17 september 2016.
- 1 2 3 Elphick DA, Mahida YR (December 2005). Paneth cells: their role in innate immunity and inflammatory disease. Gut 54 (12): 1802–1809. PMID 16284290. PMC 1774800. DOI: 10.1136/gut.2005.068601.
- ↑ Ireland H, Houghton C, Howard L, Winton DJ (August 2005). Cellular inheritance of a Cre-activated reporter gene to determine Paneth cell longevity in the murine small intestine. Developmental Dynamics 233 (4): 1332–1336. PMID 15937933. DOI: 10.1002/dvdy.20446.
- 1 2 Clevers HC, Bevins CL (2013). Paneth cells: maestros of the small intestinal crypts. Annual Review of Physiology 75: 289–311. PMID 23398152. DOI: 10.1146/annurev-physiol-030212-183744.
- 1 2 Cray P, Sheahan BJ, Dekaney CM (2021). Secretory Sorcery: Paneth Cell Control of Intestinal Repair and Homeostasis. Cellular and Molecular Gastroenterology and Hepatology 12 (4): 1239–1250. PMID 34153524. PMC 8446800. DOI: 10.1016/j.jcmgh.2021.06.006.
- 1 2 3 4 Ganz T (August 2000). Paneth cells--guardians of the gut cell hatchery. Nature Immunology 1 (2): 99–100. PMID 11248797. DOI: 10.1038/77884.
- ↑
- ↑ Rumio C, Besusso D, Palazzo M, Selleri S, Sfondrini L, Dubini F, Ménard S, Balsari A (August 2004). Degranulation of paneth cells via toll-like receptor 9. The American Journal of Pathology 165 (2): 373–381. PMID 15277213. PMC 1618569. DOI: 10.1016/S0002-9440(10)63304-4.
- ↑ Wilson CL, Ouellette AJ, Satchell DP, Ayabe T, López-Boado YS, Stratman JL, Hultgren SJ, Matrisian LM, Parks WC (October 1999). Regulation of intestinal alpha-defensin activation by the metalloproteinase matrilysin in innate host defense. Science 286 (5437): 113–117. PMID 10506557. DOI: 10.1126/science.286.5437.113.
- ↑ Ayabe T, Satchell DP, Wilson CL, Parks WC, Selsted ME, Ouellette AJ (August 2000). Secretion of microbicidal alpha-defensins by intestinal Paneth cells in response to bacteria. Nature Immunology 1 (2): 113–118. PMID 11248802. DOI: 10.1038/77783.
- ↑ Ehmann D, Wendler J, Koeninger L, Larsen IS, Klag T, Berger J, Marette A, Schaller M, Stange EF, Malek NP, Jensen BA, Wehkamp J (February 2019). Paneth cell α-defensins HD-5 and HD-6 display differential degradation into active antimicrobial fragments. Proceedings of the National Academy of Sciences of the United States of America 116 (9): 3746–3751. PMID 30808760. PMC 6397583. DOI: 10.1073/pnas.1817376116.
- 1 2 Schroeder BO, Ehmann D, Precht JC, Castillo PA, Küchler R, Berger J, Schaller M, Stange EF, Wehkamp J (May 2015). Paneth cell α-defensin 6 (HD-6) is an antimicrobial peptide. Mucosal Immunology 8 (3): 661–671. PMID 25354318. PMC 4424388. DOI: 10.1038/mi.2014.100.
- 1 2 3 4 5 Lee VH, Gulati AS (November 2022). Implications of Paneth cell dysfunction on gastrointestinal health and disease. Current Opinion in Gastroenterology 38 (6): 535–540. PMID 36165037. PMC 9561020. DOI: 10.1097/MOG.0000000000000887.
- 1 2 3 4 Lueschow SR, McElroy SJ (2020). The Paneth Cell: The Curator and Defender of the Immature Small Intestine. Frontiers in Immunology 11: 587. PMID 32308658. PMC 7145889. DOI: 10.3389/fimmu.2020.00587.
- ↑ Bel S, Pendse M, Wang Y, Li Y, Ruhn KA, Hassell B, Leal T, Winter SE, Xavier RJ, Hooper LV (September 2017). Paneth cells secrete lysozyme via secretory autophagy during bacterial infection of the intestine. Science 357 (6355): 1047–1052. PMID 28751470. PMC 5702267. DOI: 10.1126/science.aal4677.
- ↑ Shankman LS, Fleury ST, Evans WB, Penberthy KK, Arandjelovic S, Blumberg RS, Agaisse H, Ravichandran KS (June 2021). Efferocytosis by Paneth cells within the intestine. Current Biology 31 (11): 2469–2476.e5. PMID 33852873. PMC 8281366. DOI: 10.1016/j.cub.2021.03.055.
- ↑ Hauer-Jensen M, Denham JW, Andreyev HJ (August 2014). Radiation enteropathy--pathogenesis, treatment and prevention. Nature Reviews. Gastroenterology & Hepatology 11 (8): 470–479. PMID 24686268. PMC 4346191. DOI: 10.1038/nrgastro.2014.46.
- ↑ Pentinmikko N, Iqbal S, Mana M, Andersson S, Cognetta AB, Suciu RM, Roper J, Luopajärvi K, Markelin E, Gopalakrishnan S, Smolander OP, Naranjo S, Saarinen T, Juuti A, Pietiläinen K, Auvinen P, Ristimäki A, Gupta N, Tammela T, Jacks T, Sabatini DM, Cravatt BF, Yilmaz ÖH, Katajisto P (July 2019). Notum produced by Paneth cells attenuates regeneration of aged intestinal epithelium. Nature 571 (7765): 398–402. PMID 31292548. PMC 8151802. DOI: 10.1038/s41586-019-1383-0.
- ↑ Podany AB, Wright J, Lamendella R, Soybel DI, Kelleher SL (May 2016). ZnT2-Mediated Zinc Import Into Paneth Cell Granules Is Necessary for Coordinated Secretion and Paneth Cell Function in Mice. Cellular and Molecular Gastroenterology and Hepatology 2 (3): 369–383. PMID 28174721. PMC 5042355. DOI: 10.1016/j.jcmgh.2015.12.006.
- ↑ Wallaeys C, Garcia-Gonzalez N, Libert C (February 2023). Paneth cells as the cornerstones of intestinal and organismal health: a primer. EMBO Molecular Medicine 15 (2): e16427. PMID 36573340. PMC 9906427. DOI: 10.15252/emmm.202216427.
- ↑ Zhong W, Wei X, Hao L, Lin TD, Yue R, Sun X, Guo W, Dong H, Li T, Ahmadi AR, Sun Z, Zhang Q, Zhao J, Zhou Z (May 2020). Paneth Cell Dysfunction Mediates Alcohol-related Steatohepatitis Through Promoting Bacterial Translocation in Mice: Role of Zinc Deficiency. Hepatology 71 (5): 1575–1591. PMID 31520476. PMC 7069794. DOI: 10.1002/hep.30945.
- ↑ Wehkamp J, Salzman NH, Porter E, Nuding S, Weichenthal M, Petras RE, Shen B, Schaeffeler E, Schwab M, Linzmeier R, Feathers RW, Chu H, Lima H, Fellermann K, Ganz T, Stange EF, Bevins CL (December 2005). Reduced Paneth cell alpha-defensins in ileal Crohn's disease. Proceedings of the National Academy of Sciences of the United States of America 102 (50): 18129–18134. PMID 16330776. PMC 1306791. DOI: 10.1073/pnas.0505256102.
- 1 2 Salzman NH, Bevins CL (November 2013). Dysbiosis--a consequence of Paneth cell dysfunction. Seminars in Immunology Microbiota and the immune system, an amazing mutualism forged by co-evolution 25 (5): 334–341. PMID 24239045. DOI: 10.1016/j.smim.2013.09.006.
- ↑ Liu TC, Gurram B, Baldridge MT, Head R, Lam V, Luo C, Cao Y, Simpson P, Hayward M, Holtz ML, Bousounis P, Noe J, Lerner D, Cabrera J, Biank V, Stephens M, Huttenhower C, McGovern DP, Xavier RJ, Stappenbeck TS, Salzman NH (June 2016). Paneth cell defects in Crohn's disease patients promote dysbiosis. JCI Insight 1 (8): e86907. PMID 27699268. PMC 5033844. DOI: 10.1172/jci.insight.86907.
- ↑ McElroy SJ, Weitkamp JH (September 2011). Innate Immunity in the Small Intestine of the Preterm Infant. NeoReviews 12 (9): e517–e526. PMID 22639551. PMC 3359837. DOI: 10.1542/neo.12-9-e517.
- ↑ Garabedian EM, Roberts LJ, McNevin MS, Gordon JI (September 1997). Examining the role of Paneth cells in the small intestine by lineage ablation in transgenic mice. The Journal of Biological Chemistry 272 (38): 23729–23740. PMID 9295317. DOI: 10.1074/jbc.272.38.23729.
- ↑ Niemarkt HJ, de Meij TG, van de Velde ME, van der Schee MP, van Goudoever JB, Kramer BW, Andriessen P, de Boer NK (February 2015). Necrotizing enterocolitis: a clinical review on diagnostic biomarkers and the role of the intestinal microbiota. Inflammatory Bowel Diseases 21 (2): 436–444. PMID 25268636. DOI: 10.1097/MIB.0000000000000184.
- ↑ Stappenbeck TS, McGovern DP (February 2017). Paneth Cell Alterations in the Development and Phenotype of Crohn's Disease. Gastroenterology 152 (2): 322–326. PMID 27729212. PMC 5209278. DOI: 10.1053/j.gastro.2016.10.003.
- ↑ Zhou H, Zhou SY, Gillilland M, Li JY, Lee A, Gao J, Zhang G, Xu X, Owyang C (October 2020). Bile acid toxicity in Paneth cells contributes to gut dysbiosis induced by high-fat feeding. JCI Insight 5 (20). PMID 33055426. PMC 7605541. DOI: 10.1172/jci.insight.138881.
- ↑ Nakamura S, Nakamura K, Yokoi Y, Shimizu Y, Ohira S, Hagiwara M, Song Z, Gan L, Aizawa T, Hashimoto D, Teshima T, Ouellette AJ, Ayabe T (March 2023). Decreased Paneth cell α-defensins promote fibrosis in a choline-deficient L-amino acid-defined high-fat diet-induced mouse model of nonalcoholic steatohepatitis via disrupting intestinal microbiota. Scientific Reports 13 (1): 3953. PMID 36894646. PMC 9998432. DOI: 10.1038/s41598-023-30997-y.
- ↑ Zhang S, Tun HM, Zhang D, Chau HT, Huang FY, Kwok H, Wong DK, Mak LY, Yuen MF, Seto WK (25 februari 2022). Alleviation of Hepatic Steatosis: Dithizone-Related Gut Microbiome Restoration During Paneth Cell Dysfunction. Frontiers in Microbiology 13: 813783. PMID 35283810. PMC 8914291. DOI: 10.3389/fmicb.2022.813783.
- bronvermelding
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Paneth cell op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.