Lineaire moleculaire geometrie
| Lineaire moleculaire geometrie | ||||
|---|---|---|---|---|
| Ruimtelijke structuur | ||||
 | ||||
Ruimtelijke schikking van de atomen | ||||
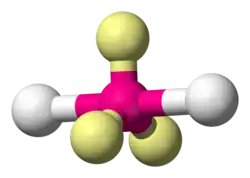 | ||||
■ vrije elektronenparen | ||||
| Eigenschappen | ||||
| Puntgroep | D∞h, C∞v | |||
| Bindende elektronenparen | 1 of 2 | |||
| Vrije elektronenparen | 0, 1 of 3 | |||
| Bindingshoeken | 180° | |||
| Coördinatiegetal | 2 | |||
| AXE-symbool | AX1E1, AX2E0 AX2E3 | |||
| ||||
In de scheikunde verwijst een lineaire moleculaire geometrie ernaar dat de atomen van een molecuul op één lijn liggen. Diatomische moleculen zoals koolstofmonoxide of waterstoffluoride zijn ipso facto lineair. Bij drie of meer atomen bedraagt de bindingshoek 180°. In lineaire organische verbindingen zoals ethyn (C2H2) en koolstofdioxide (CO2) zijn de atomen gewoonlijk sp-gehybridiseerd. Andere voorbeelden van lineaire verbindingen zijn waterstofcyanide (HCN), xenondifluoride (XeF2), carbonylsulfide (COS), de ionen azide (N3−), thiocyanaat (SCN−) en nitronium (NO2+). In de gasfase zijn berylliumfluoride (BeF2), berylliumchloride (BeCl2) en siliciumdioxide (SiO2) ook lineair. Twee voorbeelden van lineaire organometaalverbindingen zijn dimethylkwik en dimethylzink.
De puntgroepen van lineaire moleculen met een oneven aantal atomen, dus met een inversiecentrum, is D∞h en met een even aantal atomen C∞v. Die hebben geen inversiecentrum. Symmetrische moleculen, zoals koolstofdisulfide (CS2), zijn apolair en hun netto dipoolmoment is bijgevolg gelijk aan 0 D.