Hexamethylwolfraam
| Hexamethylwolfraam | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
 | ||||
 | ||||
Structuurparameters van W(CH3)6 | ||||
| Algemeen | ||||
| Chemische formule | C6H18W W(CH3)6 | |||
| Andere namen | wolfraamhexamethyl | |||
| SMILES | C[W](C)(C)(C)(C)(C)C | |||
| CAS-nummer | 36133-73-0 | |||
| Wikidata | Q2031142 | |||
| Beschrijving | rode kristallijne stof | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | rood | |||
| Sublimatiepunt | −30 °C | |||
| Goed oplosbaar in | n-pentaan, n-hexaan, benzeen, tolueen, di-ethylether, koolstofdisulfide, tetrachloormethaan | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Hexamethylwolfraam is de organowolfraamverbinding met als brutoformule W(CH3)6. Er treedt een directe binding op tussen koolstof en het metaal wolfraam, dus deze verbinding valt onder de organometaalverbindingen. W(CH3)6 is bij kamertemperatuur een rode kristallijne stof die gemakkelijk met lucht reageert, met zuurstof. De stof is zeer vluchtig en sublimeert al bij −30 °C. De zes methylgroepen zorgen voor een hydrofobe mantel, waardoor W(CH3)6 goed oplost in petroleum, alkanen, aromatische koolwaterstoffen, ethers, koolstofdisulfide en tetra.[1][2]
Synthese
Hexamethylwolfraam is voor het eerst in 1973 door Wilkinson en Shortland beschreven, die de reactie van methyllithium met wolfraam(VI)chloride in ether bestudeerden.[1] Het onderzoek naar deze reactie werd deels uitgevoerd in de hoop dat de octaëdrische complexen stablieler zouden blijken dan de thermisch instabiele tetraëdrische methylcomplexen van de overgangsmetalen. Wilkinson en Galyer beschreven in 1976 een verbeterde synthese waarbij trimethylaluminium, in combinatie met trimethylamine, als methylbron werd toegepast.[3] De verbeterde synthese verloopt volgens onderstaande reactievergelijking:
Behalve de twee eerder beschreven syntheses is later ook de synthese op basis van WCl6 of WF6 en dimethylzink beschreven:[4]
Moleculaire geometrie
Op het eerste gezicht lijkt de structuur eenvoudig: zes substituenten dus een molecuul in de vorm van een regelmatig achtvlak, maar W(CH3)6 blijkt een vervormd driehoekig prisma te zijn. Het molecuul heeft C3v symmetrie en staat in de onderste figuur rechts. Het driehoekige prisma is ongebruikelijk voor zes-gecoördineerde organometaalcomplexen. De valentiebindingstheorie en berekingen met de computer liggen er aan de basis van de structuurformule van hexamethylwolfraam te verklaren.[5][6]
In de eerste publicaties werden de resultaten van vooral de infraroodspectroscopie uitgelegd in het voordeel van de verwachte octaëdrische omringing van wolfraam door de methylgroepen en een studie in 1978, waarin fotoelektron spectroscopie werd toegepast, leek deze structuur te bevestigen.[7] Vanaf de eerste beschrijving in 1973 bleef het octaëdrische model onaangetast, totdat in 1989 door Morse en Girolami met behulp van röntgendiffractie werd aangetoond dat [Zr(CH3)6]2− een trigonaal prismatische structuur heeft. Er was voor 1989 geen aanleiding te denken dat de structuur van ML6 geen octaëdrische verbinding was, maar nieuwe gegevens en verbeterde analytische methoden suggereerden het bestaan van uitzonderingen op de regel en W(CH3)6 bleek daar een van. [8]
Morse en Girolami voorspelden aan de hand van deze door hen bestudeerde verbinding dat andere d0 ML6 verbindingen zoals de, soms negatief geladen, hexamethylcomplexen niobium Nb(CH3)6−, tantaal Ta(CH3)6− en W(CH3)6 dezelfde structuur met een driehoekig prisma hebben. Deze voorspelling werd bevestigd, waarbij van elektronendiffractie gebruik werd gemaakt met het medium in de gasfase. Het prisma is vervormd, wat blijkt uit het ontbreken van de D3h of C3v symmetrie.[9] De onderzoeksgroep rond Seppelt kon in 1996 met röntgendiffractie aan een eenkristal aantonen dat er in de structuur van W(CH3)6 vervormde driehoekige prisma's voorkomen.[4][10]
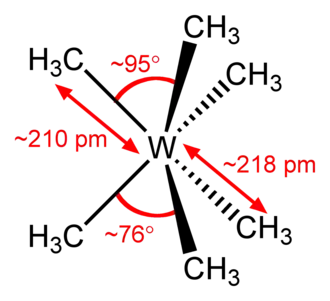
De parameters die door Seppelt et al zijn gemeten staan in de tweede figuur. De symmetrie van het driehoekige prisma D3h is vervormd door het meer openvouwen van het ene, bovenste drietal methylgroepen. De hoek C-W-C bedraagt 94 tot 97° en de koolstof-wolfraambindingen zijn iets korter. Het andere, onderste drietal heeft kleinere bindingshoeken van 75-78° in combinatie met een iets langere binding. De afwijking van de verwachte octaëdrische structuur kan aan een tweede orde Jahn-Teller-effect worden toegeschreven.[11][12]
Reactiviteit
Hexamethylwolfraam ontleedt bij kamertemperatuur, waarbij methaan en sporen ethaan ontstaan. Het zwarte residu bevat polymethyleen en wolfraam, hoewel de vorming van metallisch wolfraam uit W(CH3)6 zeer onwaarschijnlijk is.
Zoals veel complementariteit, is ook WMe6 niet tegen zuurstof bestand. Op vergelijkbare wijze geeft de reactie met zuren aanleiding tot het vrijmaken van methaan en ongedefinieerde substanties waarin wolfraam voorkomt. Met halogenen ontstaan de monohalomethanen in combinatie met wolfraamhalogenides.
Overige
In 1991 is een patent aangevraagd waarbij W(CH3)6 werd toegepast als bron van wolfraam in de chemical vapor deposition.[13] Hoewel het principe van deze techniek wel wordt toegepast in de fabricage van halfgeleiders worden daarvoor wolfraam(VI)chloride en waterstof gebruikt.[14]
Als gevolg van het werken met W(CH3)6 is een aantal ernstige explosies opgetreden. Zelfs het weghalen van lucht, van alle zuurstof uit de omgeving bood geen voldoende bescherming.[7][15]
Voorbeelden
Vervormd driehoekig prisma
Andere verbindingen met de structuur van een vervormd driehoekig prisma zijn onder andere:
- MoMe6
- [NbMe6]−
- [TaPh6]−, Ph = fenyl
Dit zijn alle drie complexen van het type d0.
Regelmatige structuur van een driehoekig prisma
Regelmatige driehoekige prisma's met D3h symmetrie worden onder andere aangetroffen in:
- ReMe6, d1
- [TaMe6]−, d0
- [ZrMe6]2−, d0[16]
- 1 2 A.J. Shortland, G. Wilkinson. (1973). Preparation and properties of hexamethyltungsten J.Chem.Soc.,Dalton Trans.. 1973 (8): pag.: 872–876 DOI:10.1039/DT9730000872
- ↑ A. Koutsospyros, W. Braida, C. Christodoulatos, D. Dermatas, N. Strigul. (2006). A review of tungsten: From environmental obscurity to scrutiny Journal of Hazardous Materials. 136 (1): pag.: 1–19 DOI:10.1016/j.jhazmat.2005.11.007
- ↑ A.L. Galyer, G. Wilkinson. New synthesis of hexamethyltungsten(VI). The octamethyltungstate-(VI) lon J.Chem.Soc., Dalton Trans.. 1976 (21): pag.: 2235 DOI:10.1039/DT9760002235
- 1 2 S. Kleinhenz, V. Pfennig, K. Seppelt, K.. (1998). Preparation and Structures of [W(CH3)6], [Re(CH3)6], [Nb(CH3)6]−, and [Ta(CH3)6]− Chem.Eur.J.. 4 (9): pag.: 1687
- ↑ C.K. Landis, T. Cleveland, T.K. Firman. (1995). Making sense of the shapes of simple metal hydrides J.Amer.Chem.Soc.. 117 (6): pag.: 1859–1860 DOI:10.1021/ja00111a036
- ↑ C.K. Landis, T. Cleveland, T.K. Firman. (1996). Structure of W(CH3)6 Science. 272 (5259): pag.: 182–183 DOI:10.1126/science.272.5259.182b
- 1 2 J.C. Green, D.R. Lloyd, L. Galyer, K. Mertis, G. Wilkinson, G.. Photoelectron spectra of some transition metal alkyls and oxoalkyls J.Chem.Soc.Dalton Trans.. 1978 (10): pag.: 1403 DOI:10.1039/DT9780001403
- ↑ P.M. Morse, G.S. Girolami. (1989). Are d0 ML6 complexes always octahedral? The x-ray structure of trigonal-prismatic [Li(tmed)]2[ZrMe6] J.Amer.Chem.Soc.. 111 (11): pag.: 4114 DOI:10.1021/ja00193a061
- ↑ A. Haalan, A. Hammel, K. Rydpal, H.V. Volden. (1990). The coordination geometry of gaseous hexamethyltungsten is not octahedral J.Amer.Chem.Soc.. 112 (11): pag.: 4547–4549 DOI:10.1021/ja00167a065
- ↑ K. Seppelt, V. Pfennig. (1996). Crystal and Molecular Structures of Hexamethyltungsten and Hexamethylrhenium Science. 271 (5249): pag.: 626 DOI:10.1126/science.271.5249.626
- ↑ K. Seppelt. (2003). Nonoctahedral Structures Accounts of Chemical Research. 36 (2): pag.: 147–153 DOI:10.1021/ar020052o
- ↑ M. Kaupp. (1998). The Nonoctahedral Structures of d0, d1, and d2 Hexamethyl Complexes Chemistry - A European Journal. 4 (9): pag.: 1678–1686
- ↑ S. Matsumoto, O. Ikeda, K. Ohmi. (1991). GEEN TITEL OPGEGEVEN Eur.Pat.Appl..
- ↑ R.U. Kirss, L. Meda. (1998). Chemical vapor deposition of tungsten oxide Applied Organometallic Chemistry. 12 (3): pag.: 155–160
- ↑ K. Mertis, L. Galyer, G. Wilkinson. (1975). Permethyls of tantalum, tungsten and rhenium: a warning J. Organometallic Chemistry. 97 (3): pag.: C65 DOI:10.1016/S0022-328X(00)89324-9
- ↑ C.R. Housecroft, A.G. Sharpe. (2004). Inorganic Chemistry (2nd ed.) – Prentice Hall ISBN 978-0130399137