Donor-acceptorbinding
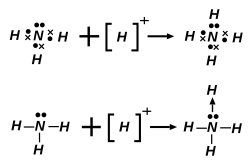
Een donor-acceptorbinding, ook wel datieve binding, coördinatief-covalente binding, semipolaire binding of dipolaire binding genoemd, is een speciaal type covalente binding waarbij de beide elektronen die deel uitmaken van een gemeenschappelijk elektronenpaar bij hetzelfde atoom horen. Nadat op deze manier bindingen zijn gevormd, zijn deze even sterk en hebben dezelfde eigenschappen als gewone polaire covalente bindingen. Het onderscheid met andere covalente bindingen is kunstmatig, de terminologie wordt vooral gebruikt bij het beschrijven van coördinatieverbindingen.
Donor-acceptorbindingen treden op wanneer een lewisbase een elektronenpaar levert aan een lewiszuur, waardoor een zogeheten adduct ontstaat. Het vormingsproces van de datieve binding heet coördinatie. De elektronendonor krijgt hierbij een positieve formele lading, terwijl de elektronenacceptor een negatieve formele lading krijgt.
Elke chemische verbinding die een vrij elektronenpaar bevat kan een donor-acceptorbinding aangaan. De binding die zo ontstaat wordt ook wel coördinatief-covalente binding genoemd.
Bij de vorming van een donor-acceptorbinding fungeert het lewiszuur als elektronenacceptor (het heeft een lege orbitaal die elektronen kan opnemen), terwijl de lewisbase de elektronenpaar-donor is. Wanneer het elektronenpaar gedeeld wordt, ontstaat er een nieuwe σ-binding, net als bij een gewone covalente binding.
Een typisch voorbeeld hiervan is de vorming van ammonium (NH4+) uit ammoniak (NH3) en een proton (H+):
NH3 + H+ → NH4+
In dit geval levert het stikstofatoom van NH3 een vrij elektronenpaar aan het proton. Nadat de binding is gevormd, zijn alle vier N–H-bindingen equivalent, ondanks dat één ervan oorspronkelijk via een donor-acceptormechanisme tot stand kwam. Een ander belangrijk voorbeeld is te vinden in complexverbindingen van overgangsmetalen. Zo vormt het hexa-aquakoper(II)-ion [Cu(OH2)6]2+ door coördinatie van zes watermoleculen aan een Cu2+-ion. Elk watermolecuul treedt op als ligand en doneert een vrij elektronenpaar van het zuurstofatoom aan het metaalion:
Cu2+ + 6 H2O → [Cu(OH2)6]2+
De bindingen tussen Cu2+ en de waterliganden zijn dus donor-acceptorbindingen.
Donor-acceptorbindingen spelen een sleutelrol in:
- Complexchemie (zoals bij metaalionen en liganden)
- Zuurbasereacties volgens Lewis
- Moleculaire orbitalentheorie, waarin elektronenparen worden gedeeld tussen een donor en een acceptor
- Biologische systemen, bijvoorbeeld bij metalloproteïnen of enzymen die metaalionen bevatten
Hoewel donor-acceptorbindingen conceptueel verschillen van gewone covalente bindingen, zijn ze structureel en energetisch gelijkwaardig nadat ze zijn gevormd. Het onderscheid wordt dus vooral gebruikt om het vormingstraject van de binding te beschrijven, niet de uiteindelijke binding zelf.
Voorbeeld
- Koolstofmonoxide bevat één coördinatieve binding en twee gewone covalente bindingen tussen het zuurstofatoom en het koolstofatoom. Dit komt erop neer dat koolstof de elektronenacceptor en zuurstof de elektronendonor is.