Cyclobutadieen
| Cyclobutadieen | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
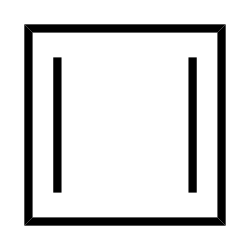 | ||||
Structuurformule van cyclobutadieen | ||||
| Algemeen | ||||
| Chemische formule | C4H4 | |||
| IUPAC-naam | 1,3-cyclobutadieen | |||
| Andere namen | [4]annuleen | |||
| Molaire massa | 52,07456 g/mol | |||
| SMILES | C1=CC=C1 | |||
| InChI | 1S/C4H4/c1-2-4-3-1/h1-4H | |||
| CAS-nummer | 1120-53-2 | |||
| PubChem | 136879 | |||
| Wikidata | Q415302 | |||
| ||||
Cyclobutadieen is een organische verbinding met als brutoformule C4H4. Het is het kleinste annuleen, namelijk [4]-annuleen. Cyclobutadieen is een zeer instabiele koolwaterstof: in de vrije toestand heeft het een levensduur van nog geen 5 seconden. Het tetra-tert-butylderivaat is wel stabiel genoeg.
Synthese
De structuurformule van cyclobutadieen lijkt eenvoudig, maar verscheidene scheikundigen hebben tevergeefs geprobeerd de stof te bereiden. Het lukte Pettit in 1965, onderzoeker aan de Universiteit van Texas, de stof aantoonbaar te maken, hoewel isolatie nog niet lukte. Cyclobutadieen kan worden bereid door het ontleden van een cyclobutadieen-metaal-verbinding: cyclobutadieen komt met behulp van ammoniumcerium(IV)nitraat bij de ontleding van het ijzer-carbonylcomplex C4H4Fe(CO)3 vrij. Dit cyclobutadieen-ijzer-tricarbonylcomplex wordt bereid uit Fe4(CO)9 en cis-3,4,-dichloorcyclobuteen via een dubbele dehydrohalogenering.[1][2] Als cyclobutadieen uit het ijzercomplex vrijkomt reageert het gemakkelijk met elektrondeficiënte alkynen, waarbij een dewarbenzeen wordt gevormd:[3]
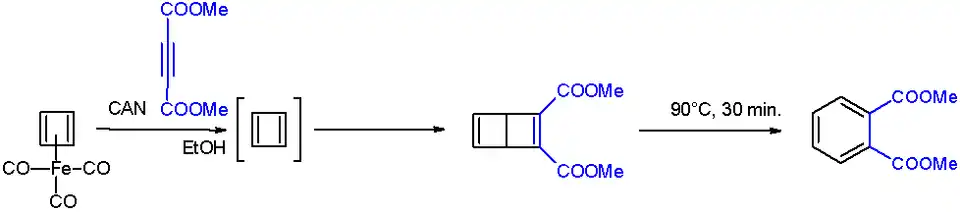
Omzetting van cyclobutadieen naar dewarbenzeen
Bij verwarming tot 90°C wordt het dewarbenzeen omgezet naar een benzeenderivaat. Welke verbinding hier wordt gevormd hangt van het gebruikte alkyn af: zo wordt met dimethylacetyleendicarboxylaat dimethylftalaat gevormd.
Derivaten
Een fenyl-derivaat van cyclobutadieen kan gesynthetiseerd worden door een [2+2]-cycloadditie, uitgevoerd met een di-alkyn. Het cyclobutadieen zelf is ook weer niet isoleerbaar, maar kan via een diels-alderreactie met tetrafenylcyclopentadienon worden afgevangen. Nadat het ontstane adduct een equivalent koolstofmonoxide heeft afgegeven, ontstaat een derivaat van cyclo-octatetraëen:[4]
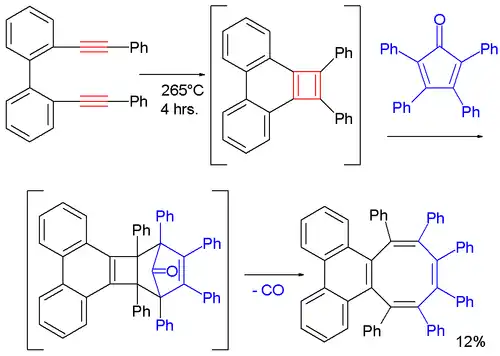
Cycloadditie van twee alkynen ter synthese van een fenylcyclobutadieenderivaat
Structuur en eigenschappen
Cyclobutadieen bezit, zoals met infraroodspectrometrie is aangetoond, een rechthoekige vorm. Deze vorm staat in contrast met het vierkant dat door een eenvoudige toepassing van de benadering van Hückel wordt voorspeld. Deze afwijkende vorm wordt door het Jahn-Teller-effect verklaard. Hoewel het, net zoals benzeen, is opgebouwd uit een afwisseling van enkele en dubbele bindingen, voldoet het niet aan de regel van Hückel. Meer nog: het aantal π-elektronen bedraagt 4, waardoor cyclobutadieen als anti-aromatisch wordt bestempeld. Sommige cyclobutaan-metaalcomplexen zijn stabiel, omdat het metaal twee extra elektronen in het systeem kan brengen, waardoor het wel aromatisch wordt.
Studies hebben aangetoond dat de dubbele bindingen gelokaliseerd zijn en niet met de benadering van Hückel kunnen worden beschreven. De instabiliteit van de verbinding wordt nog eens onderstreept door het feit dat zelfs bij een temperatuur van 35 kelvin nog dimerisatie optreedt via een diels-alderreactie. Het monomeer is bij hogere temperaturen bestudeerd door het te isoleren in een matrix van edelgas.
Cyclobutadieen is geen heterocyclische verbinding.
- ↑ GF Emerson, L Watts en R Pettit. Cyclobutadiene- and Benzocyclobutadiene-Iron Tricarbonyl Complexes, 1965. in Journal of the American Chemical Society 87, 1, blz 131-133
- ↑ R Pettit en J Henery. Cyclobutadieneiron tricarbonyl, 1970. in Organic Syntheses 50, blz 21. Gearchiveerd op 4 november 2020.
- ↑ L Watts, JD Fitzpatrick en R Pettit. Cyclobutadiene, 1965. in Journal of the American Chemical Society 87, 14, blz 3253-3254
- ↑ C-C Lee, M-K Leung, G-H Lee, Y-H Liu en S-M Peng, Revisit of the Dessy-White Intramolecular Acetylene-Acetylene [2+2]-Cycloadditions, 2006. in Journal of Organic Chemistry 71, 22, blz 8417-8423