Cupraat
Cupraten (van Latijn cuprum = koper[1]) zijn chemische verbindingen (zouten) die koper bevatten en waarin het koperatoom het centrale atoom is in een verder negatief geladen samengesteld ion.
Gebruik
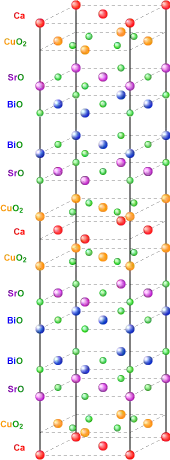
Cupraten zijn al eeuwenlang bekend en worden gebruikt in de organische en anorganische chemie. Nochtans is de belangstelling ervoor beduidend gestegen sinds 1986 na de ontdekking van supergeleiding op relatief hoge temperatuur in een lanthaan-barium-koperoxide door Georg Bednorz en Alex Müller. Tussen 1986 en 2001 werden meer dan 100.000 wetenschappelijke documenten over supergeleiding in cupraten gepubliceerd. Bednorz en Müller wonnen de Nobelprijs voor Natuurkunde slechts een jaar na hun ontdekking. Vanaf 1986 waren bijna alle bekende hogetemperatuursupergeleiders cupraatsupergeleiders.
Terminologie
In de IUPAC-nomenclatuur (IUPAC Red Book ed. 2005)[2] spreekt men van een cupraat wanneer koper het centraal atoom in een complex anion is. Een voorbeeld is amminepentachloridocupraat(II) [CuCl5(NH3)]2−. Wanneer de elektrische lading van het complex neutraal of positief is, spreekt men van kopercomplexen, niet van cupraten. Bijvoorbeeld tetra-amminekoper(II)chloride [Cu(NH3)4]Cl2, waar het kopercomplex het kation is, en niet het anion.
In oudere nomenclatuur werd een verbinding een cupraat genoemd wanneer deze koper bevat in zijn hoogste oxidatietoestand 2+ of hoger. Voor een verbinding waar koper het oxidatiegetal 1+ bezit, sprak men dan niet van cupraten maar van cuprieten, welke momenteel de aanduiding cupraat(I) krijgen. De naam cupriet wordt wel nog gebruikt voor een mineraal dat een koper(I)oxide is. In zgn. cupraatsupergeleiders is er meestal sprake van deels koper(II) en deels koper(III).
Anorganische cupraten
.png)
Cupraatanionen vormen complexe negatief geladen ionen met liganden zoals cyanide, hydroxide of halogeniden. Typische voorbeelden van deze complexen zijn tetracyanidocupraat(I) [Cu(CN)4]3−, tetrachloridocupraat(II) [CuCl4]2− en hexahydroxidocupraat(II) [Cu(OH)6]4−. Er zijn ook zeldzame koper(III)- en koper(IV)-complexen zoals hexafluoridocupraat(III) [CuF6]3− of hexafluoridocupraat(IV) [CuF6]2−. Dit zijn sterk oxiderende reagentia.
Terwijl tetracyanidocupraat(I) [Cu(CN)4]3− kleurloos is, zijn de meeste andere koper(I)-complexen roodbruin; koper(II)-complexen hebben een intense turkooisblauwe kleur, terwijl koper(III)- en koper(IV)-complexen oranjerood zijn. Lithiumtetrachloridocupraat(II) (Li2[CuCl4]) is een efficiënte katalysator voor de koppelingen van alkylhalogeniden in de grignardreactie. Het wordt bereid door lithiumchloride (LiCl) en koper(II)chloride (CuCl2) door tetrahydrofuraan te mengen. Wanneer koper(II)hydroxide wordt verhit met natriumhydoxide ontstaat natriumtetrahydroxidocupraat(II):[3]
- Cu(OH)2 + 2 NaOH → Na2Cu(OH)4
Organische cupraten
.png)
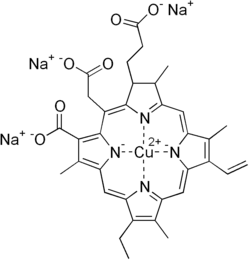
Cupraten spelen een grote rol in de organische chemie. De eerste organische koperverbinding, het explosieve koper(I)acetylide Cu2C2, werd door Rudolf Christian Böttger in 1859 bereid.
Organische cupraten bevatten gewoonlijk een groep R2Cu, waarbij R een koolstof bevattende eenheid is. Ze reageren met zuurstof en water en vormen daarbij koper(I)oxide; zij zijn over het algemeen onoplosbaar in inerte oplosmiddelen, ze hebben de neiging om onstabiel te zijn bij bepaalde temperaturen en ze zijn moeilijk te hanteren. Niettemin worden organische koperreagentia vaak in de organische chemie gebruikt als alkylatiereagentia die ter plaatse in een inert milieu worden bereid.
Zie ook: Organokoperchemie
- ↑ Lewis, C.T. & Short, C. (1879). A Latin dictionary founded on Andrews' edition of Freund's Latin dictionary. Oxford: Clarendon Press.
- ↑ Nomenclature of inorganic chemistry: IUPAC recommendations 2005. Royal society of chemistry, Cambridge (2005). ISBN 978-0-85404-438-2.
- ↑ (en) Tetrahydroxycuprate in de Big Chemical Encyclopedia. Gearchiveerd op 18 juni 2023.