Western blot
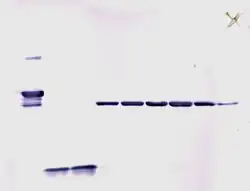
De western blot of immunoblot is een analytische techniek in de moleculaire biologie en biochemie waarmee men heel specifiek de aanwezigheid van een bepaald eiwit kan aantonen. Het is een detectiemethode die gebruikt wordt om één of verschillende eiwitten in een complex eiwitmengsel – zoals een cellysaat of weefselextract – zichtbaar te maken. Het is een standaardtechniek in biochemisch onderzoek.
Het uitvoeren van een western blot gaat volgens een vast aantal stappen. Eerst worden de eiwitten in het mengsel op grootte gescheiden door middel van gelelektroforese, veelal SDS-PAGE. Dan worden de gescheiden eiwitten van de gel via een tweede elektroforese overgebracht naar een eiwithechtend membraan (blotting). Ten slotte wordt dit membraan geweekt in een oplossing met antilichamen die specifiek aan het eiwit van interesse binden. De antilichamen kunnen zichtbaar gemaakt worden, bijvoorbeeld via fluorescentie.
De western blot is zeer gevoelig: het kan 1 nanogram of zelfs minder van een specifiek eiwit aantonen. De techniek is nuttig als men wil weten hoe de expressie van een eiwit verandert onder verschillende omstandigheden. Hoewel men door de dikte van de band een idee kan krijgen van de hoeveelheid eiwit in het onderzoeksmonster, zijn western blots meestal ongeschikt om een precieze kwantificatie van het aangetoonde eiwit te geven. Daarvoor wordt vaak gebruik gemaakt van een verwante techniek, de ELISA.
Geschiedenis
De naam western blot is een woordspeling op Southern blot, een verwante techniek waarmee men geen eiwitten, maar DNA-moleculen zichtbaar maakt. De Southern blot is vernoemd naar de Engelse bioloog Edwin Southern, die de techniek ontwikkelde. De term 'western blot' werd voor het eerst gegeven in 1981 door W. Neal Burnette,[1] hoewel de techniek zelf al in 1979 werd ontwikkeld door een onderzoeksteam aan Stanford University, en onafhankelijk door een ander team in het Friedrich Miescher Instituut in Bazel, Zwitserland.[2] Deze laatste groep maakte gebruikt van secundaire antilichamen voor detectie, wat al sterk lijkt op de moderne western blot-methode die tegenwoordig bijna universeel wordt gebruikt. Tussen 1979 en 2019 werd de techniek gebruikt in meer dan 400.000 publicaties op PubMed.[2] Het is een van de belangrijkste analytische technieken in de biochemie en moleculaire biologie.
Werking
Elektroforese

De eerste stap van een Western blot is de scheiding van het eiwitmengsel door middel van gelelektroforese. Het doel hiervan is om de complexe mix van eiwitten uiteen te splitsen in goed gedefinieerde bandjes, zodat ze later specifiek gedetecteerd kunnen worden.
De eiwitsamples worden hiervoor in een gel geladen, in kleine welletjes. Tijdens de elektroforese migreren de eiwitten door een dragermatrix – meestal polyacrylamide – onder invloed van een elektrisch veld. Polyacrylamide gedraagt zich als een moleculaire zeef, waarbij de poriegrootte kan worden aangepast door de concentratie acrylamide te variëren. Gels met een laag percentage worden gebruikt om grote eiwitten te scheiden, gels met een hoog percentage zijn geschikt voor kleinere eiwitten.
Er bestaan meerdere vormen van eiwit-elektroforese, zoals Native-PAGE en iso-elektrische focussering, maar in de context van Western blotting is SDS-PAGE veruit de meest gebruikte methode. Bij SDS-PAGE worden eiwitten vóór het laden gemengd met een buffer die het detergens SDS bevat. Deze zeepachtige stof denatureert de eiwitten en vouwt ze open tot lineaire polypeptiden. SDS maakt de eiwitketens daarnaast negatief geladen. Het gevolg is dat de migratie tijdens de elektroforese vrijwel uitsluitend wordt bepaald door het moleculair gewicht: kleinere polypeptiden bewegen sneller door de gel richting de positieve pool.
Blotting
De gescheiden eiwitbanden worden vervolgens overgebracht van de gel naar een vast draagmembraan. Het membraan bestaat meestal uit nitrocellulose of PVDF; materialen met een hoge affiniteit voor eiwit. De overdracht van eiwitbandjes naar het membraan vindt plaats onder invloed van een elektrische stroom, en wordt 'blotting' of transfer genoemd. De reden dat men deze stap uitvoert, is omdat de eiwitbandjes in een membraan makkelijk toegankelijk zijn voor (detecterende) antilichamen. Een gel is hier te dik voor; de antilichamen kunnen niet door de gelmatrix heen.
Blotting gebeurt vaak in een aparte transfer-tank of in een gespecialiseerd systeem (semi-dry transfer). Het membraan – dat dezelfde lengte en breedte heeft als de gel – wordt over de gel heen gelegd, en beide zijden worden afdekt met filterpapier en een spons. Belangrijk hierbij is dat het membraan tussen de gel en de positief geladen anode ligt, dit is immers de richting waarin de eiwitbandjes zich zullen bewegen. Het stapeltje wordt in het overdrachtssysteem geplaatst en gedurende een bepaalde tijdsperiode aan elektrische stroom aangesloten. Na een uur zijn alle eiwitten van de gel in het membraan gedreven en gehecht.
Detectie

Het eiwit waarin men geïnteresseerd is kan gedetecteerd worden met een voor dat eiwit specifiek antilichaam. In de moderne biochemie wordt het eiwit van interesse meestal gedetecteerd via een tweestapsdetectie met behulp van een primair en een secundair antilichaam. Het primaire antilichaam herkent een specifieke epitoop op het eiwit (dit kan een natuurlijk voorkomend deel van het eiwit zijn, of een toegevoegde eiwit-tag). Het primaire antilichaam bindt specifiek aan deze epitoop op de blot.
Na incubatie met het primaire antilichaam wordt de blot gewassen om niet-specifieke bindingen te verwijderen. Vervolgens wordt een secundair antilichaam toegevoegd dat specifiek gericht is tegen het primaire antilichaam. Dit secundaire antilichaam is meestal afkomstig van een andere diersoort (bijvoorbeeld geit-anti-muis als het primaire antilichaam uit muis komt), en bindt aan de constante regio van het primaire antilichaam.
Het secundaire antilichaam is gelabeld met een detecteerbare groep, zoals een enzym – bijvoorbeeld horseradish peroxidase (HRP) of alkalische fosfatase (AP) – of een fluorofoor. Wanneer een geschikt substraat wordt toegevoegd, produceert het enzym een kleurreactie (chemiluminescentie), of in het geval van een fluorofoor kan het eiwit direct worden gevisualiseerd met behulp van fluorescentieapparatuur. De blot wordt in een geschikt detectiesysteem ontwikkeld.
Detectie-tags
Als men een bekend eiwit van interesse wilt visualiseren door middel van western blot, wordt het eiwit vaak uitgerust met een eiwit-tag. Hierbij wordt op DNA-niveau een specifieke aminozuursequentie (meestal 6–20 aminozuren) toegevoegd aan het uiteinde van het eiwit, dat daardoor zeer efficiënt herkend kan worden door een antilichaam. Voorbeelden zijn FLAG-tags, HA-tags en Myc-tags.
Zie ook
Bronnen
- (en) Alberts, B. (2022). Molecular Biology of The Cell, 7th. W.W. Norton & Company, p. 490. ISBN 978-0-393-42708-0.
- ↑ (en) Burnette WN. (1981). "Western blotting": electrophoretic transfer of proteins from polyacrylamide gels to unmodified nitrocellulose and radiographic detection with antibody. Analytical Biochemistry 112. DOI: 10.1016/0003-2697(81)90281-5.
- 1 2 (en) Moritz, CP. (2020). 40 years Western blotting: a scientific birthday toast. Journal of Proteomics. DOI: 10.1016/j.jprot.2019.103575.