Hemangioblast

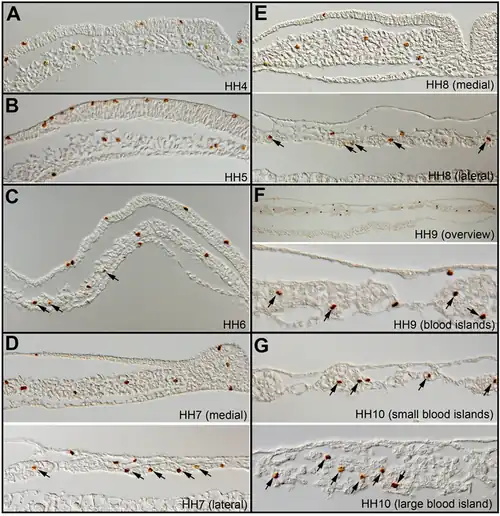
Hemangioblasten zijn de multipotente voorlopercellen die kunnen differentiëren tot angioblasten, hematopoëtische en endotheelcellen.[1][2][3] In het muizenembryo markeert het ontstaan van bloedeilandjes in de dooierzak op embryonale dag 7 het begin van de hematopoëse. Vanuit deze bloedeilandjes worden kort daarna de hematopoëtische cellen en bloedvaten gevormd. Bloedeilanden zijn structuren rond het zich ontwikkelende embryo die naar verschillende delen van de bloedsomloop leiden. Bloedeilandjes ontstaan buiten het zich ontwikkelende embryo op de dooierzak, allantois, hechtsteel en chorion.
Hemangioblasten zijn de voorlopercellen die de bloedeilandjes vormen. Tot op heden is de hemangioblast geïdentificeerd in embryo's van mensen, muizen en zebravissen[4].
Hemangioblasten zijn eerst uit embryonale culturen geëxtraheerd en met cytokines gemanipuleerd om te differentiëren langs hematopoëtische of endothele weg. Het is aangetoond dat deze pre-endothele/pre-hematopoëtische cellen in het embryo voortkomen uit een fenotype CD34-populatie. Vervolgens werd ontdekt dat hemangioblasten ook aanwezig zijn in het weefsel van postnatale individuen, zoals pasgeborenen en volwassenen.
Er zijn nu steeds meer aanwijzingen dat hemangioblasten bij volwassenen blijven bestaan als circulerende stamcellen in het perifeer bloed, die zowel endotheelcellen als hematopoëtische cellen kunnen vormen. Men denkt dat deze cellen zowel CD34 als CD133 tot expressie brengen.[5] Deze cellen zijn waarschijnlijk afkomstig uit het beenmerg en mogelijk zelfs uit hematopoëtische stamcellen.
Geschiedenis
De hypothese van een hemangioblast werd voor het eerst voorgesteld in 1900 door Wilhelm His. Het bestaan van de hemangioblast werd voor het eerst voorgesteld in 1917 door Florence Sabin, die de nauwe ruimtelijke en temporele nabijheid observeerde van de ontwikkeling van bloedvaten en rode bloedcellen in de dooierzak van kippenembryo's.[6] In 1932 bedacht Murray, met dezelfde observatie als Sabin, de term "hemangioblast".[7]
De hypothese van een bipotente voorloper werd verder ondersteund door het feit dat endotheelcellen en hematopoëtische cellen veel van dezelfde markers delen, waaronder Flk1, Vegf, CD34, Scl, Gata2, Runx1 en Pecam-1. Bovendien werd aangetoond dat zonder Flk1 in het zich ontwikkelende embryo resulteert in het verdwijnen van zowel hematopoëtische cellen als endotheelcellen.[8]
In 1997 isoleerde Kennedy van het Keller Lab voor het eerst het in-vitro-equivalent van de hemangioblast. Deze cellen werden blastkolonievormende cellen (BL-CFC) genoemd. Met behulp van aggregaten van differentiërende embryonale stamcellen van muizen, embryoïde lichamen genaamd, plaatsten de auteurs cellen in de differentiatietijdlijn vlak vóór het ontstaan van hematopoëtische cellen. In aanwezigheid van de juiste cytokinen kon een subset van deze cellen differentiëren tot hematopoëtische cellen.[9] Bovendien kunnen deze cellen ook differentiëren tot endotheelcellen, zoals aangetoond door Choi van het Keller Lab.[10]
In 2004 werden hemangioblasten geïsoleerd in het muizenembryo door Huber van het Keller Lab. Ze zijn afkomstig van het achterste primitieve streepgebied van het mesoderm tijdens de gastrulatie. Door gebruik te maken van verdunningsklonering hebben de auteurs aangetoond dat de resulterende hematopoëtische en endotheelcellen inderdaad van klonale oorsprong waren, wat bewijst dat ze de hemangioblast succesvol hebben geïsoleerd in het zich ontwikkelende embryo.[11] Verdunningsklonering[12][13] beschrijft een procedure om een monoklonale celpopulatie te verkrijgen uitgaande van een polyklonale celmassa. Dit wordt bereikt door een reeks toenemende verdunningen van de oorspronkelijke (polyklonale) celcultuur op te zetten.
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Hemangioblast op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- ↑ Basak GW, Yasukawa S, Alfaro A, etal (2009). Human embryonic stem cells hemangioblast express HLA-antigens. J Transl Med 7 (1): 27. PMID 19386101. PMC 2680830. DOI: 10.1186/1479-5876-7-27.
- ↑ Miki Takeuchi, Yuji Fusei, Mana Watanabe (2015). LSD1/KDM1A promotes hematopoietic commitment of hemangioblasts through downregulation of Etv2. Proceedings of the National Academy of Sciences of the United States of America 112 (45): 13922–13927. PMID 26512114. PMC 4653156. DOI: 10.1073/pnas.1517326112.
- ↑ MeSH Hemangioblasts
- ↑ Vogeli KM, Jin SW, Martin GR, Stainier DY (September 2006). A common progenitor for haematopoietic and endothelial lineages in the zebrafish gastrula. Nature 443 (7109): 337–9. PMID 16988712. DOI: 10.1038/nature05045.
- ↑ Loges S, etal (2004). Identification of the Adult Hemangioblast. Stem Cells and Development 13 (1): 229–42. PMID 15186719. DOI: 10.1089/154732804323099163.
- ↑ Sabin F (2002). Preliminary note on the differentiation of angioblasts and the method by which they produce blood-vessels, blood-plasma and red blood-cells as seen in the living chick (1917). J Hematother Stem Cell Res 11 (1): 5–7. PMID 11846999. DOI: 10.1089/152581602753448496.
- ↑ Murray PDF (1932). The development in vitro of the blood of early chick embryo.. Proceedings of the Royal Society 111 (773): 497–521. DOI: 10.1098/rspb.1932.0070.
- ↑ Zambidis ET, Park TS, Yu W, etal (2008). Expression of angiotensin-converting enzyme (CD143) identifies and regulates primitive hemangioblasts derived from human pluripotent stem cells. Blood 112 (9): 3601–14. PMID 18728246. PMC 2572789. DOI: 10.1182/blood-2008-03-144766.
- ↑ Kennedy M, Firpo M, Choi K, Wall C, Robertson S, Kabrun N, Keller GA (1997). A common precursor for primitive erythropoisis and definitive hematopoiesis. Nature 386 (6624): 488–93. PMID 9087406. DOI: 10.1038/386488a0.
- ↑ Choi K, Kennedy M, Kazarov A, etal (1998). A common precursor for hematopoietic and endothelial cells. Development 125 (4): 725–32. PMID 9435292. DOI: 10.1242/dev.125.4.725.
- ↑ Huber TL, Kouskoff V, Fehling HJ, Palis J, Keller G (2004). Haemangioblast commitment is initiated in the primitive streak of the mouse embryo. Nature 432 (7017): 625–30. PMID 15577911. DOI: 10.1038/nature03122.
- ↑ Freshney, R. Ian (2010). Culture of animal cells : a manual of basic technique and specialized applications, 6th. Wiley-Blackwell, Hoboken, N.J., 208–211. ISBN 9780470528129.
- ↑ Animal cell culture: Essential Methods.