Hartspiercel
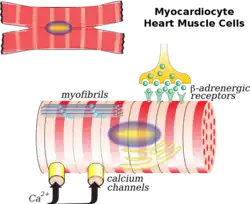


Hartspiercellen of cardiomyocyten zijn de contractiele spiercellen van de hartspier. De cellen worden omgeven door een extracellulaire matrix, geproduceerd door ondersteunende fibroblasten. Hartspiercellen bevatten veel mitochondriën, die de benodigde energie leveren in de vorm van adenosinetrifosfaat (ATP), waardoor ze zeer goed bestand zijn tegen vermoeidheid.[1] [2] Er worden door middel van gap junctions in de lengterichting actiepotentialen doorgegeven. In de breedterichting (transversaal) zorgen banddesmosomen en desmosomen voor de aanhechtingsplaten die te zien zijn in een microscoop. In de lichtmicroscoop ontstaat een trappatroon. Dit zijn plaatsen waar twee hartspiercellen samengehecht zijn. De desmosomen zorgen dat de spiercellen niet loskomen van elkaar.
Hartspiercellen zijn de samentrekkende cellen die het hart in staat stellen te pompen. Elke hartspiercel moet samentrekken in coördinatie met de aangrenzende cellen – bekend als een functioneel syncytium – om efficiënt bloed uit het hart te pompen. Als deze coördinatie verstoord raakt, kan het hart – ondanks de samentrekking van individuele cellen – helemaal niet meer pompen, zoals kan gebeuren bij hartritmestoornissen zoals ventrikelfibrilleren.[3]
Hartspiercellen zijn onder een microscoop ongeveer rechthoekig, met afmetingen van 100–150 μm bij 30–40 μm.[1] Individuele hartspiercellen zijn aan hun uiteinden verbonden door intercalaire schijven voor het vormen van lange vezels. Elke cel bevat myofibrillen, gespecialiseerde eiwitcontractiele vezels van actine en myosine die langs elkaar schuiven. Deze zijn georganiseerd in sarcomeren, de fundamentele contractiele eenheden van spiercellen. De regelmatige organisatie van myofibrillen in sarcomeren geeft hartspiercellen een gestreept of dwarsgestreept uiterlijk wanneer ze onder een microscoop worden bekeken, vergelijkbaar met skeletspieren. Deze strepen worden veroorzaakt door lichtere I-banden die voornamelijk uit actine bestaan, en donkerdere A-banden die voornamelijk uit myosine bestaan.[2]
Hartspiercellen bevatten T-tubuli, zakjes celmembraan die van het celoppervlak naar het binnenste van de cel lopen en die de contractie-efficiëntie helpen verbeteren. De meeste van deze cellen bevatten slechts één celkern (sommige hebben er twee), in tegenstelling tot skeletspiercellen die meerdere celkernen bevatten.
De Purkinjevezels geleiden snel elektrische signalen; kransslagaders brengen voedingsstoffen naar de hartspiercellen, en aders en het haarvatennetwerk voeren afvalstoffen af.[2]
Pacemakercel
Gespecialiseerde gemodificeerde langwerpige hartspiercellen, pacemakercellen genoemd, bepalen het ritme van de hartcontracties. De pacemakercellen zijn slechts zwak contractiel zonder sarcomeren en zijn via gap junctions verbonden met aangrenzende contractiele cellen.[4] Ze bevinden zich in de sinusknoop (de primaire pacemaker) op de wand van het rechter atrium, vlakbij de ingang van de vena cava superior.[5] Andere pacemakercellen bevinden zich in de atrioventriculaire knoop (secundaire pacemaker).
Pacemakercellen geleiden de impulsen die verantwoordelijk zijn voor het kloppen van het hart. Ze zijn verspreid over het hart en zijn verantwoordelijk voor verschillende functies. Ten eerste zijn ze verantwoordelijk voor het spontaan kunnen genereren en uitzenden van elektrische impulsen. Ze moeten ook elektrische impulsen van de hersenen kunnen ontvangen en erop kunnen reageren. Ten slotte moeten ze elektrische impulsen van cel naar cel kunnen overbrengen.[6] Pacemakercellen in de sinusknoop en de atrioventriculaire knoop zijn kleiner en geleiden met een relatief lage snelheid tussen de cellen. Gespecialiseerde geleidende cellen in de bundel van His en de Purkinjevezels hebben een grotere diameter en geleiden signalen met een hoge snelheid.[7]
Stationaire macrofagen
Tussen de hartspiercellen bevinden zich talrijke stationaire macrofagen, maar deze zijn veel kleiner. Gemiddeld is elke hartspiercel verbonden met vijf macrofagen, die dienen voor het handhaven van de weefselhomeostase en immuunbewaking. Ze nemen ook beschadigde of disfunctionele mitochondriën op, die worden vrijgegeven door de hartspiercellen, ingekapseld in exosomen en door de macrofagen via autofagie afgebroken. De exosomen zijn gelabeld met fosfatidylserine, wat de MerTK-receptor (myeloïde-epitheliale-reproductieve tyrosinereceptor) van de macrofagen activeert, die essentieel is voor de opname van exosomen en tevens een belangrijke rol speelt bij weefselgenezing na een hartinfarct.[8]
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Cardiac mussle#Microanatomy op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- 1 2 M., Bers, D. (2001). Excitation-contraction coupling and cardiac contractile force, 2nd. Kluwer Academic Publishers, Dordrecht. ISBN 978-0792371588.
- 1 2 3 Stevens, Alan (1997). Human histology, Lowe JS, 2nd. Mosby, London. ISBN 978-0723424857.
- ↑ Camm AJ, Lüscher TF, Serruys PW (2009). The ESC textbook of cardiovascular medicine, 2nd. Oxford University Press, Oxford. ISBN 9780199566990.
- ↑ Neil A. Campbell (2006). Biology : concepts & connections, 5th. Pearson/Benjamin Cummings, San Francisco, 473. ISBN 0-13-193480-5.
- ↑ Kashou AH, Basit H, Chhabra L, Physiology, Sinoatrial Node (SA Node). StatPearls (January 2020). Geraadpleegd op 10 May 2020.
- ↑ Anatomy and Physiology of the Heart.
- ↑ Standring, Susan (2016). Gray's anatomy: the anatomical basis of clinical practice, Forty-first. Elsevier, Philadelphia, p. 139. ISBN 9780702052309.
- ↑ Elizabeth M. McNally: Cardiac Macrophages — Keeping the Engine Running Clean New England Journal of Medicine 2020, Band 383, Ausgabe 25 vom 17. Dezember 2020, Seiten 2474–2476, DOI: 10.1056/NEJMcibr2030271