CRISPR
| CRISPR | ||||
|---|---|---|---|---|
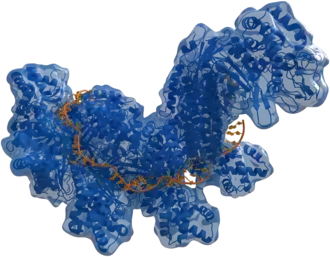 | ||||
Het CRISPR-eiwit Cas (blauw) gebonden aan enkelstrengs-DNA (oranje) | ||||
| Identificatie | ||||
| Organisme | Escherichia coli | |||
| Symbool | CRISPR | |||
| PDB-codes | 4QYZ | |||
| Externe identificaties | ||||
| UniProt | P38036 | |||
| Entrez | 947229 | |||
| ||||
Crispr,[1] in jargon vanuit het Engels vaak als CRISPR gespeld, een afkorting van het Engelse clustered regularly interspaced short palindromic repeats, vormt een cruciaal onderdeel van het verdedigingsmechanisme van bacteriën en archaea tegen virussen. Het systeem bestaat uit specifieke DNA-sequenties in het prokaryotisch genoom, die bacteriën gebruiken om virussen te herkennen en te neutraliseren.[2] CRISPR-sequenties bestaan uit korte, regelmatig herhaalde basenreeksen van 21–48 nucleotiden, die elk worden gescheiden door zogenaamde spacers: stukjes DNA die afkomstig zijn van eerdere virale infecties. Op deze manier functioneert het CRISPR-systeem als een moleculair 'geheugen' van eerdere infecties.
Het CRISPR-systeem werkt in combinatie met het enzym Cas9 (en andere Cas-eiwitten bij verschillende CRISPR-types), dat het virale DNA kan knippen op locaties die overeenkomen met de spacers. Dit mechanisme lijkt qua werking op RNA-interferentie dat voorkomt bij eukaryoten, waarbij ook specifieke basenreeksen worden herkend en afgebroken. Door de enorme specificiteit en veelzijdigheid hebben onderzoekers het CRISPR/Cas-systeem kunnen omzetten in een krachtige en relatief eenvoudige genetische technologie, waarmee men gerichte veranderingen kan maken in het erfelijk materiaal van een levend organisme.[3]
CRISPR is wijdverspreid onder prokaryoten: CRISPR-sequenties zijn aangetoond bij ruim 40% van de vastgestelde bacteriële genomen, en bij ongeveer 85% van de archaeale genomen.[4] Er bestaan verschillende types CRISPR-systemen (Type I, II en III), elk met unieke Cas-eiwitten en werkingsmechanismen. Onderzoek in bacteriën heeft duidelijk gemaakt dat het niet alleen een verdedigingsrol heeft; sommige soorten gebruiken CRISPR-sequenties ook voor regulatie van hun eigen genexpressie en communicatie met andere cellen.[2]
Ontdekking en naamgeving
Francisco Mojica was de eerste onderzoeker die in 1993 karakteriseerde wat nu een CRISPR-plaats wordt genoemd.[5] Een deel van de volgorde werd eerder al gerapporteerd door Yoshizumi Ishino bij zijn onderzoek naar E. coli in 1987. Mojica beschreef de volledige gen-volgorde-herhalingen in de archaeale organismen Haloferax en Haloarcula-soorten, en onderzocht hun functie. Hij zette het onderzoek naar deze volgorden gedurende de jaren negentig voort, en in 2000 herkende Mojica dat wat was gerapporteerd als ongelijksoortige herhalingsvolgorden, in feite een gemeenschappelijke reeks kenmerken deelden, nu bekend zijn als de kenmerken van CRISPR-volgorden. Hij bedacht de term CRISPR in correspondentie met Ruud Jansen van de Universiteit Utrecht en stelde de afkorting Clustered Regularly Interspaced Short Palindromic Repeats (CRISPR) voor.[6][7]
De herhaalde DNA-codes van CRISPR werden voor het eerst gezien in de jaren 1980 in E. coli.[8] Wetenschappers probeerden toen een specifiek gen van E. coli te onderzoeken, waarbij het opviel dat eenzelfde stukje DNA zich steeds herhaalde. In 2007 werd de functie van CRISPR-cas9 bevestigd toen duidelijk werd dat de bacterie S. thermophilus resistentie kan ontwikkelen tegen een bacteriofaag nadat er een fragment van het genoom van het virus was toegevoegd aan het CRISPR-systeem.[9]
De wetenschappers Jennifer Doudna (Universiteit van Californië) en Emmanuelle Charpentier (Max Planck Institut Berlijn) ontdekten in het laboratorium dat ze dit afweermechanisme zelf konden modificeren.[10] Ze konden heel precies op een door hen gewenste plek in het DNA knippen en plakken. In januari 2013 publiceerde de wetenschapper Feng Zhang de eerste methode om CRISPR in het genoom van mensen en muizen te bewerken.[11]
Mechanisme
CRISPR en cas9 werken samen en spelen beide een aparte rol. CRISPR kan gezien worden als een enorme DNA-bibliotheek met steeds dezelfde korte stukjes van eigen DNA en ingebouwde stukjes DNA van een agressief virus, dat spacer DNA wordt genoemd. Het fungeert als een bacterieel immuunsysteem. Cas9 is een soort schaar die virus-DNA herkent en direct optreedt tegen dit gevaar door het virus-DNA kapot te knippen. Bacteriofagen zijn deze gevaarlijke virussen die bacteriën aanvallen door het plaatsen van hun eigen DNA in de bacteriën en zo de DNA- en eiwitsynthese overnemen. Als bacteriën de aanval overleven kunnen ze dit virus-DNA opbergen in de CRISPR-bibliotheek.
Telkens nadat de bacterie door een bacteriofaag is aangevallen maar de aanval overleeft, bewaart de bacterie een stukje van het virus-DNA in zijn bibliotheek. Cas9 gebruikt RNA-sequenties, overgeschreven uit de bibliotheek, om al het DNA in de bacterie te vergelijken. Cas9 scant al het DNA in de bacterie totdat het een match vindt tussen het nieuwe virus-DNA dat de bacterie is binnengedrongen en het DNA van die bacterie dat was opgeslagen in CRISPR. Als hetzelfde soort virus opnieuw aanvalt en er een 100%-match gevonden wordt, kan cas9 het DNA van het binnengedrongen virus kapot knippen en daarmee onschadelijk maken. Zo wordt de bacterie genetisch beschermd tegen het ooit eerder binnengedrongen virus.
Toepassingen
Wetenschappers ontdekten dat cas9 programmeerbaar is en in elk soort cel werkt. Zo kunnen stukken DNA makkelijk, snel, goedkoop en precies worden bewerkt in allerlei soorten cellen. CRISPR-cas9 kan genen aan- of uitzetten en bewerken in planten, dieren en mensen.[12][13] In 2015 werd CRISPR-cas9 in het laboratorium gebruikt om het hiv-virus uit levende cellen van patiënten te knippen, om te laten zien dat het mogelijk is. De verwachting was dat CRISPR-cas9 niet alleen hiv maar ook andere retrovirussen die zich verstoppen in DNA zou kunnen bestrijden. Mogelijk zou CRISPR in de toekomst kanker kunnen bestrijden door immuuncellen kanker te laten opsporen.
Een onderzoeker van Harvard David Liu en collega's publiceerden in 2017 de techniek van 'base editing'. Hierbij kan een coderende 'A' gericht in het gen worden opgespoord en omgezet in een 'G', Omgekeerd lukt ook en dit alles zonder de DNA-streng te hoeven openknippen.[14] Dit deden ze door een tRNA-deaminase los te laten op een 'A' in het genetisch materiaal, die zo werd omgezet in een 'G' zonder het gen open te knippen.[15][16]
Zie ook
- Questions and Answers about CRISPR, Broad Institute
- CRISPR/Cas9 and Targeted Genome Editing: A New Era in Molecular Biology, New England Biolabs, Inc.
- Stephen Wilson. Potential Contributions of Bioartists to Research
- Nick Bostrom (2003). Human Genetic Enhancements: A Transhumanist Perspective. The Journal of Value Inquiry 37: 493.
- Wim Köhler. Worden er straks alleen nog perfecte baby’s geboren?, NRC.nl (30 september 2016)
- ↑ woordenlijst.org. woordenlijst.org. Geraadpleegd op 21 september 2025.
- 1 2 (en) Barrangou R (2015). The roles of CRISPR-Cas systems in adaptive immunity and beyond. Current Opinion in Immunology 32: 36–41. PMID 25574773. DOI: 10.1016/j.coi.2014.12.008.
- ↑ (en) Wang JY, Doudna JA. (2023). CRISPR technology: A decade of genome editing is only the beginning. Science 379. DOI: 10.1126/science.add8643.
- ↑ (en) Pinilla-Redondo R, Russel J, Mayo-Muñoz D, Fineran PC, Sørensen SJ. (2022). CRISPR-Cas systems are widespread accessory elements across bacterial and archaeal plasmids. Nucleic Acids Research 50 (8): 4315–4328. PMID 34606604. PMC 9071438. DOI: 10.1093/nar/gkab859.
- ↑ Francis Mojica: The Modest Microbiologist Who Discovered and Named CRISPR. Gearchiveerd op 4 juni 2023.
- ↑ Biological significance of a family of regularly spaced repeats in the genomes of Archaea, Bacteria and mitochondria
- ↑ Nobelprijs scheikunde voor techniek waarmee we –‘poef! – opeens alles genetisch kunnen veranderen’. Gearchiveerd op 6 februari 2023.
- ↑ Wat is CRISPR/Cas9 en waarom heeft iedereen het er opeens over?. Gearchiveerd op 2 april 2019.
- ↑ Science: CRISPR provides acquired resistance against viruses in prokaryotes. Gearchiveerd op 6 mei 2020.
- ↑ Jennifer Doudna: ‘I have to be true to who I am as a scientist’ . Gearchiveerd op 5 april 2023.
- ↑ How CRISPR pioneer Feng Zhang would use his invention on himself . Gearchiveerd op 29 maart 2023.
- ↑ In overheidspublicaties gespeld als 'CRISPR/Cas9
- ↑ 2017D26107 INBRENG VERSLAG VAN EEN SCHRIFTELIJK OVERLEG
- ↑ Wim Köhler. Uitroeien van eenvoudige erfelijke ziekten weer stap dichterbij met CRISPR-Cas, NRC.nl (27 oktober 2017). Gearchiveerd op 30 januari 2023.
- ↑ Programmable base editing of A•T to G•C in genomic DNA without DNA cleavage, Nature DOI:10.1038/nature24644
- ↑ Peter Reuell. A step forward in DNA base editing, Harvard Gazette (25 oktober 2017). Gearchiveerd op 22 mei 2023.