Bariumferraat(VI)
| Bariumferraat | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
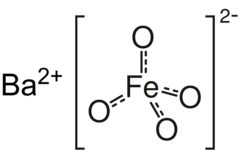 | ||||
Structuurformule van bariumferraat | ||||
Bariumferraatpoeder | ||||
| Algemeen | ||||
| Chemische formule | BaFeO4 | |||
| IUPAC-naam | bariumtetraoxidoferraat(VI) | |||
| Andere namen | bariumferraat(VI), bariumijzertetraoxide | |||
| Molaire massa | 257,1846 g/mol | |||
| CAS-nummer | 13773-23-4 | |||
| Wikidata | Q413900 | |||
| Beschrijving | Bruine vaste stof | |||
| Vergelijkbaar met | kaliumferraat(VI) | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| EG-Index-nummer | 056-002-00-7 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | bruin | |||
| Onoplosbaar in | water | |||
| Geometrie en kristalstructuur | ||||
| Kristalstructuur | tetragonaal | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Bariumferraat of bariumtetraoxidoferraat(VI) is een anorganische verbinding van barium en ijzer, met als structuurformule Ba[FeO4]. De stof komt voor als een kastanjebruine vaste stof, die onoplosbaar is in water. Bariumferraat is een sterke oxidator door de aanwezigheid van het oxiderende zeswaardig ijzer.[1] De aanwezigheid van twee ongepaarde elektronen in het ferraat(VI)ion maakt de stof paramagnetisch.[2] De stof is isostructureel met met een tetraëdrisch -ion.[3]
Synthese
Bariumferraat kan worden bereid uit een reactie van kaliumferraat(VI) en bariumchloride (dihydraat). Hierbij wordt een 86,5% zuivere bariumferraat verkregen.
Een alternatieve methode is de oxidatie van ijzer met kaliumnitraat tot oplosbaar kaliumferraat(VI):
Kaliumferraat wordt neergeslagen met bariumchloride:[4]
Reacties
Bariumferraat(VI) is de meest stabiele ferraat(VI)-verbinding. Het wordt ontleed door alle water-oplosbare zuren, inclusief koolzuur. Als door een suspensie van gehydrateerd koolstofdioxide geleid wordt, ontleed de verbinding compleet in bariumcarbonaat, ijzer(III)hydroxide en zuurstof:
Toepassingen
Bariumferraat vindt toepassing in de organische synthese als oxidator (het is sterker oxiderend dan kaliumpermanganaat).[5] Het vindt ook toepassing als kathode in de super-ijzerbatterij.[6]
- ↑ J. G. R. Briggs. (2005). Longman A-level course in chemistry (4th ed.) pag.: 536 – Pearson Education (South Asia) ISBN 978-981-4105-08-8
- ↑ Egon Wiberg, Nils Wiberg, Arnold Holleman. (2001). Inorganic chemistry pag.: 1457–1458 – Academic Press ISBN 978-0-12-352651-9
- ↑ A.F. Wells. (1986). Structural inorganic chemistry (5th ed.) – Clarendon Press (Oxford, Oxfordshire) ISBN 978-0-19-855370-0
- ↑ (en) J. R. Gump, W. F. Wagner & J. M. Scheyer - Preparation and Analysis of Barium Ferrate(VI), Analytical chemistry, 1954
- ↑ Firouzabadi, H., Mohajer, D. & Entezari-moghaddam, M. (1986). Barium Ferrate Monohydrate BaFeO4, H2O, A Versatile Reagent for the Oxidation of Organic Compounds under Aprotic Condiiton. Synthetic Communications: An International Journal for Rapid Communication of Synthetic Organic Chemistry, 16(6), 723-731. doi:10.1080/00397918608057745
- ↑ https://web.archive.org/web/20110105163958/http://www.reade.com/Products/Other_Compounds/ferrate.html