Alvleeskliervoorlopercel

Alvleeskliervoorlopercellen zijn multipotente stamcellen afkomstig uit het zich ontwikkelende endoderm van de voordarm. Deze cellen kunnen differentiëren tot de specifieke voorlopercellen die verantwoordelijk zijn voor de ontwikkeling van de alvleesklier.[1][2]
Ze vormen zowel endocriene als exocriene cellen. Exocriene cellen vormen de acinaire cellen en de ductale cellen (ductale cellen: epitheelcellen van de alvleesgang). De endocriene cellen vormen de bètacellen die insuline aanmaken, alfacellen die glucagon afscheiden, deltacellen die somatostatine afscheiden en de PP-cellen die pancreas polypeptide afscheiden.[3]
Ontwikkeling
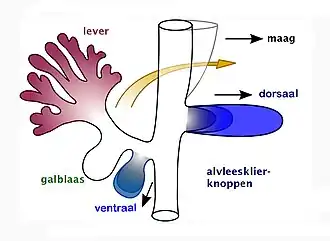
De alvleesklier is een orgaan van endodermale oorsprong. Het alvleesklierweefsel ontstaat vanuit de dorsale en ventrale delen van de achterste voordarm. Ze zijn te zien bij E9.0 tot E9.5 (embryonale dagen vanaf de bevruchting) tijdens de embryonale ontwikkeling. Fusie van deze knoppen vindt plaats tijdens de rotatie van de zich ontwikkelende darm. De gefuseerde en ontwikkelde alvleesklier bestaat uit cellen die alvleesklierenzymen afscheiden (exocriene cellen), cellen die spijsverteringsenzymen transporteren (ductale cellen: epitheelcellen van de alvleesgang) en hormoonproducerende cellen (endocriene cellen). Deze endocriene cellen ontwikkelen zich in afzonderlijke gebieden binnen de alvleesklier, de zogenaamde eilandjes van Langerhans.
Bij mensen kan de dorsale knop 26 dagen na de bevruchting worden waargenomen. De eilandcellen kunnen echter pas 52 dagen na de bevruchting worden waargenomen. De ontwikkeling van bètacellen gaat vooraf aan de ontwikkeling van andere endocriene cellen in de eilandjes. Alle eilandcellen kunnen bij de mens in het eerste trimester worden waargenomen. Deze variatie in de ontwikkeling van subtypen eilandcellen is te wijten aan differentiële genexpressie en inductiepaden van voorlopercellen.[4]
Locaties
Experimenten met genetische afstammingslijnen zijn uitgevoerd door verschillende onderzoeksgroepen om aan te tonen dat de celclusters afkomstig uit de zich ontwikkelende voordarm een transcriptiefactor genaamd PDX1 tot expressie brengen. Deze transcriptiefactor is aangetoond als aanleiding voor de multipotente stamcellijnen die bijdragen aan de endocriene, exocriene en ductale cellen van de alvleesklier. Deze cellen blijken zich ruimtelijk te bevinden aan de top van de vertakkende alvleesklierboom. Later blijkt dat deze cellen afkomstig zijn van de dorsale knop van de zich ontwikkelende alvleesklier.
PDX1 wordt geaccepteerd als de vroegste marker voor alvleesklierdifferentiatie. PDX1 is aangetoond een marker te zijn voor alle alvleesklier- en middendarmvoorlopercellen. De expressie van PDX1 is empirisch bewezen en stimuleert de zich ontwikkelende alvleesklier na het knopstadium, waarin twee knoppen (dorsaal en lateraal) van de onvolgroeide alvleesklier zich ontwikkelen. Notch-signalering blijkt het aantal exocriene en endocriene cellen in de alvleesklier te reguleren, maar niet zonder de aanwezigheid van PDX1.[5][6] Notch-signalering maakt de toename van alvleeskliervoorlopercellen mogelijk via laterale inhibitie.[7]
Er is aangetoond dat deze cellen 28 genen hebben die de celcyclus reguleren, wat aantoont dat het proliferatieve cellen zijn die het vermogen hebben om meerdere celpopulaties in de alvleesklier te vervangen en te laten ontstaan.[8][9]
Regulering van de vorming van de alvleeskliervoorlopercel

Het is aangetoond dat alvleeskliervoorlopercellen ontstaan door de vroege expressie van het gen MNX1/HLXB1. Expressie van MNX1 is belangrijk gebleken voor de ontwikkeling van dorsaal PDX1 en fungeert daarom als een noodzakelijke transcriptiefactor voor de specificatie van het endoderm van de voordarm tot PDX1-expressieve alvleeskliervoorlopercellen. Evenzo is een andere set genen, GATA4 en HNMF1b/TCF2, vereist voor de ontwikkeling van de ventrale knop van de zich ontwikkelende alvleesklier. Deze genen reguleren de expressie van MNX1 in de ventrale knop, wat leidt tot de ontwikkelingsspecificatie van de alvleeskliervoorlopercellen die PDX1 tot expressie brengen. Eén gen, Onecut1/HNF6, is ook verantwoordelijk voor de tijdige expressie van PDX1 in zowel de ventrale als de dorsale knoppen. De expressie van dit eiwit draagt dus ook bij aan de vorming van deze alvleeskliervoorlopercellen die PDX1 tot expressie brengen. Het is belangrijk om hierbij op te merken dat de zich ontwikkelende dorsale en ventrale knoppen worden gekarakteriseerd als endoderm en pas bij de expressie van PDX1 (de specificatie van endoderm tot een multipotente stamcelstatus) vindt de overgang van endoderm naar alvleeskliervoorlopercel plaats.
Het variabele aantal genen toont de verschillende routes van inductie van het zich ontwikkelende endoderm, intrinsiek binnen het endoderm (bijvoorbeeld via Notch-signalering) of vanuit het aangrenzende cardiale mesoderm (remming van Sonic Hedgehog-proteïne door fibroblastgroeifactor).[8][9]
Het onderscheid tussen alvleeskliervoorlopercellen en levervoorlopercellen is ook opmerkelijk, aangezien Hhex1 verantwoordelijk is voor het ontstaan van alvleeskliervoorlopercellen. Bij afwezigheid van HHEX (bij dubbelnegatieve HHEX-muizen) ontwikkelt de lever zich wel, maar niet de alvleesklier, wat aantoont dat Hhex divergente specificatie van een alvleeskliervoorlopercel mogelijk maakt in plaats van de vorming van een levervoorlopercel.[7]
Ontwikkeling cellijnen
Alvleeskliervoorlopercellen kunnen differentiëren tot zowel endocriene als exocriene voorlopercellen.[10]
Endocriene cellijn
De endocriene voorlopercellen vormen een groep voorlopercellen die zich ontwikkelen tot alle endocriene cellen in de alvleesklier. Endocriene cellijnen ontwikkelen zich tot deltacellen, PP-cellen, epsiloncellen, bètacellen en alfacellen. Alfacellen produceren glucagon en bètacellen produceren insuline. Insuline en glucagon reguleren antagonistisch de glucosehomeostase in het zoogdierlichaam. PP-cellen produceren pancreas polypeptide, een regulator van endocriene en exocriene secreties in de alvleesklier en darmen. Deltacellen produceren somatostatine, een groeihormoonremmend hormoon dat een belangrijke functie heeft bij de regulering van de hormoonproductie vanuit de adenohypofyse. Epsiloncellen produceren ghreline (hongerhormoon), een neuropeptide dat inwerkt op het hypothalamische centrum van de hersenen, waar het samenwerkt met GHSR (ghrelinreceptoren die groeihormoonsecretie bevorderen) en betrokken is bij het hongergevoel.[11]
Exocriene cellijn
De exocriene voorlopercel ontwikkelt zich tot voorlopercellen die amylase tot expressie brengen. Deze cellen kunnen vervolgens in weefsel worden geïdentificeerd als secretoir van aard en dragen bij aan de productie van alvleesklierenzymen.[12]
Ductale cellijn
De ductale voorlopercellen zijn een groep voorlopercellen die zich in de alvleesklier ontwikkelen tot ductale cellen. Deze cellen bekleden de afvoergangen en zijn ook afkomstig van alvleeskliervoorlopercellen.[13][14]
Transcriptiefactoren
De endodermale voorlopercellen blijken HNF6 en HNF1b tot expressie te brengen en zijn daarom HNF6+/HNF1b+ cellen. Door de onderdrukking van Sonic Hedgehog-signalering ontwikkelen alvleeskliervoorlopercellen zich en ontstaan er meerdere cellijnen. Alvleeskliervoorlopercellen zijn NKX2.2+/NKX6.1+/P48+ cellen.[15]
Endocriene cellen
Endocriene voorlopercellen ontwikkelen zich vanuit alvleeskliervoorlopercellen onder invloed van NGN3. Deze celbestemming is te danken aan de expressie van SOX9 en de onderdrukking van Notch-signalering. Alvleeskliervoorlopercellen zijn daarom NGN3+/NeuroD+/IA1+/ISL1+/PAX6+ cellen. Deze cellen ontwikkelen zich vervolgens tot bètacel-pro-voorlopercellen onder invloed van PAX4. Bètacel-pro-voorlopercellen zijn MAFB+/PDX1+/NKX2.2+-cellen. Deze bètacel-pro-voorlopercellen blijken bètacel-voorlopercellen te vormen die PAX1 tot expressie brengen.[16] Ten slotte rijpen bètacel-voorlopercellen uit tot volwassen bètacellen, namelijk PDX1+/NKX2.2+/NKX6.1+/PAX6+/NeuroD+/MAFA+.[17]
Endocriene voorlopercellen ontwikkelen zich ook tot deltacel-pro-voorlopercellen die PAX4 en PAX6 tot expressie brengen. Ze vormen vervolgens SOM+ deltacel-voorlopercellen. Deze deltacel-voorlopercellen rijpen uit tot deltacellen, namelijk BRN+/PAX6+.[18]
Daarnaast vormen endocriene voorlopercellen ook NKX2.2+ PP-cel-pro-voorlopercellen, die vervolgens PP+ (pancreas polypeptide)-voorlopercellen en later PP-cellen vormen. Endocriene voorlopercellen zijn ook verantwoordelijk voor de vorming van epsiloncellen.[19]
Exocriene cellen
Deze voorlopercellen ontwikkelen zich uit alvleeskliervoorlopercellen en zijn P48+-cellen. Deze cellen ontwikkelen zich tot volwassen amylase+/P48+-exocriene cellen.[20]
Ductale cellen
Deze cellen brengen HNF6 tot expressie en zijn afkomstig van alvleeskliervoorlopercellen. Ze zijn bijzonder omdat hun morfologie en kenmerken vergelijkbaar zijn met die van de alvleeskliervoorlopercel. Voorlopercellen van ductale cellen brengen HNF6 tot expressie voordat ze zich ontwikkelen tot de volwassen ductale cel van de alvleesklier.[21]
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Pancreatic progenitor cell op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- ↑ Ku, H. T. (2008). Pancreatic progenitor cells—recent studies. Endocrinology 149 (9): 4312–4316. PMID 18535096. PMC 2553367. DOI: 10.1210/en.2008-0546.
- ↑ Noguchi, H (2010). Pancreatic stem/progenitor cells for the treatment of diabetes. Rev Diabet Stud 7 (2): 105–111. PMID 21060969. PMC 2989783. DOI: 10.1900/RDS.2010.7.105.
- ↑ Cabrera, O., berman, D.M., Kenyon, N.S., Ricordi, C., Berggren, P-O. (2006). The unique cytoarchitecture of human pancreatic islets has implications for islet cell function. PNAS 7 (103): 2334–2339. PMID 16461897. PMC 1413730. DOI: 10.1073/pnas.0510790103.
- ↑ Like, A. A., & Orci, L. (1972). Embryogenesis of the human pancreatic islets: a light and electron microscopic study. Diabetes, 21(Supplement 2), 511-534. http://diabetes.diabetesjournals.org/content/21/Supplement_2/511.abstract
- ↑ Apelqvist, Å., Li, H., Sommer, L., Beatus, P., Anderson, D. J. (1999). Notch signalling controls pancreatic cell differentiation. Nature 400 (6747): 877–881. PMID 10476967. DOI: 10.1038/23716.
- ↑ Kim, W., Shin, Y. K., Kim, B. J., Egan, J. M. (2010). Notch signaling in pancreatic endocrine cell and diabetes. Biochemical and Biophysical Research Communications 392 (3): 247–251. PMID 20035712. PMC 4152840. DOI: 10.1016/j.bbrc.2009.12.115.
- 1 2 Zaret, K. S. (2008). Genetic programming of liver and pancreas progenitors: lessons for stem-cell differentiation. Nature Reviews Genetics 9 (5): 329–340. PMID 18398419. DOI: 10.1038/nrg2318.
- 1 2 Jiang, F. X., Mehta, M., Morahan, G. (2010). Quantification of insulin gene expression during development of pancreatic islet cells. Pancreas 39 (2): 201–208. PMID 19812524. DOI: 10.1097/mpa.0b013e3181bab68f.
- 1 2 Jørgensen, M. C., Ahnfelt-Rønne, J., Hald, J., Madsen, O. D., Serup, P. (2007). An illustrated review of early pancreas development in the mouse. Endocrine Reviews 28 (6): 685–705. PMID 17881611. DOI: 10.1210/er.2007-0016.
- ↑ Kahan, B. W., Jacobson, L. M., Hullett, D. A., Ochoada, J. M., Oberley, T. D. (2003). Pancreatic precursors and differentiated islet cell types from murine embryonic stem cells an in vitro model to study islet differentiation. Diabetes 52 (8): 2016–2024. PMID 12882918. DOI: 10.2337/diabetes.52.8.2016.
- ↑ Márquez-Aguirre, A. L., Canales-Aguirre, A. A., Padilla-Camberos, E., Esquivel-Solis, H., Díaz-Martínez, N. E. (2015). Development of the endocrine pancreas and novel strategies for β-cell mass restoration and diabetes therapy. Brazilian Journal of Medical and Biological Research 48 (9): 765–76. PMID 26176316. PMC 4568803. DOI: 10.1590/1414-431X20154363.
- ↑ Burke, Z. D., Thowfeequ, S., Peran, M., Tosh, D. (2007). Stem cells in the adult pancreas and liver. Biochemical Journal 404 (2): 169–178. PMID 17488235. PMC 2715288. DOI: 10.1042/BJ20070167.
- ↑ Gu, G., Dubauskaite, J., Melton, D. A. (2002). Direct evidence for the pancreatic lineage: NGN3+ cells are islet progenitors and are distinct from duct progenitors. Development 129 (10): 2447–2457. PMID 11973276. DOI: 10.1242/dev.129.10.2447.
- ↑ Li, W. C., Rukstalis, J. M., Nishimura, W., Tchipashvili, V., Habener, J. F. (2010). Activation of pancreatic-duct-derived progenitor cells during pancreas regeneration in adult rats. Journal of Cell Science 123 (16): 2792–2802. PMID 20663919. PMC 2915881. DOI: 10.1242/jcs.065268.
- ↑ He, K. H., Juhl, K., Karadimos, M., El Khattabi, I., Fitzpatrick, C. (2014). Differentiation of pancreatic endocrine progenitors reversibly blocked by premature induction of MafA. Developmental Biology 385 (1): 2–12. PMID 24183936. PMC 3918466. DOI: 10.1016/j.ydbio.2013.10.024.
- ↑ Lin, C. L., Vuguin, P. M. (2012). Determinants of pancreatic islet development in mice and men: a focus on the role of transcription factors. Hormone Research in Paediatrics 77 (4): 205–213. PMID 22487552. DOI: 10.1159/000337219.
- ↑ Gasa, R., Mrejen, C., Leachman, N., Otten, M., Barnes, M. (2004). Proendocrine genes coordinate the pancreatic islet differentiation program in vitro. Proceedings of the National Academy of Sciences of the United States of America 101 (36): 13245–13250. PMID 15340143. PMC 516555. DOI: 10.1073/pnas.0405301101.
- ↑ Guz, Y., Montminy, M. R., Stein, R., Leonard, J., Gamer, L. W. (1995). Expression of murine STF-1, a putative insulin gene transcription factor, in beta cells of pancreas, duodenal epithelium and pancreatic exocrine and endocrine progenitors during ontogeny. Development 121 (1): 11–18. PMID 7867492. DOI: 10.1242/dev.121.1.11.
- ↑ Schaffer, A. E., Taylor, B. L., Benthuysen, J. R., Liu, J., Thorel, F. (2013). Nkx6. 1 controls a gene regulatory network required for establishing and maintaining pancreatic Beta cell identity. PLOS Genet 9 (1). PMID 23382704. PMC 3561089. DOI: 10.1371/journal.pgen.1003274.
- ↑ Mastracci, T. L., Sussel, L. (2012). The endocrine pancreas: insights into development, differentiation, and diabetes. Developmental Biology 1 (5): 609–628. PMID 22905335. PMC 3420142. DOI: 10.1002/wdev.44.
- ↑ Neoptolemos, J. P., Urrutia, R., Abbruzzese, J. L., & Büchler, M. W. (2010). Pancreatic cancer. New York, NY: Springer. ISBN 978-0-387-77498-5